Clear Sky Science · pt
AMPK é dispensável para as funções fisiológicas de podócitos e glomérulos, mas previne a fibrose glomerular em modelo experimental de diabetes
Por que as células filtrantes do rim importam no diabetes
Nossos rins filtram o sangue milhares de vezes por dia de forma silenciosa, e uma parte essencial desse filtro é composta por células chamadas podócitos. Essas células envolvem pequenos vasos sanguíneos em estruturas conhecidas como glomérulos, retendo proteínas no sangue enquanto permitem que resíduos e água passem para a urina. Este estudo faz uma pergunta aparentemente simples, mas com grandes implicações para pessoas com diabetes: um interruptor energético celular importante, chamado AMPK, realmente protege essas células filtrantes e evita a formação de cicatrizes no rim? A resposta é sutil — a AMPK não é necessária para a função renal do dia a dia, mas torna-se crucial quando o diabetes sobrecarrega o sistema.
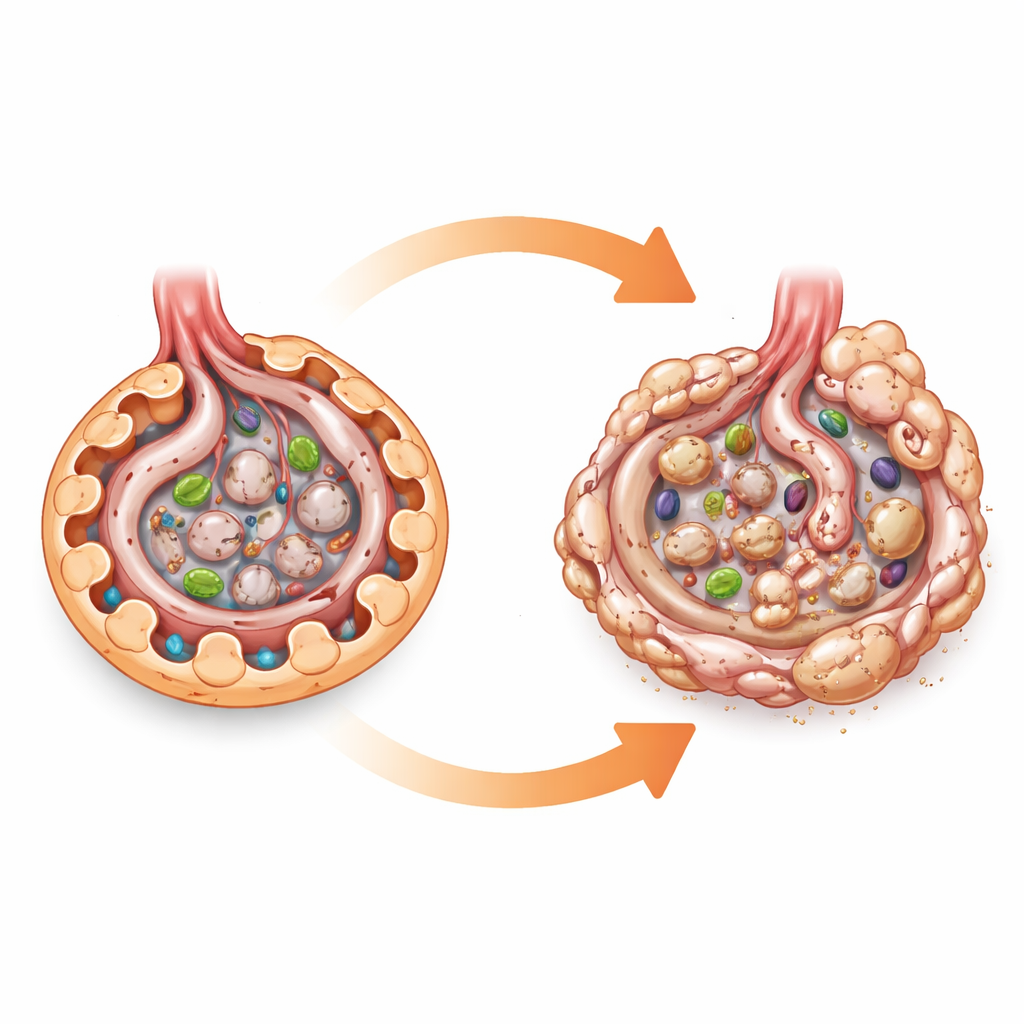
Um medidor de combustível celular sob o microscópio
A AMPK pode ser vista como um medidor de combustível celular. Quando a energia está baixa, ela ativa processos que queimam gordura e açúcar e apoia sistemas de limpeza, como a autofagia, que ajuda as células a reciclar componentes desgastados. Como o diabetes sobrecarrega as células renais com açúcar e nutrientes, muitos pesquisadores supuseram que uma redução na atividade da AMPK prejudica diretamente os podócitos e impulsiona a doença renal diabética. Grande parte dessa convicção veio de estudos em culturas celulares e de animais tratados com fármacos que ativam a AMPK, os quais podem ter muitos efeitos secundários. Para testar o papel da AMPK de forma mais direta, os autores criaram camundongos sem as duas subunidades principais da AMPK especificamente nos podócitos, mantendo a AMPK intacta no restante do corpo.
Rins surpreendentemente normais na ausência de AMPK
Quando esses camundongos geneticamente modificados foram acompanhados por dois anos com dieta normal, seus rins apresentaram aparência e função semelhantes aos de seus irmãos normais. O número de podócitos foi preservado, a estrutura fina dos glomérulos permaneceu intacta e exames de urina não mostraram perda excessiva de proteínas. Mesmo processos-chave que a AMPK costuma influenciar — como a via de crescimento chamada mTORC1 e o sistema interno de reciclagem celular — não foram visivelmente perturbados nesses podócitos. Isso sugere que, em um estado saudável e bem alimentado, os podócitos conseguem manter sua função sem depender da AMPK, talvez apoiando-se em vias alternativas que executam trabalhos semelhantes.
O diabetes revela fragilidades ocultas
O quadro mudou drasticamente quando o diabetes foi induzido, usando tanto um modelo tipo 1 quanto um modelo combinado de alta gordura com baixa dose de toxina que imita aspectos do diabetes tipo 2. Com os mesmos níveis elevados de glicose no sangue, camundongos sem AMPK nos podócitos desenvolveram lesão renal mais grave do que camundongos diabéticos normais. Seus glomérulos eram maiores e mais fibrosados, e apresentaram maior perda de albumina na urina, um sinal clínico importante de dano renal. Colorações detalhadas mostraram acúmulo mais intenso de colágeno e de proteínas de “estresse” nos glomérulos, indicando uma aceleração da fibrose glomerular — a substituição gradual do tecido filtrante delicado por cicatriz endurecida.
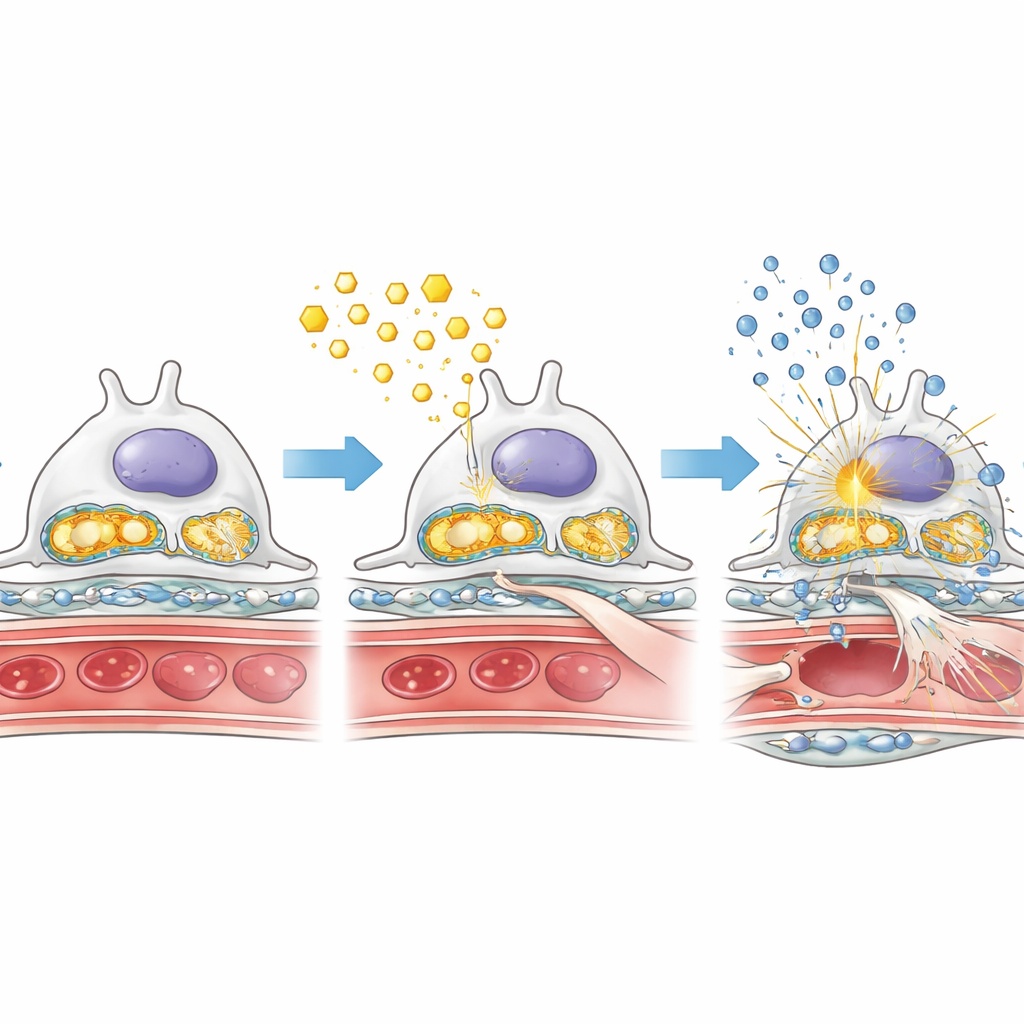
Sobrecarrega de gordura, usinas danificadas e alarmes inflamatórios
Para entender por que a falta de AMPK agravou o dano, os pesquisadores examinaram de perto como os podócitos lidavam com gorduras e açúcares em condições diabéticas. Em camundongos diabéticos sem AMPK nos podócitos, gotículas de gordura se acumularam nos glomérulos, enquanto uma enzima-chave para queimar ácidos graxos estava reduzida. Ao mesmo tempo, enzimas que promovem a quebra rápida de açúcar estavam mais ativas, sugerindo uma mudança para um metabolismo menos eficiente e mais “fermentativo” que pode favorecer a fibrose. As usinas de energia da célula — as mitocôndrias — também foram afetadas: suas proteínas de suporte estavam em menor quantidade e seu material genético vazou para o citosol. Esse DNA mitocondrial liberado parece ativar um sistema de alarme interno conhecido como via cGAS–STING, que por sua vez liga interruptores inflamatórios como NF‑κB e aumenta a produção de moléculas inflamatórias. Juntas, essas alterações criam uma mistura tóxica de sobrecarga lipídica, dano mitocondrial e inflamação crônica dentro do filtro renal.
Ondas dos podócitos para as células vizinhas
Os podócitos não trabalham isoladamente; eles ficam diretamente opostos às células endoteliais glomerulares, que revestem o lado sanguíneo do filtro. O estudo descobriu que, quando a AMPK dos podócitos estava ausente em diabetes, essas células endoteliais vizinhas estavam mais propensas a adotar um estado semelhante a fibroblastos, um processo chamado transição endotélio‑para‑mesenquimal. Nesse estado, elas contribuem de forma mais ativa para a formação de cicatriz. Essas células endoteliais mostraram as mesmas assinaturas metabólicas observadas nos podócitos: menor capacidade de queimar gordura e maior dependência da glicólise. Isso sugere que podócitos estressados podem indiretamente empurrar células vizinhas para comportamentos prejudiciais, amplificando a fibrose por todo o glomérulo.
O que isso significa para pessoas com diabetes
No dia a dia, os podócitos parecem capazes de funcionar sem muita ajuda da AMPK. Mas sob o estresse crônico do diabetes, a atividade residual da AMPK em podócitos normais age como um defensor silencioso, ajudando‑os a queimar gordura corretamente, proteger as mitocôndrias e manter os alarmes inflamatórios sob controle. Quando essa rede de segurança é removida, o manejo de gorduras e açúcares se desregula, as mitocôndrias se deterioram, vias inflamatórias são ativadas e a cicatrização se espalha pelo filtro renal. Esses achados sustentam a ideia de que terapias que estimulem suavemente a atividade da AMPK, ou imitem seus efeitos protetores sobre o metabolismo e a inflamação, poderiam ajudar a desacelerar ou prevenir a doença renal diabética — reforçando a resiliência dos podócitos e de seus vizinhos próximos em vez de depender apenas do controle da glicemia.
Citação: Srivastava, S.P., Kopasz-Gemmen, O., Kunamneni, A. et al. AMPK is dispensable for physiological podocyte and glomerular functions but prevents glomerular fibrosis in experimental diabetes. Cell Death Discov. 12, 204 (2026). https://doi.org/10.1038/s41420-026-03078-y
Palavras-chave: doença renal diabética, podócitos, AMPK, fibrose glomerular, metabolismo celular