Clear Sky Science · fr
L’AMPK est dispensable pour les fonctions physiologiques des podocytes et du glomérule mais prévient la fibrose glomérulaire dans un modèle expérimental de diabète
Pourquoi les cellules filtrantes du rein comptent dans le diabète
Nos reins filtrent silencieusement le sang des milliers de fois par jour, et une partie essentielle de ce filtre est constituée de cellules appelées podocytes. Ces cellules enserrent de minuscules vaisseaux sanguins dans des structures appelées glomérules, retenant les protéines dans le sang tout en laissant passer déchets et eau vers l’urine. Cette étude pose une question apparemment simple mais aux grandes implications pour les personnes atteintes de diabète : un interrupteur majeur de détection énergétique des cellules, nommé AMPK, protège‑t‑il réellement ces cellules filtrantes et empêche‑t‑il la cicatrisation du rein ? La réponse se révèle nuancée — l’AMPK n’est pas nécessaire au fonctionnement courant du rein, mais elle devient cruciale lorsque le diabète met le système à rude épreuve.
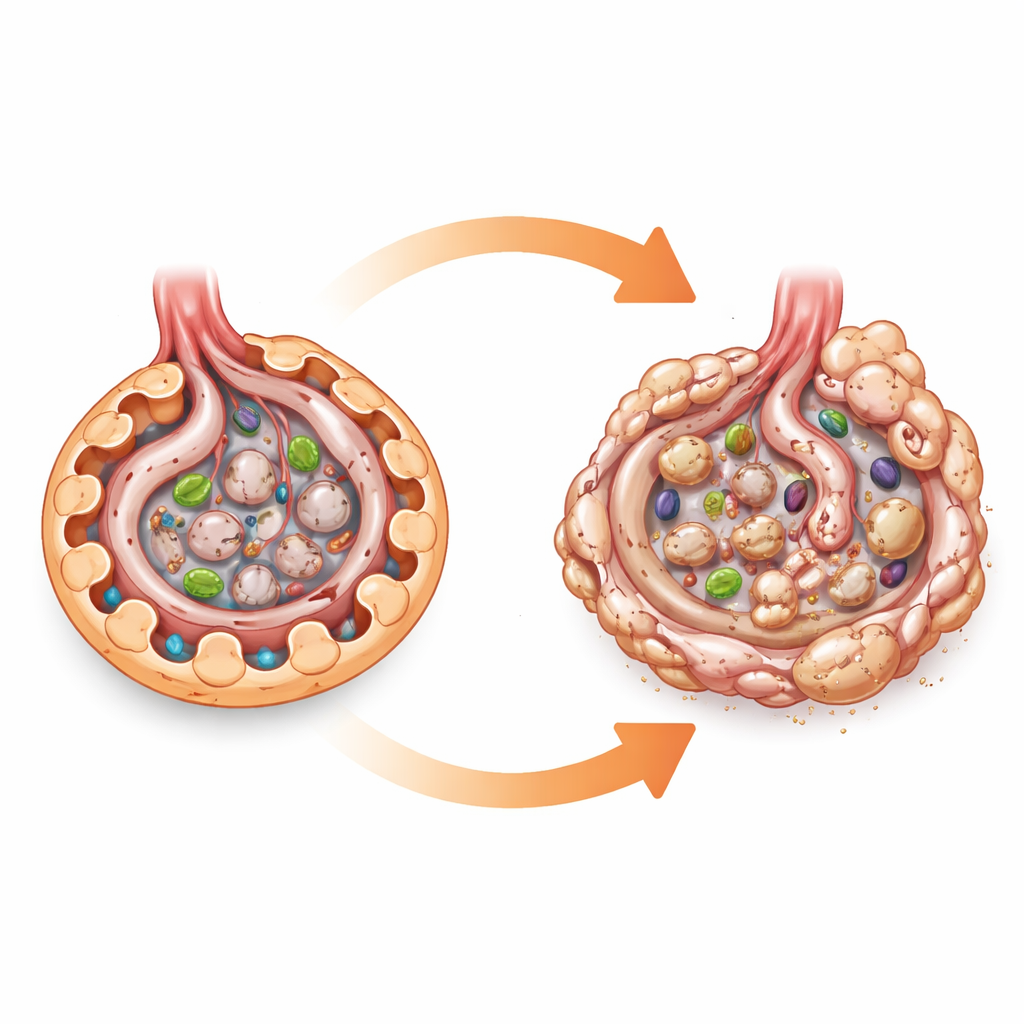
Une jauge de carburant cellulaire au microscope
On peut voir l’AMPK comme une jauge de carburant cellulaire. Quand l’énergie manque, elle active des processus qui brûlent graisses et sucres et soutient des systèmes de nettoyage comme l’autophagie, qui aide la cellule à recycler ses composants usés. Parce que le diabète surcharge les cellules rénales en sucres et nutriments, beaucoup de chercheurs ont supposé qu’une baisse de l’activité de l’AMPK nuit directement aux podocytes et conduit à la maladie rénale diabétique. La plupart de cette conviction provenait d’études en culture de cellules et d’animaux traités par des médicaments activant l’AMPK, qui peuvent avoir de nombreux autres effets. Pour tester le rôle de l’AMPK de façon plus propre, les auteurs ont conçu des souris dépourvues des deux sous‑unités majeures de l’AMPK spécifiquement dans les podocytes, tout en laissant l’AMPK intacte dans le reste de l’organisme.
Des reins étonnamment normaux en l’absence d’AMPK
Quand ces souris modifiées ont été suivies pendant deux ans avec une alimentation normale, leurs reins avaient l’aspect et le fonctionnement des reins de leurs congénères normaux. Le nombre de podocytes était préservé, la structure fine des glomérules restait intacte, et les analyses d’urine ne montraient pas de fuite protéique excessive. Même les processus clés que l’on sait influencés par l’AMPK — comme une voie de croissance appelée mTORC1 et le système interne de recyclage cellulaire — n’étaient pas visiblement perturbés dans ces podocytes. Cela suggère que, dans un état sain et bien nourri, les podocytes peuvent accomplir leur travail sans dépendre de l’AMPK, s’appuyant peut‑être sur des voies de secours qui remplissent des fonctions similaires.
Le diabète révèle des fragilités cachées
Le tableau a changé radicalement lorsque le diabète a été induit, en utilisant à la fois un modèle de type 1 et un modèle combinant alimentation riche en graisses et faible dose de toxine imitant des aspects du diabète de type 2. À niveaux glycémiques élevés identiques, les souris dépourvues d’AMPK dans les podocytes ont développé des lésions rénales plus sévères que les souris diabétiques normales. Leurs glomérules étaient plus volumineux et plus cicatrisés, et elles présentaient une fuite d’albumine vers l’urine plus importante, un signe clinique clé de lésion rénale. Des colorations détaillées ont montré un dépôt plus important de collagène et de protéines de « stress » dans les glomérules, indiquant une accélération de la fibrose glomérulaire — le remplacement progressif du tissu filtrant délicat par une cicatrice rigide.
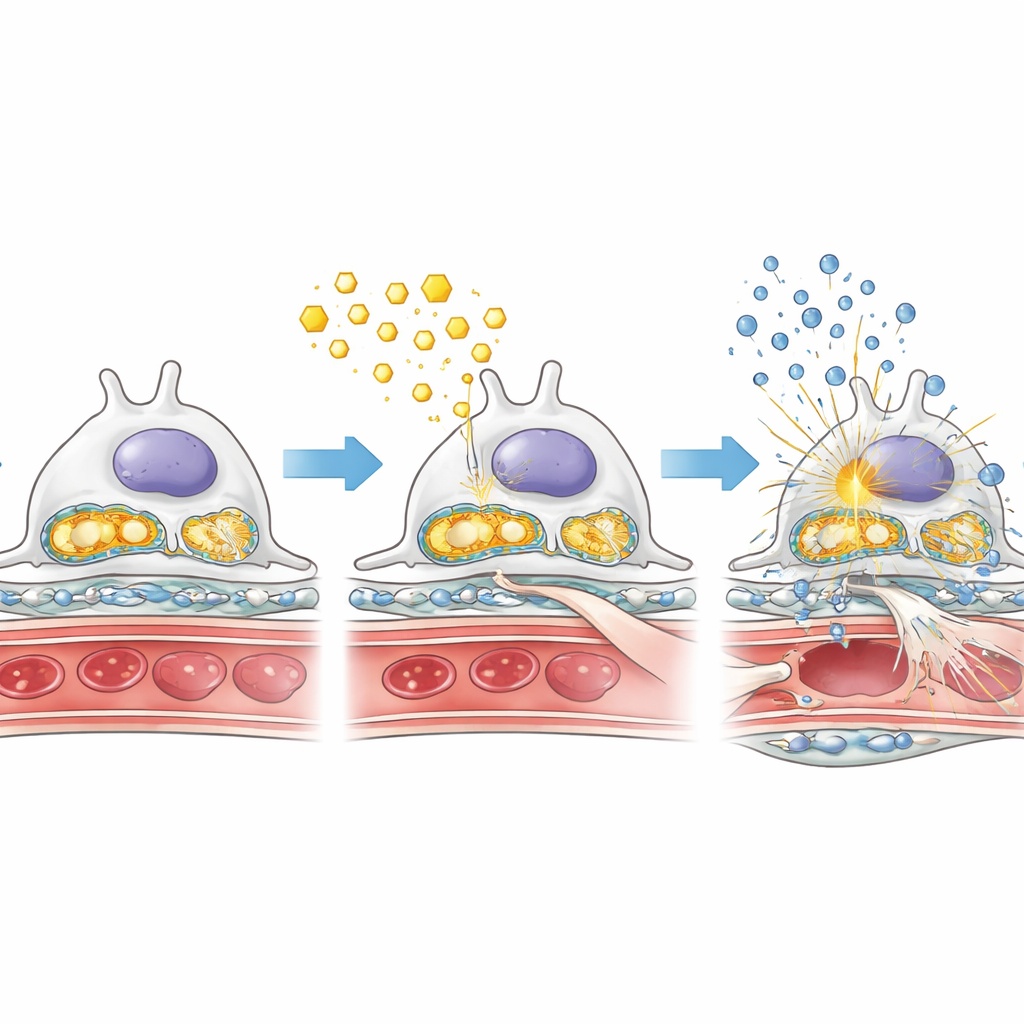
Surcharge lipidique, centrales énergétiques endommagées et signaux inflammatoires
Pour comprendre pourquoi l’absence d’AMPK aggravait les lésions, les chercheurs ont examiné de près la façon dont les podocytes traitaient les lipides et les sucres dans des conditions diabétiques. Chez les souris diabétiques sans AMPK podocytaire, des gouttelettes de graisse se sont accumulées dans les glomérules, tandis qu’une enzyme clé de la combustion des acides gras était réduite. Parallèlement, des enzymes favorisant la dégradation rapide des sucres étaient plus actives, suggérant un basculement vers un métabolisme moins efficace, plus « fermentaire », qui peut favoriser la cicatrisation. Les centrales énergétiques de la cellule — les mitochondries — étaient aussi affectées : leurs protéines de soutien étaient diminuées et leur matériel génétique fuyait dans le cytosol. Cet ADN mitochondrial libéré semble activer un système d’alarme interne connu sous le nom de voie cGAS–STING, qui à son tour déclenche des commutateurs inflammatoires comme NF‑κB et augmente la production de molécules inflammatoires. Ensemble, ces changements créent un mélange toxique de surcharge lipidique, de détérioration mitochondriale et d’inflammation chronique à l’intérieur du filtre rénal.
Ondes des podocytes aux cellules voisines
Les podocytes ne fonctionnent pas isolément ; ils sont directement en vis‑à‑vis des cellules endothéliales glomérulaires, qui tapissent le côté sanguin du filtre. L’étude a montré que, lorsque l’AMPK des podocytes faisait défaut en situation diabétique, ces cellules endothéliales voisines avaient davantage tendance à adopter un état de type fibroblaste, un processus appelé transition endothéliale‑vers‑mésenchyme. Dans cet état, elles contribuent plus activement à la formation de cicatrices. Ces cellules endothéliales présentaient les mêmes signatures métaboliques observées dans les podocytes : moins de capacité à brûler les graisses et plus de dépendance à la glycolyse. Cela suggère que des podocytes en détresse peuvent indirectement pousser les cellules voisines vers des comportements nocifs, amplifiant la fibrose dans l’ensemble du glomérule.
Qu’est‑ce que cela signifie pour les personnes atteintes de diabète
Dans la vie quotidienne, les podocytes semblent capables de fonctionner sans beaucoup d’aide de l’AMPK. Mais sous le stress chronique du diabète, l’activité résiduelle de l’AMPK dans les podocytes normaux devient un défenseur discret, les aidant à brûler correctement les graisses, à protéger leurs mitochondries et à maintenir les systèmes d’alerte inflammatoire sous contrôle. Lorsque ce filet de sécurité est supprimé, la gestion des lipides et des sucres déraille, les mitochondries se désagrègent, les voies inflammatoires s’enflamment et la cicatrisation se propage à travers le filtre rénal. Ces résultats soutiennent l’idée que des thérapies visant à stimuler modérément l’activité de l’AMPK, ou à en imiter les effets protecteurs sur le métabolisme et l’inflammation, pourraient aider à ralentir ou prévenir la maladie rénale diabétique — en renforçant la résilience des podocytes et de leurs voisins proches plutôt qu’en modifiant seulement la glycémie.
Citation: Srivastava, S.P., Kopasz-Gemmen, O., Kunamneni, A. et al. AMPK is dispensable for physiological podocyte and glomerular functions but prevents glomerular fibrosis in experimental diabetes. Cell Death Discov. 12, 204 (2026). https://doi.org/10.1038/s41420-026-03078-y
Mots-clés: maladie rénale diabétique, podocytes, AMPK, fibrose glomérulaire, métabolisme cellulaire