Clear Sky Science · nl
AMPK is niet noodzakelijk voor fysiologische podocyt- en glomerulaire functies maar voorkomt glomerulaire fibrose in experimentele diabetes
Waarom filtercellen van de nier belangrijk zijn bij diabetes
Onze nieren filteren stilletjes duizenden keren per dag bloed, en een cruciaal onderdeel van dat filter bestaat uit cellen die podocyten worden genoemd. Deze cellen wikkelen zich om kleine bloedvaatjes in structuren die glomeruli worden genoemd en houden eiwitten in het bloed terwijl afvalstoffen en water in de urine kunnen passeren. Deze studie stelt een bedrieglijk eenvoudige vraag met grote implicaties voor mensen met diabetes: beschermt een belangrijke energieregulerende schakel in cellen, genaamd AMPK, deze filtercellen echt en voorkomt het littekenvorming in de nier? Het antwoord blijkt genuanceerd te zijn — AMPK is niet nodig voor het dagelijkse nierwerk, maar wordt cruciaal wanneer diabetes het systeem belast.
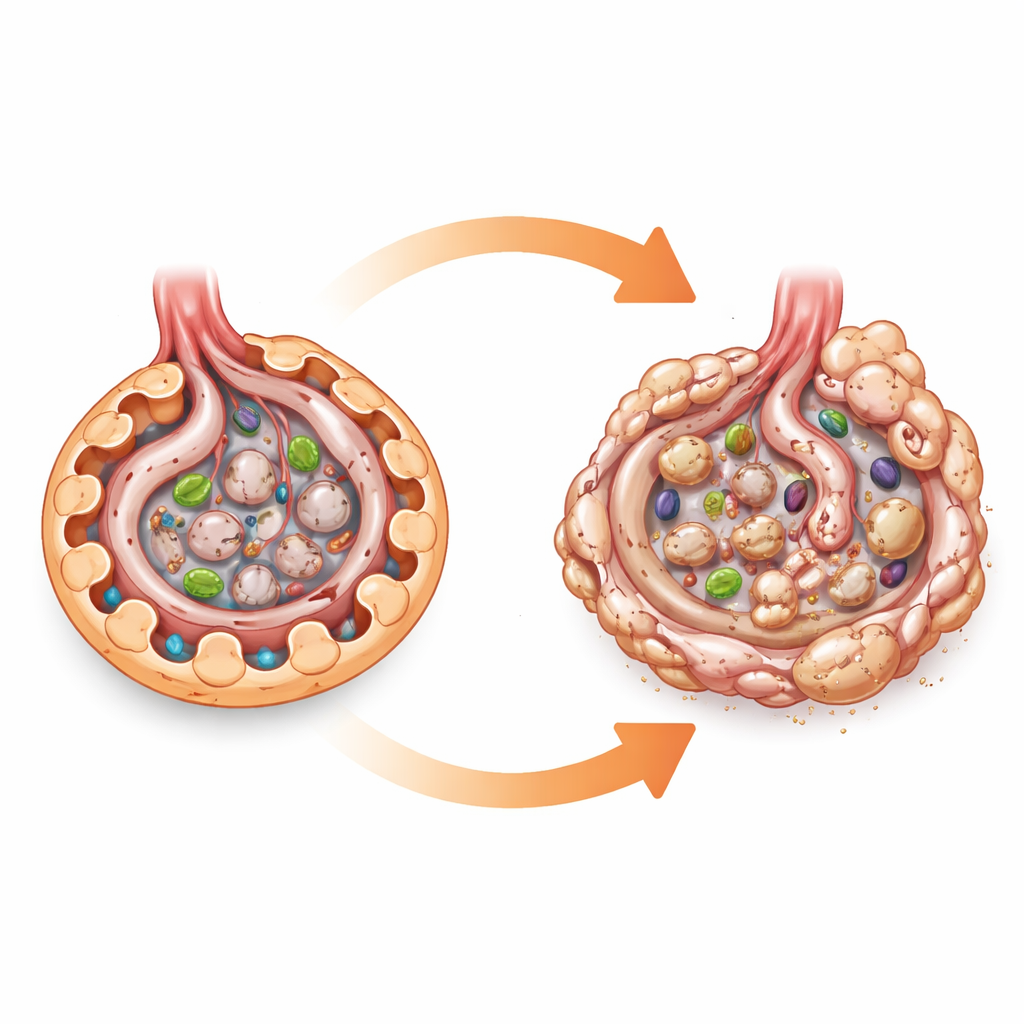
Een cellulair brandstofmeter onder de microscoop
AMPK kun je beschouwen als een cellulair brandstofmeter. Wanneer de energie laag is, schakelt het processen aan die vet en suiker verbranden en ondersteunt het opruimsystemen zoals autofagie, die cellen helpen versleten onderdelen te recyclen. Omdat diabetes niercellen overbelast met suiker en voedingsstoffen, hebben veel onderzoekers aangenomen dat een afname van AMPK-activiteit direct podocyten schaadt en de diabetische nierziekte aandrijft. Het grootste deel van dit geloof kwam uit kweekstudies en uit dierproeven met medicijnen die AMPK activeren, middelen die vaak meerdere effecten hebben. Om de rol van AMPK zuiverder te testen, maakten de auteurs muizen die beide belangrijke AMPK-subunits specifiek in podocyten misten, terwijl AMPK in de rest van het lichaam intact bleef.
Verrassend normale nieren bij afwezigheid van AMPK
Toen deze gemodificeerde muizen gedurende twee jaar op een normaal dieet werden gevolgd, zagen hun nieren er hetzelfde uit en functioneerden ze zoals die van hun normale nestgenoten. Het aantal podocyten bleef behouden, de fijne structuur van de glomeruli bleef intact en urinetests toonden geen overmatige eiwitlekkage. Zelfs belangrijke processen waarvan bekend is dat AMPK ze beïnvloedt — zoals een groeipad genaamd mTORC1 en het intracellulaire recyclingsysteem — waren in deze podocyten niet duidelijk verstoord. Dit suggereert dat podocyten in een gezonde, goed gevoede toestand hun werk kunnen blijven doen zonder op AMPK te vertrouwen, mogelijk door terug te vallen op reservepaden die vergelijkbare taken uitvoeren.
Diabetes onthult verborgen zwaktes
Het beeld veranderde scherp toen diabetes werd geïnduceerd, met zowel een type-1-achtig model als een gecombineerd high-fat model met lage dosis gif dat aspecten van type 2 diabetes nabootst. Onder dezelfde hoge bloedglucosewaarden ontwikkelden muizen zonder AMPK in podocyten ernstiger nierschade dan normale diabetische muizen. Hun glomeruli waren groter en meer verkleefd, en ze verloren meer albumine in de urine, een belangrijke klinische aanwijzing voor nierschade. Gedetailleerde kleuring toonde zwaardere ophoping van collageen en ‘stress’-eiwitten in de glomeruli, wat wijst op een versnelling van glomerulaire fibrose — de geleidelijke vervanging van delicaat filterweefsel door stug littekenweefsel.
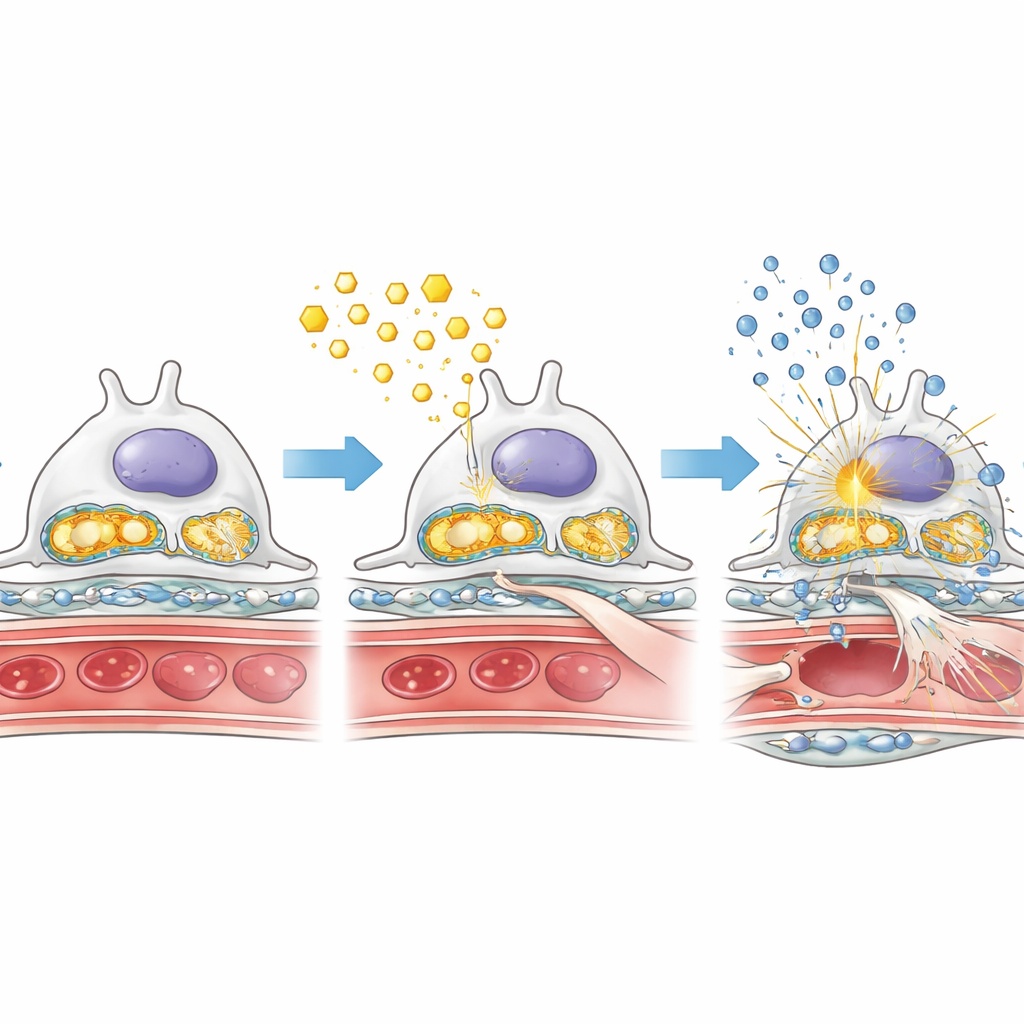
Vetoverload, beschadigde energiecentrales en ontstekingsalarmen
Om te begrijpen waarom het ontbreken van AMPK de schade verergerde, onderzochten de onderzoekers nauwkeurig hoe podocyten vetten en suikers verwerkten onder diabetische omstandigheden. In diabetische muizen zonder podocyt-AMPK stapelden vetdruppels zich op binnen de glomeruli, terwijl een sleuteleiwit voor het verbranden van vetzuren was verminderd. Tegelijkertijd waren enzymen die snelle suikerafbraak aansturen actiever, wat wijst op een verschuiving naar een minder efficiënte, meer ‘fermenterende’ stijl van metabolisme die fibrose kan bevorderen. De energiecentrales van de cel — de mitochondriën — werden ook aangetast: hun ondersteunende eiwitten waren lager en hun genetisch materiaal lekte in het celvocht. Dit gelekte mitochondriale DNA lijkt een intern alarmsysteem te activeren dat bekendstaat als de cGAS–STING-route, die op zijn beurt ontstekingsschakelaars zoals NF-κB activeert en de productie van ontstekingsmoleculen verhoogt. Samen creëren deze veranderingen een toxische mix van vetoverload, mitochondriale schade en chronische ontsteking in het nierfilter.
Golfbewegingen van podocyten naar naburige cellen
Podocyten werken niet geïsoleerd; ze liggen direct tegenover glomerulaire endotheelcellen, die de bloedzijde van het filter bekleden. De studie ontdekte dat wanneer podocyt-AMPK ontbrak bij diabetes, deze naburige endotheelcellen eerder de neiging hadden om een fibroblastachtige toestand aan te nemen, een proces dat endotheel‑naar‑mesenchymale transitie wordt genoemd. In deze staat dragen ze actiever bij aan littekenvorming. Deze endotheelcellen vertoonden dezelfde metabolische kenmerken als podocyten: minder capaciteit om vetten te verbranden en meer afhankelijkheid van glycolyse. Dit suggereert dat gestreste podocyten indirect naburige cellen naar schadelijk gedrag kunnen duwen, waardoor fibrose zich door de hele glomerulus versterkt.
Wat dit betekent voor mensen met diabetes
In het dagelijks leven lijken podocyten te kunnen functioneren zonder veel hulp van AMPK. Maar onder de chronische stress van diabetes wordt de resterende AMPK-activiteit in normale podocyten een stille verdediger: het helpt hen vetten op de juiste manier te verbranden, beschermt hun mitochondriën en houdt ontstekingsalarmen onder controle. Wanneer dat vangnet wegvalt, raken vet- en suikerverwerking ontregeld, breken mitochondriën af, slaan ontstekingsroutes aan en verspreidt littekenvorming zich door het nierfilter. Deze bevindingen ondersteunen het idee dat therapieën die AMPK-activiteit voorzichtig verhogen, of de beschermende effecten ervan op metabolisme en ontsteking nabootsen, kunnen helpen de progressie van diabetische nierziekte te vertragen of te voorkomen — door de veerkracht van podocyten en hun directe buren te versterken in plaats van alleen de bloedglucose te veranderen.
Bronvermelding: Srivastava, S.P., Kopasz-Gemmen, O., Kunamneni, A. et al. AMPK is dispensable for physiological podocyte and glomerular functions but prevents glomerular fibrosis in experimental diabetes. Cell Death Discov. 12, 204 (2026). https://doi.org/10.1038/s41420-026-03078-y
Trefwoorden: diabetische nierziekte, podocyten, AMPK, glomerulaire fibrose, cellulair metabolisme