Clear Sky Science · sv
AMPK är överflödigt för fysiologiska podocyt- och glomerulära funktioner men förhindrar glomerulär fibros vid experimentell diabetes
Varför njurens filtrerande celler spelar roll vid diabetes
Våra njurar filtrerar stillsamt blod tusentals gånger om dagen, och en viktig del av det filtret består av celler som kallas podocyter. Dessa celler omsluter små blodkärl i strukturer som kallas glomeruli och håller proteiner kvar i blodet samtidigt som avfall och vatten släpps ut i urinen. Denna studie ställer en till synes enkel fråga med stora konsekvenser för personer med diabetes: skyddar en central energikänslig brytare i cellerna, kallad AMPK, verkligen dessa filterceller och förhindrar ärrbildning i njuren? Svaret visar sig vara nyanserat — AMPK behövs inte för daglig njurfunktion, men blir avgörande när diabetes utsätter systemet för stress.
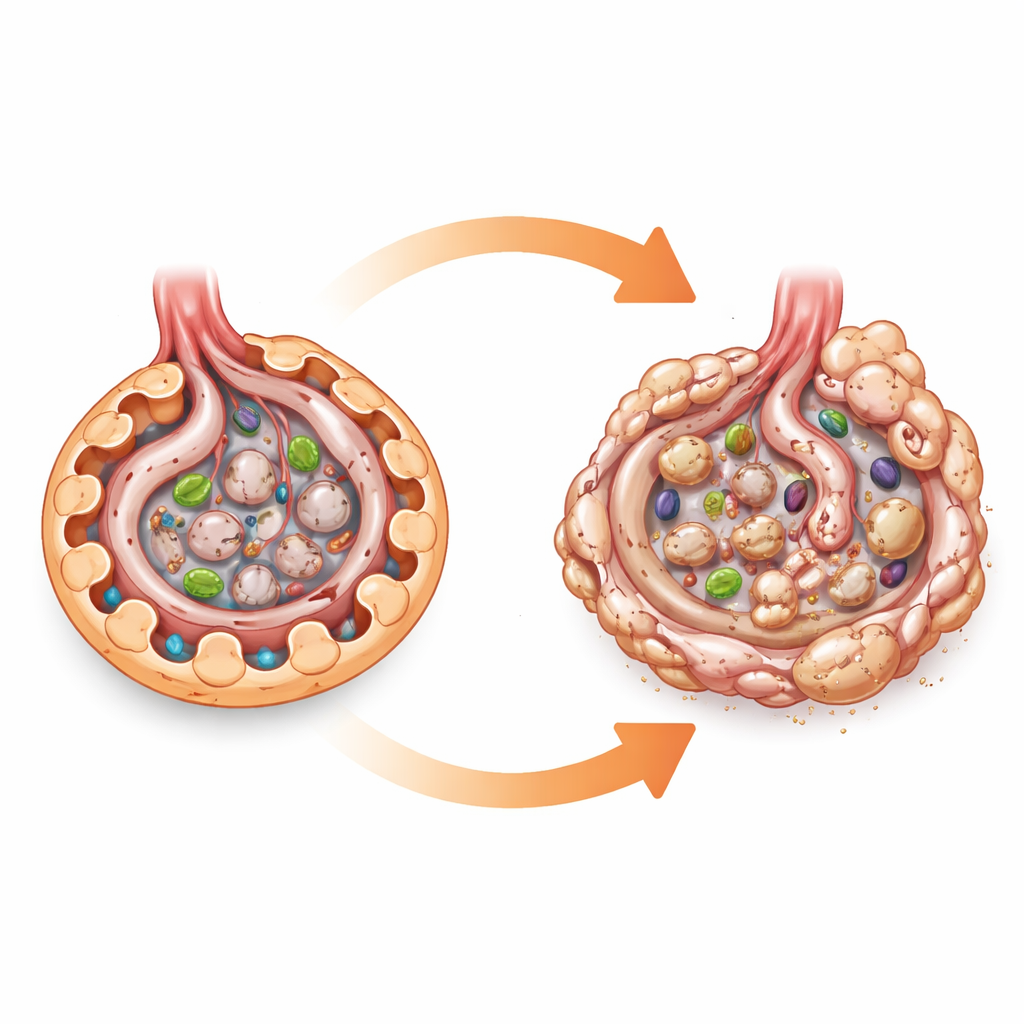
En cellulär bränslemätare under lupp
AMPK kan ses som en cellulär bränslemätare. När energin är låg slår den på processer som förbränner fett och socker och stöder städsystem som autofagi, vilket hjälper celler att återvinna utslitna komponenter. Eftersom diabetes överlastar njurceller med socker och näringsämnen har många forskare antagit att en nedgång i AMPK-aktivitet direkt skadar podocyter och driver diabetisk njursjukdom. Mycket av detta förtroende kom från cellodlingsstudier och från djur som behandlats med läkemedel som aktiverar AMPK, vilka kan ha många andra effekter. För att rena bilden konstruerade författarna möss som saknade båda huvudsubenheterna av AMPK specifikt i podocyter, samtidigt som AMPK lämnades intakt i resten av kroppen.
Överraskande normala njurar utan AMPK
När dessa konstruerade möss följdes i två år på normal diet såg deras njurar ut och fungerade precis som deras normala kullsyskon. Antalet podocyter bevarades, glomerulernas finstruktur förblev intakt och urinprov visade inget ökat proteinläckage. Även centrala processer som AMPK är kända för att påverka — såsom tillväxtvägen mTORC1 och cellens interna återvinningssystem — var inte uppenbart störda i dessa podocyter. Det tyder på att i ett friskt, välmatat tillstånd kan podocyter utföra sitt arbete utan att vara beroende av AMPK, kanske genom att förlita sig på reservvägar som utför liknande uppgifter.
Diabetes avslöjar dolda svagheter
Bilden förändrades drastiskt när diabetes inducerades, både i en typ 1‑liknande modell och i en kombinerad högfetts‑/lågdos‑toxinsmodell som efterliknar delar av typ 2‑diabetes. Vid samma höga blodsockernivåer utvecklade möss utan AMPK i podocyterna allvarligare njurskador än normala diabetiska möss. Deras glomeruli var större och mer ärrbildade, och de läckte mer albumin i urinen, ett centralt kliniskt tecken på njurskada. Detaljerad färgning visade kraftigare uppbyggnad av kollagen och stressproteiner i glomeruli, vilket pekar på en acceleration av glomerulär fibros — den gradvisa ersättningen av känslig filtrerande vävnad med stel ärrvävnad.
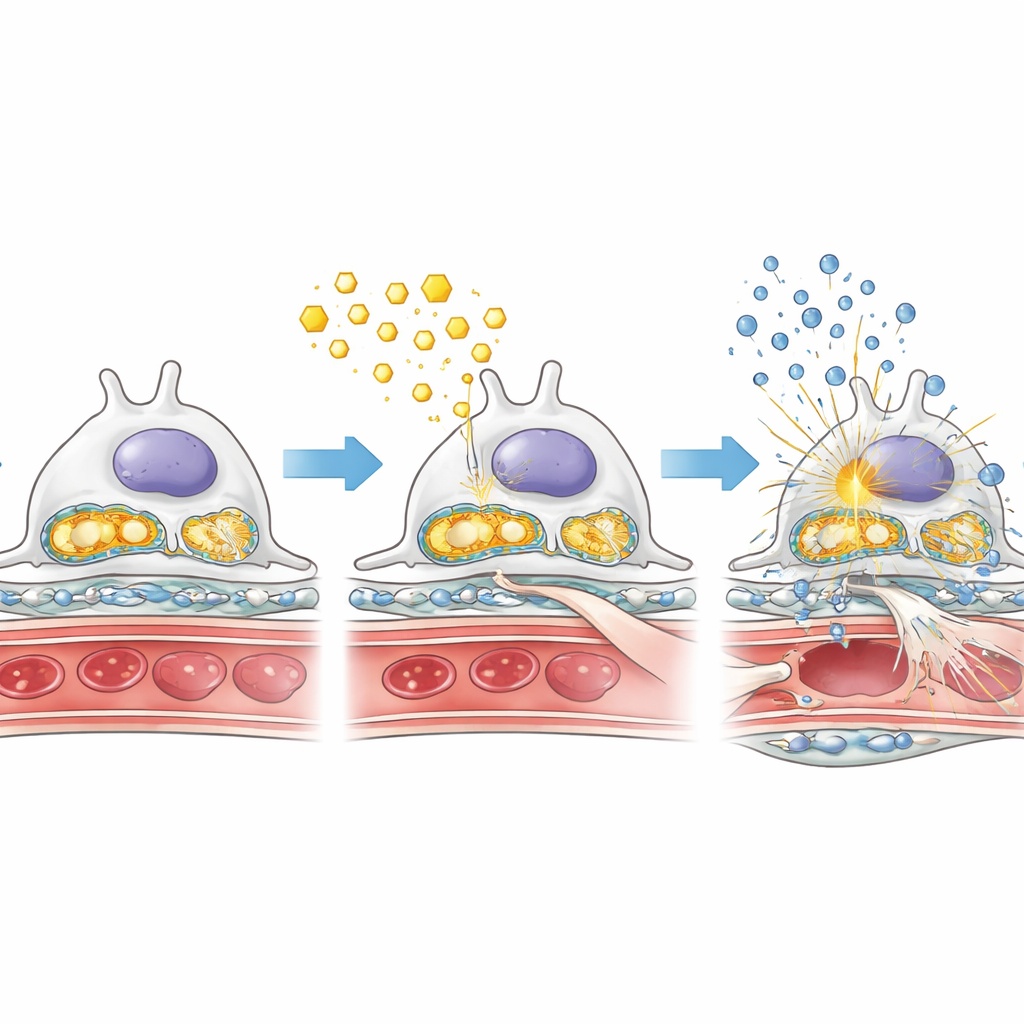
Fettöverbelastning, skadade kraftverk och inflammatoriska larm
För att förstå varför avsaknaden av AMPK förvärrade skadan undersökte forskarna noggrant hur podocyter hanterade fett och socker under diabetiska förhållanden. I diabetiska möss utan podocyt‑AMPK ackumulerades fettkroppar i glomeruli, samtidigt som ett nyckelenzym för förbränning av fettsyror var reducerat. Samtidigt var enzymer som driver snabb sockernedbrytning mer aktiva, vilket antyder en förskjutning mot en mindre effektiv, mer "fermenterande" metabolism som kan gynna ärrbildning. Cellens energifabriker — mitokondrierna — påverkades också: deras stödproteiner var lägre och deras genetiska material läckte ut i cellvätskan. Denna läckta mitokondrie‑DNA verkar utlösa ett internt larmsystem känt som cGAS–STING‑vägen, som i sin tur aktiverar inflammatoriska brytare som NF‑κB och ökar produktionen av inflammatoriska molekyler. Tillsammans skapar dessa förändringar en toxisk blandning av fettöverbelastning, mitokondrieskada och kronisk inflammation inne i njurens filter.
Vågor från podocyter till intilliggande celler
Podocyter arbetar inte isolerat; de sitter direkt mitt emot glomerulära endotelceller som klär blodsidan av filtret. Studien fann att när podocyt‑AMPK saknades vid diabetes var dessa intilliggande endotelceller mer benägna att anta ett fibroblastliknande tillstånd, en process som kallas endotel‑till‑mesenkymal omvandling. I detta tillstånd bidrar de mer aktivt till ärrbildning. Dessa endotelceller visade samma metabola signaturer som sågs i podocyterna: mindre kapacitet att förbränna fett och större beroende av glykolys. Det tyder på att stressade podocyter indirekt kan driva närliggande celler mot skadligt beteende och på så sätt förstärka fibros över hela glomerulus.
Vad detta betyder för personer med diabetes
I vardagen verkar podocyter klara sig utan mycket hjälp från AMPK. Men under den kroniska stress som diabetes innebär blir den kvarvarande AMPK‑aktiviteten i normala podocyter en tyst försvarare som hjälper dem att förbränna fett korrekt, skydda sina mitokondrier och hålla inflammatoriska larm i schack. När det skyddsnätet tas bort går fett‑ och sockerhanteringen fel, mitokondrier bryts ner, inflammatoriska vägar tänds och ärrbildning sprider sig genom njurens filter. Dessa fynd stödjer idén att terapier som försiktigt stimulerar AMPK‑aktivitet, eller efterliknar dess skyddande effekter på metabolism och inflammation, skulle kunna bromsa eller förebygga diabetisk njursjukdom — genom att stärka motståndskraften hos podocyter och deras nära grannar snarare än genom att enbart påverka blodsockret.
Citering: Srivastava, S.P., Kopasz-Gemmen, O., Kunamneni, A. et al. AMPK is dispensable for physiological podocyte and glomerular functions but prevents glomerular fibrosis in experimental diabetes. Cell Death Discov. 12, 204 (2026). https://doi.org/10.1038/s41420-026-03078-y
Nyckelord: diabetisk njursjukdom, podocyter, AMPK, glomerulär fibros, cellmetabolism