Clear Sky Science · de
AMPK ist für die physiologische Funktion von Podozyten und Glomeruli entbehrlich, verhindert aber glomeruläre Fibrose bei experimentellem Diabetes
Warum Filterzellen der Niere bei Diabetes wichtig sind
Unsere Nieren filtern still und leise tausendfach am Tag Blut, und ein zentraler Bestandteil dieses Filters besteht aus Zellen, die Podozyten genannt werden. Diese Zellen umhüllen winzige Blutgefäße in Strukturen, die Glomeruli genannt werden, halten Proteine im Blut zurück und lassen Abfallstoffe und Wasser in den Urin passieren. Die vorliegende Studie stellt eine auf den ersten Blick einfache, aber für Menschen mit Diabetes wichtige Frage: Schützt ein zellulärer Energiesensor namens AMPK diese Filterzellen und verhindert die Vernarbung der Niere? Die Antwort ist subtil — AMPK ist für die Alltagsfunktion der Niere nicht erforderlich, wird aber bei diabetischem Stress entscheidend.
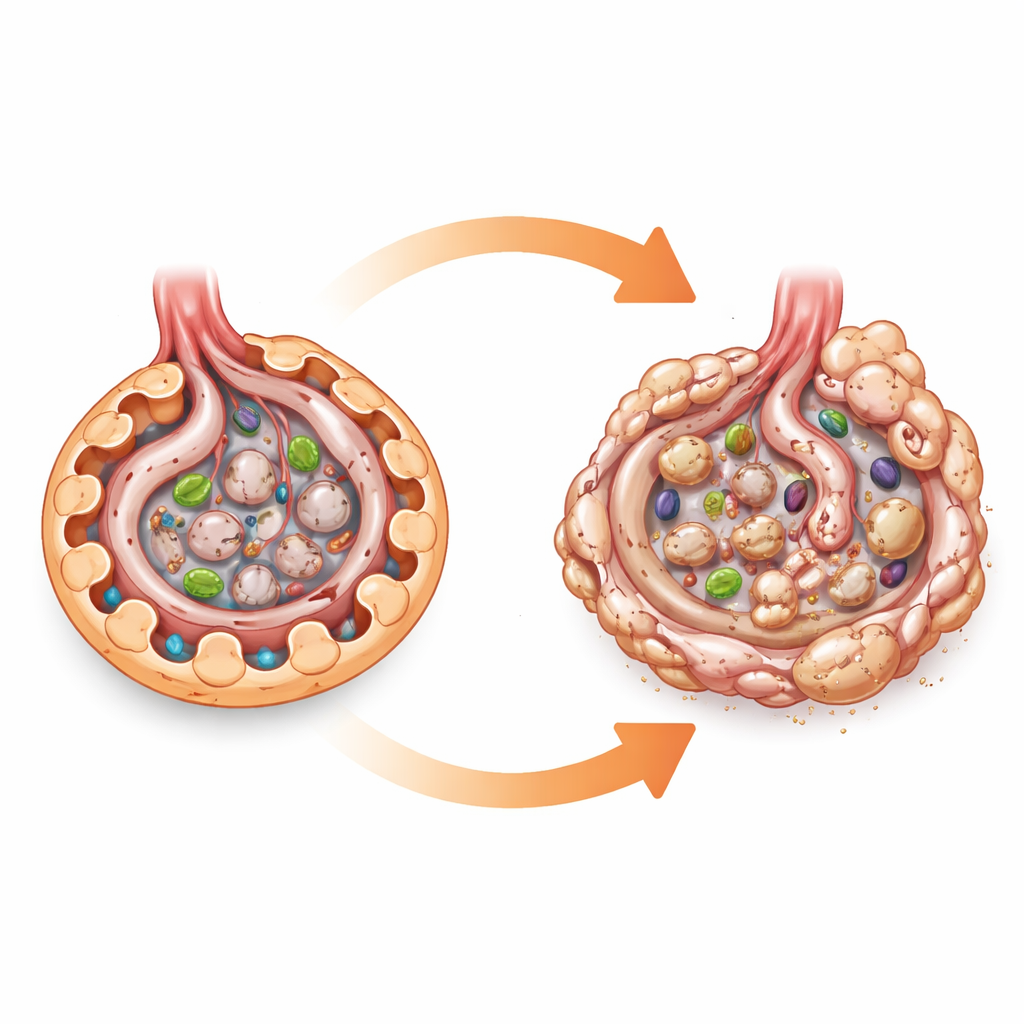
Ein zellulärer Tankmesser unter dem Mikroskop
Man kann sich AMPK als zellulären Tankmesser vorstellen. Wenn Energie knapp ist, schaltet es Prozesse an, die Fett und Zucker verbrennen, und unterstützt Recyclingsysteme wie die Autophagie, die hilft, abgenutzte Zellbestandteile zu entsorgen. Da Diabetes Nierenzellen mit Zucker und Nährstoffen überlädt, gingen viele Forscher davon aus, dass eine Abnahme der AMPK‑Aktivität Podozyten direkt schädigt und die diabetische Nierenerkrankung antreibt. Diese Annahme beruhte größtenteils auf Zellkulturstudien und auf Tierversuchen mit Wirkstoffen, die AMPK aktivieren und viele weitere Effekte haben können. Um die Rolle von AMPK sauberer zu prüfen, erzeugten die Autoren Mäuse, denen beide wichtigen AMPK‑Untereinheiten spezifisch in Podozyten fehlten, während AMPK im übrigen Körper intakt blieb.
Erstaunlich normale Nieren ohne AMPK
Wurden diese genetisch veränderten Mäuse zwei Jahre lang mit normaler Kost beobachtet, sahen ihre Nieren genauso aus und funktionierten genauso wie die ihrer normalen Wurfgeschwister. Die Anzahl der Podozyten blieb erhalten, die feine Struktur der Glomeruli war intakt, und Urintests zeigten keinen vermehrten Proteinverlust. Selbst zentrale Prozesse, von denen bekannt ist, dass AMPK sie beeinflusst — wie der Wachstumsweg mTORC1 und das zelluläre Recycling — schienen in diesen Podozyten nicht offenkundig gestört. Das deutet darauf hin, dass Podozyten in einem gesunden, gut ernährten Zustand ihre Aufgaben ohne AMPK erfüllen können, möglicherweise indem sie auf Ausweichwege zurückgreifen, die ähnliche Funktionen übernehmen.
Diabetes legt verborgene Schwachstellen offen
Das Bild änderte sich deutlich, als Diabetes induziert wurde, sowohl in einem Typ‑1‑ähnlichen Modell als auch in einem kombinierten High‑Fat/Low‑Dose‑Toxin‑Modell, das Aspekte des Typ‑2‑Diabetes nachbildet. Bei gleichen hohen Blutzuckerwerten entwickelten Mäuse ohne AMPK in Podozyten schwerwiegendere Nierenschäden als normale diabetische Mäuse. Ihre Glomeruli waren größer und stärker vernarbt, und sie verloren mehr Albumin im Urin — ein klinisch wichtiger Hinweis auf Nierenschädigung. Detaillierte Färbungen zeigten stärkere Ablagerungen von Kollagen und Stressproteinen in den Glomeruli, was auf eine beschleunigte glomeruläre Fibrose hindeutet — den schrittweisen Ersatz zarter Filterstrukturen durch steifes Narbengewebe.
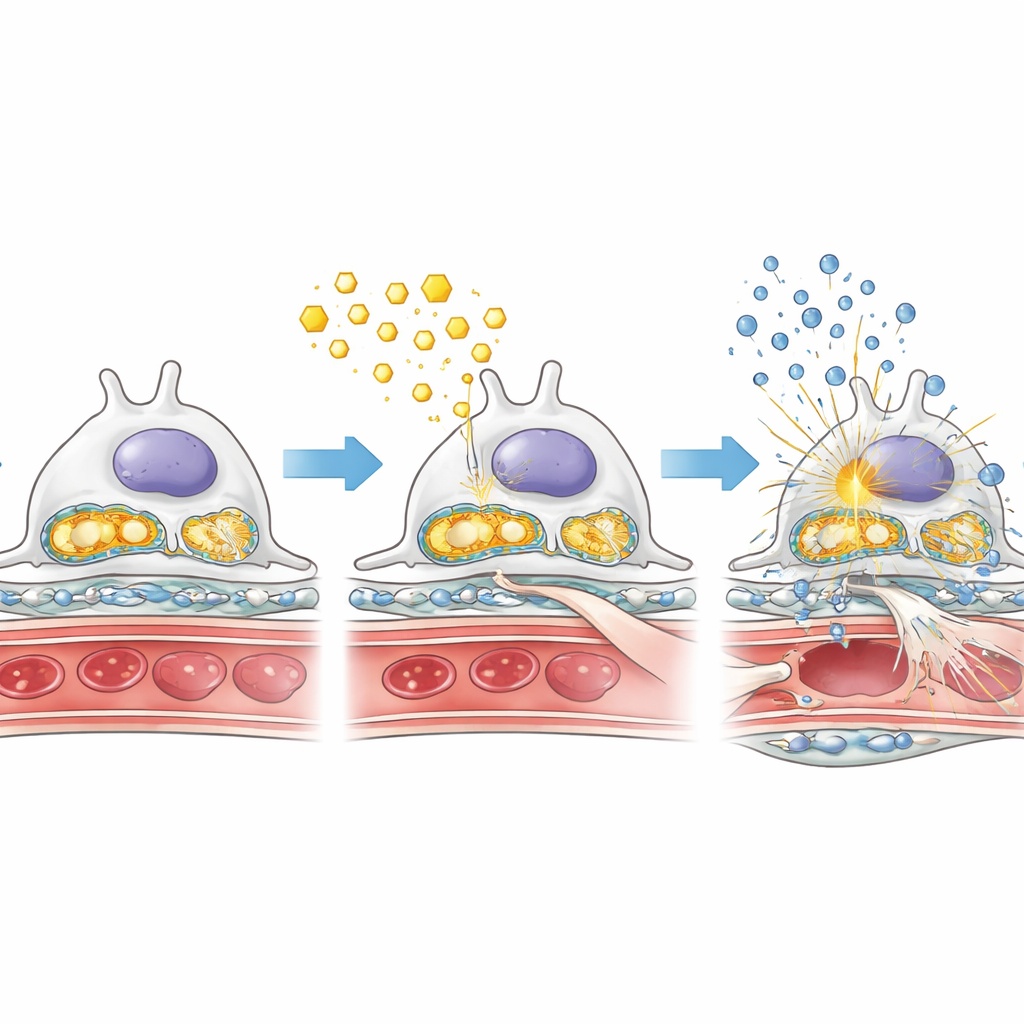
Fettüberladung, beschädigte Kraftwerke und entzündliche Alarmzeichen
Um zu verstehen, warum das Fehlen von AMPK die Schäden verschärfte, untersuchten die Forscher genau, wie Podozyten Fette und Zucker unter diabetischen Bedingungen verarbeiten. In diabetischen Mäusen ohne Podozyten‑AMPK sammelten sich Fetttropfen in den Glomeruli an, während ein wichtiges Enzym zur Verbrennung von Fettsäuren reduziert war. Gleichzeitig waren Enzyme, die schnellen Zuckerabbau antreiben, stärker aktiv, was auf eine Verschiebung hin zu einem weniger effizienten, eher „fermentativen“ Stoffwechsel hinweist, der Narbenbildung begünstigen kann. Die zellulären Kraftwerke — die Mitochondrien — waren ebenfalls betroffen: Ihre Stützproteine waren vermindert und ihre genetische Information trat ins Zellplasma über. Diese freigesetzte mitochondriale DNA scheint ein internes Alarmsystem namens cGAS–STING auszulösen, das wiederum entzündliche Schalter wie NF‑κB aktiviert und die Produktion entzündungsfördernder Moleküle erhöht. Zusammen erzeugen diese Veränderungen eine toxische Mischung aus Fettüberladung, mitochondrialer Schädigung und chronischer Entzündung im Nierenfilter.
Welleneffekte von Podozyten zu benachbarten Zellen
Podozyten arbeiten nicht isoliert; sie sitzen direkt gegenüber von glomerulären Endothelzellen, die die blutseitige Seite des Filters auskleiden. Die Studie zeigte, dass bei fehlendem Podozyten‑AMPK im Diabetes diese benachbarten Endothelzellen eher dazu neigten, einen fibroblastenähnlichen Zustand anzunehmen, einen Prozess, der als Endothel‑zu‑Mesenchymal‑Transition bezeichnet wird. In diesem Zustand tragen sie aktiver zur Narbenbildung bei. Diese Endothelzellen zeigten die gleichen metabolischen Kennzeichen wie die Podozyten: geringere Fähigkeit zur Fettverbrennung und stärkere Abhängigkeit von der Glykolyse. Das legt nahe, dass gestresste Podozyten benachbarte Zellen indirekt zu schädlichem Verhalten treiben und so die Fibrose im gesamten Glomerulus verstärken können.
Was das für Menschen mit Diabetes bedeutet
Im Alltag scheinen Podozyten weitgehend ohne AMPK auszukommen. Unter dem chronischen Stress des Diabetes wird die verbleibende AMPK‑Aktivität in normalen Podozyten jedoch zu einem stillen Verteidiger: Sie hilft, Fett korrekt zu verbrennen, die Mitochondrien zu schützen und entzündliche Alarme zu dämpfen. Wird dieses Sicherheitsnetz entfernt, geraten Fett‑ und Zuckerstoffwechsel aus dem Gleichgewicht, Mitochondrien gehen kaputt, entzündliche Wege schlagen an und Narbenbildung breitet sich im Nierenfilter aus. Diese Ergebnisse stützen die Idee, dass Therapien, die AMPK‑Aktivität moderat anheben oder seine schützenden Effekte auf Stoffwechsel und Entzündung nachahmen, helfen könnten, die diabetische Nierenerkrankung zu verlangsamen oder zu verhindern — indem sie die Widerstandskraft von Podozyten und ihren engen Nachbarn stärken, statt nur den Blutzucker zu verändern.
Zitation: Srivastava, S.P., Kopasz-Gemmen, O., Kunamneni, A. et al. AMPK is dispensable for physiological podocyte and glomerular functions but prevents glomerular fibrosis in experimental diabetes. Cell Death Discov. 12, 204 (2026). https://doi.org/10.1038/s41420-026-03078-y
Schlüsselwörter: diabetische Nierenerkrankung, Podozyten, AMPK, glomeruläre Fibrose, zellulärer Stoffwechsel