Clear Sky Science · it
AMPK è superfluo per le funzioni fisiologiche dei podociti e del glomerulo ma previene la fibrosi glomerulare nel diabete sperimentale
Perché le cellule del filtro renale contano nel diabete
I nostri reni filtrano silenziosamente il sangue migliaia di volte al giorno, e una parte chiave di quel filtro è costituita da cellule chiamate podociti. Queste cellule si avvolgono intorno a minuscoli vasi sanguigni in strutture note come glomeruli, trattenendo le proteine nel sangue mentre lasciano passare rifiuti e acqua nell’urina. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni per le persone con diabete: un importante interruttore sensibile all’energia nelle cellule, chiamato AMPK, protegge davvero questi elementi filtranti e previene la cicatrizzazione del rene? La risposta si rivela sfumata: AMPK non è necessario per la funzione renale quotidiana, ma diventa cruciale quando il diabete mette sotto stress il sistema.
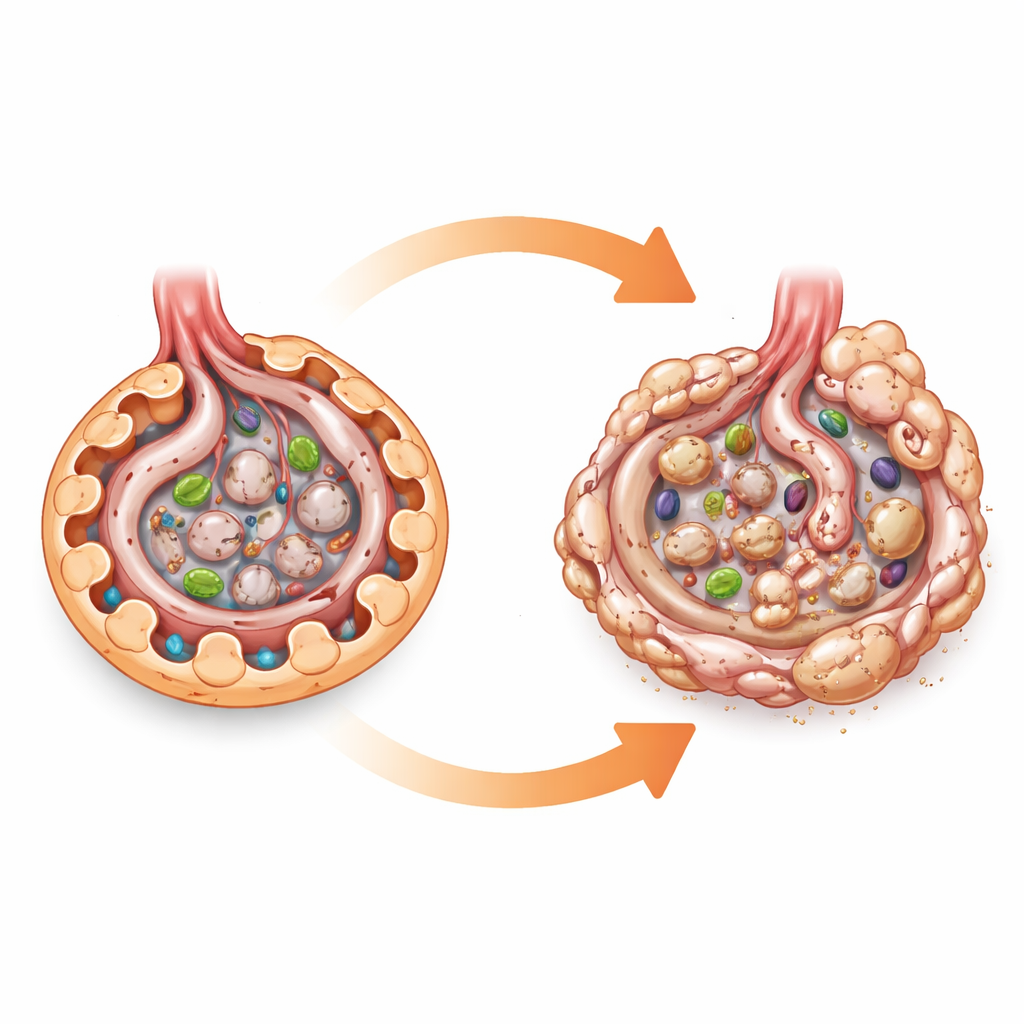
Un indicatore di carburante cellulare al microscopio
Si può pensare ad AMPK come a un indicatore di carburante cellulare. Quando l’energia scarseggia, attiva processi che bruciano grassi e zuccheri e sostiene sistemi di pulizia come l’autofagia, che aiuta le cellule a riciclare componenti usurati. Poiché il diabete sovraccarica le cellule renali di zuccheri e nutrienti, molti ricercatori hanno supposto che una riduzione dell’attività di AMPK danneggi direttamente i podociti e favorisca la malattia renale diabetica. Gran parte di questa convinzione proveniva da studi su colture cellulari e da animali trattati con farmaci che attivano AMPK, i quali possono avere molti altri effetti. Per testare più chiaramente il ruolo di AMPK, gli autori hanno ingegnerizzato topi privi di entrambi i principali subunità di AMPK specificamente nei podociti, lasciando intatto AMPK nel resto dell’organismo.
Reni sorprendentemente normali in assenza di AMPK
Quando questi topi ingegnerizzati sono stati seguiti per due anni con una dieta normale, i loro reni apparivano e funzionavano esattamente come quelli dei loro fratelli normali. Il numero di podociti era preservato, la struttura fine dei glomeruli rimaneva intatta e gli esami delle urine non mostravano perdita eccessiva di proteine. Anche processi chiave che AMPK è noto influenzare — come una via di crescita chiamata mTORC1 e il sistema interno di riciclo cellulare — non risultavano visibilmente alterati in questi podociti. Ciò suggerisce che in uno stato sano e ben nutrito i podociti possano svolgere il loro lavoro senza dipendere da AMPK, forse appoggiandosi a vie alternative che svolgono funzioni simili.
Il diabete rivela debolezze nascoste
Il quadro è cambiato radicalmente quando è stato indotto il diabete, utilizzando sia un modello simile al tipo 1 sia un modello combinato ad alto contenuto di grassi con bassa dose di tossina che imita aspetti del tipo 2. Sotto gli stessi livelli elevati di glicemia, i topi privi di AMPK nei podociti hanno sviluppato danni renali più gravi rispetto ai topi diabetici normali. I loro glomeruli erano più grandi e più cicatrizzati, e perdevano più albumina nelle urine, un segno clinico chiave di danno renale. Colorazioni dettagliate hanno mostrato un accumulo maggiore di collagene e di proteine di “stress” nei glomeruli, indicando un’accelerazione della fibrosi glomerulare — la graduale sostituzione del tessuto filtrante delicato con cicatrice rigida.
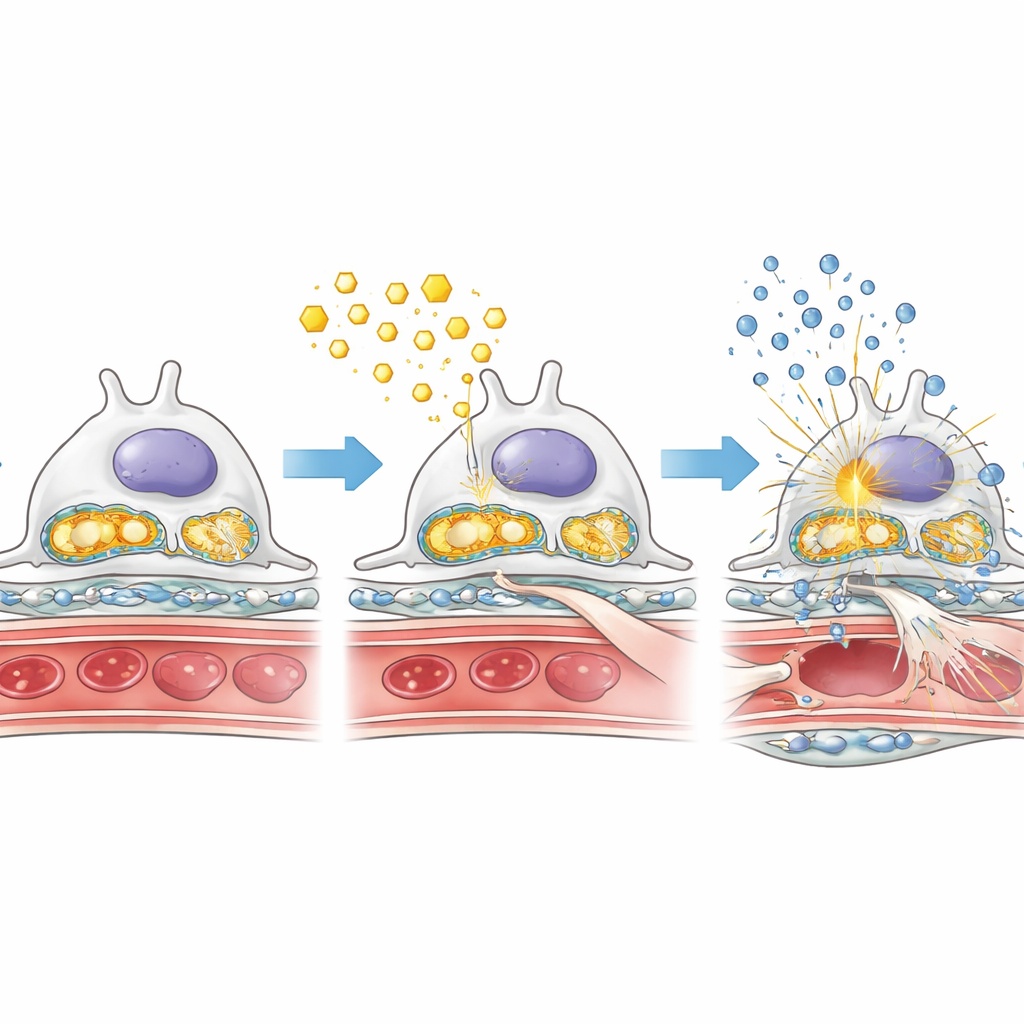
Sovraccarico di grasso, centrali energetiche danneggiate e allarmi infiammatori
Per capire perché la mancanza di AMPK peggiorasse il danno, i ricercatori hanno esaminato da vicino come i podociti gestivano grassi e zuccheri in condizioni diabetiche. Nei topi diabetici privi di AMPK nei podociti, gocce di grasso si sono accumulate all’interno dei glomeruli, mentre un enzima chiave per la combustione degli acidi grassi risultava ridotto. Allo stesso tempo, enzimi che guidano la rapida degradazione degli zuccheri risultavano più attivi, suggerendo uno spostamento verso uno stile metabolico meno efficiente e più “fermentativo” che può favorire la formazione di cicatrici. Le centrali energetiche della cellula — i mitocondri — sono state anch’esse compromesse: le proteine che li supportano erano più basse e il loro materiale genetico è trapelato nel citosol. Questo DNA mitocondriale trapelato sembra attivare un sistema di allerta interno noto come via cGAS–STING, che a sua volta accende interruttori infiammatori come NF‑κB e aumenta la produzione di molecole infiammatorie. Insieme, questi cambiamenti creano un mix tossico di sovraccarico lipidico, danno mitocondriale e infiammazione cronica all’interno del filtro renale.
Ondate dai podociti alle cellule vicine
I podociti non lavorano isolati; si trovano direttamente di fronte alle cellule endoteliali glomerulari, che rivestono il lato sanguigno del filtro. Lo studio ha rilevato che quando l’AMPK dei podociti mancava nel diabete, queste cellule endoteliali vicine avevano più probabilità di assumere uno stato simile ai fibroblasti, un processo chiamato transizione endoteliale-mesenchimale. In questo stato contribuiscono più attivamente alla formazione di cicatrici. Queste cellule endoteliali mostravano le stesse firme metaboliche osservate nei podociti: minore capacità di bruciare grassi e maggiore dipendenza dalla glicolisi. Ciò suggerisce che i podociti sotto stress possano spingere indirettamente le cellule vicine verso comportamenti dannosi, amplificando la fibrosi in tutto il glomerulo.
Cosa significa per le persone con diabete
Nella vita quotidiana, i podociti sembrano in grado di funzionare senza molto aiuto da AMPK. Ma sotto lo stress cronico del diabete, l’attività residua di AMPK nei podociti normali diventa un difensore silenzioso, aiutandoli a bruciare correttamente i grassi, proteggere i mitocondri e tenere sotto controllo gli allarmi infiammatori. Quando questa rete di sicurezza viene rimossa, la gestione di grassi e zuccheri va in tilt, i mitocondri si deteriorano, le vie infiammatorie si accendono e la cicatrizzazione si diffonde attraverso il filtro renale. Questi risultati sostengono l’idea che terapie in grado di potenziare delicatamente l’attività di AMPK, o di imitare i suoi effetti protettivi sul metabolismo e sull’infiammazione, potrebbero aiutare a rallentare o prevenire la malattia renale diabetica — rafforzando la resilienza dei podociti e dei loro vicini piuttosto che limitandosi a modificare la glicemia.
Citazione: Srivastava, S.P., Kopasz-Gemmen, O., Kunamneni, A. et al. AMPK is dispensable for physiological podocyte and glomerular functions but prevents glomerular fibrosis in experimental diabetes. Cell Death Discov. 12, 204 (2026). https://doi.org/10.1038/s41420-026-03078-y
Parole chiave: malattia renale diabetica, podociti, AMPK, fibrosi glomerulare, metabolismo cellulare