Clear Sky Science · ru
AMPK не обязателен для физиологических функций подоцитов и клубочков, но предотвращает клубочковый фиброз при экспериментальном диабете
Почему клетки фильтра почки важны при диабете
Наши почки незаметно фильтруют кровь тысячи раз в день, и ключевую часть этого фильтра составляют клетки, называемые подоцитами. Эти клетки обвивают крошечные сосуды в структурах, известных как клубочки, удерживая белки в крови и позволяя отходам и воде проходить в мочу. В этом исследовании ставится на вид простейший, но важный вопрос для людей с диабетом: действительно ли главный датчик энергии в клетках, называемый AMPK, защищает эти клетки фильтра и предотвращает образование рубцовой ткани в почке? Ответ оказался тонким — AMPK не нужен для повседневной работы почки, но становится критическим, когда диабет создает нагрузку на систему.
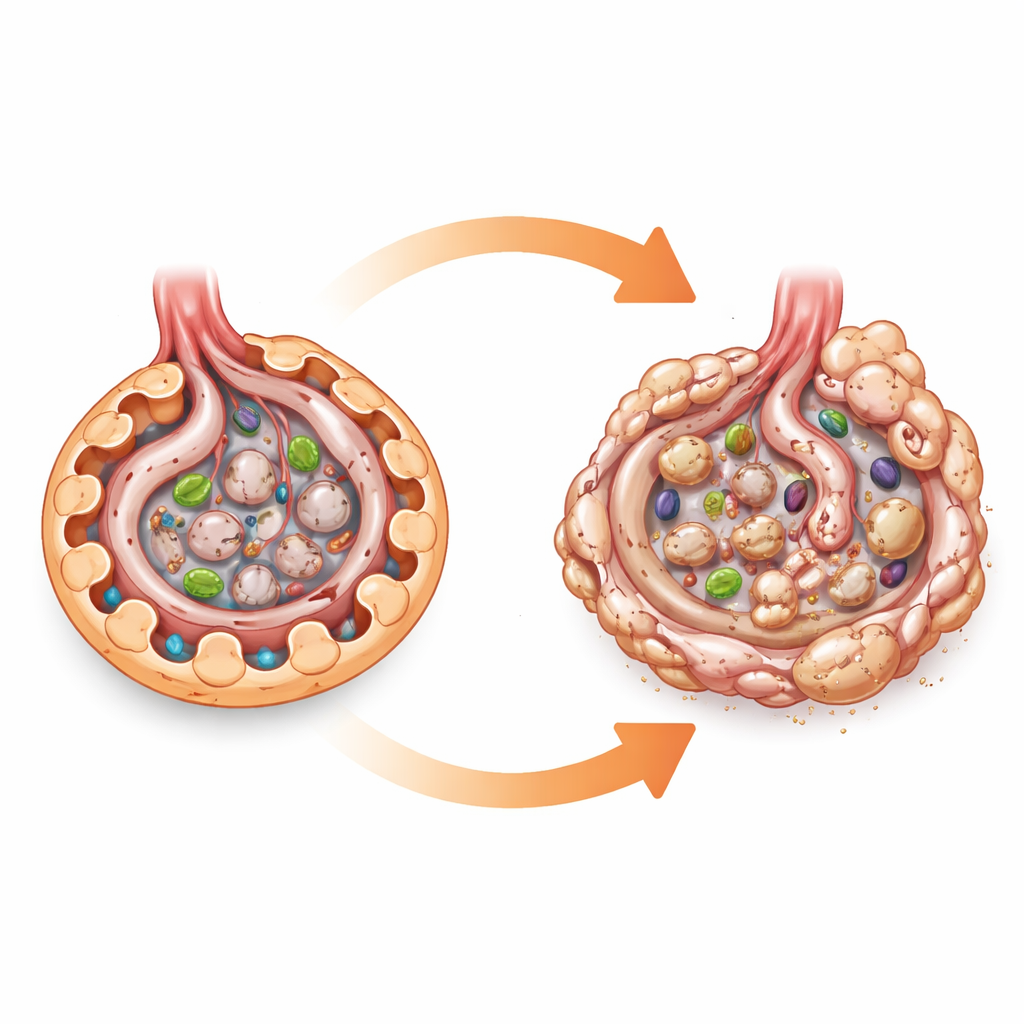
Клеточный датчик топлива под микроскопом
AMPK можно представить как клеточный датчик топлива. Когда энергии мало, он включает процессы, которые сжигают жиры и сахар, и поддерживает системы очистки, такие как аутофагия, помогающие клеткам перерабатывать изношенные компоненты. Поскольку диабет перегружает клетки почек сахаром и питательными веществами, многие исследователи считали, что снижение активности AMPK напрямую вредит подоцитам и способствует диабетической болезни почек. Большая часть этого представления основывалась на исследованиях в культуре клеток и на опытах с препаратами, активирующими AMPK, которые могут иметь и другие эффекты. Чтобы чище проверить роль AMPK, авторы создавали мышей, у которых отсутствовали обе основные субъединицы AMPK исключительно в подоцитах, в то время как AMPK в остальном теле оставался нетронутым.
Удивительно нормальные почки при отсутствии AMPK
Когда за этими генетически модифицированными мышами наблюдали в течение двух лет на обычной диете, их почки выглядели и функционировали так же, как у нормальных однопометников. Число подоцитов сохранялось, тонкая структура клубочков оставалась неповрежденной, а анализы мочи не выявляли избыточной потери белка. Даже ключевые процессы, которыми обычно управляет AMPK — такие как сигнальный путь роста mTORC1 и внутриклеточная система утилизации — в этих подоцитах явно не нарушались. Это указывает на то, что в здоровом, достаточном питании подоциты способны выполнять свою работу без опоры на AMPK, возможно, благодаря резервным путям, выполняющим схожие функции.
Диабет выявляет скрытые слабости
Ситуация резко изменилась, когда был индуцирован диабет, используя как модель, сходную с диабетом 1 типа, так и комбинированную модель с высоким содержанием жира и низкой дозой токсина, имитирующую аспекты диабета 2 типа. При одинаково высоком уровне глюкозы в крови мыши без AMPK в подоцитах развивали более тяжелые поражения почек, чем нормальные диабетические мыши. Их клубочки были крупнее и более рубцованы, и они выделяли больше альбумина с мочой — ключевой клинический признак повреждения почек. Детальные окраски показали более выраженное накопление коллагена и «стрессовых» белков в клубочках, указывая на ускорение клубочкового фиброза — постепенной замены тонкой фильтрующей ткани жестким рубцом.
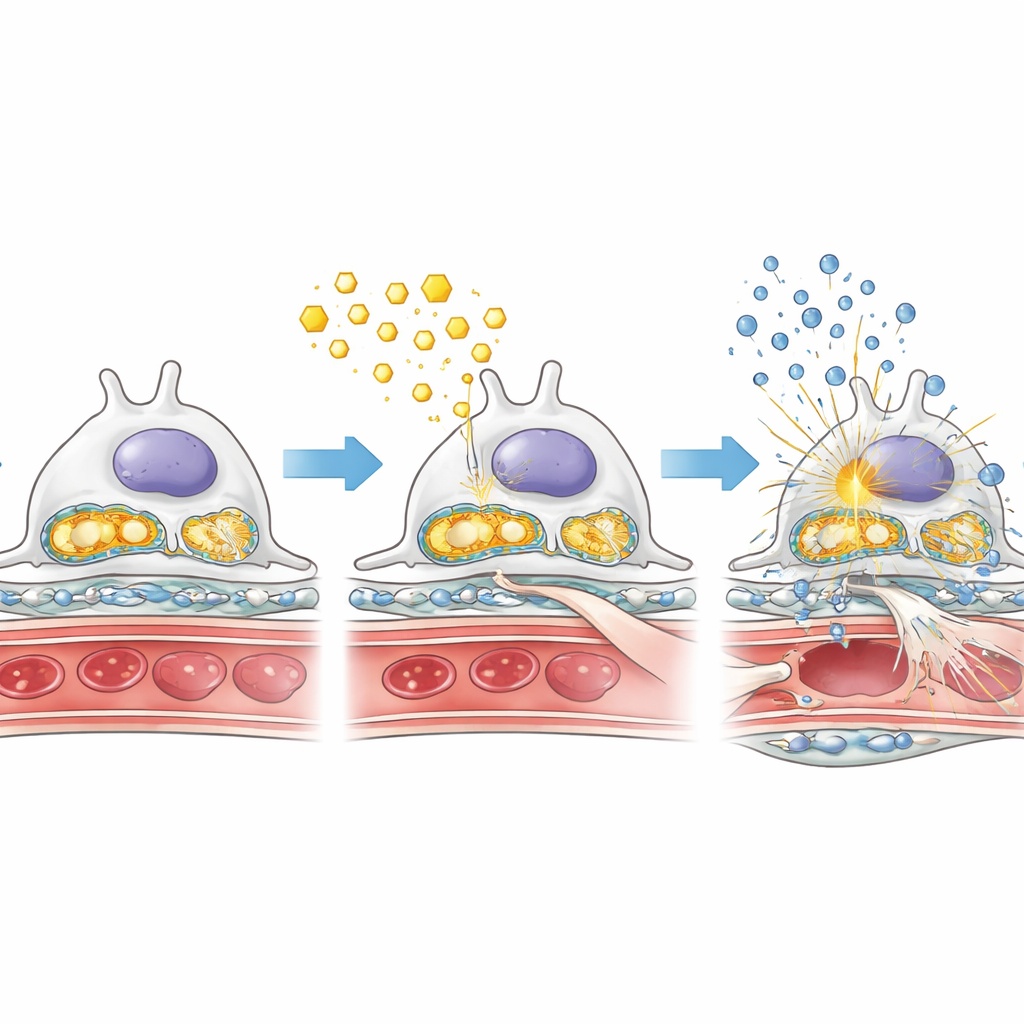
Перегрузка жирами, поврежденные «электростанции» и воспалительные сигналы
Чтобы понять, почему отсутствие AMPK усугубляло повреждение, исследователи внимательно изучили, как подоциты справляются с жирами и сахаром в условиях диабета. У диабетических мышей без AMPK в подоцитах в клубочках накапливались жировые капли, в то время как ключевой фермент для окисления жирных кислот был снижен. Одновременно ферменты, активирующие быстрый распад сахаров, работали активнее, намекая на сдвиг в сторону менее эффективного, более «ферментативного» стиля метаболизма, который может способствовать образованию рубцов. Энергетические фабрики клетки — митохондрии — также пострадали: поддерживающие их белки были снижены, а их генетический материал просачивался в цитоплазму. Похоже, что эта утечка митохондриальной ДНК запускает внутреннюю систему сигнализации, известную как путь cGAS–STING, который, в свою очередь, активирует воспалительные переключатели, такие как NF-κB, и увеличивает продукцию провоспалительных молекул. В совокупности эти изменения создают токсичную смесь из перегрузки жирами, повреждения митохондрий и хронического воспаления внутри фильтра почки.
Воздействие от подоцитов на соседние клетки
Подоциты не работают в изоляции; они расположены прямо напротив эндотелиальных клеток клубочка, выстилающих «кровяную» сторону фильтра. Исследование показало, что при отсутствии AMPK в подоцитах в условиях диабета соседние эндотелиальные клетки с большей вероятностью переходили в фибробластоподобное состояние — процесс, называемый эндотелиально-мезенхимальным переходом. В таком состоянии они активнее способствуют образованию рубца. Эти эндотелиальные клетки демонстрировали те же метаболические признаки, что и подоциты: меньшую способность окислять жиры и большую зависимость от гликолиза. Это указывает на то, что испытывающие стресс подоциты могут косвенно склонять соседние клетки к вредному поведению, усиливая фиброз по всему клубочку.
Что это значит для людей с диабетом
В повседневной жизни подоциты, по-видимому, способны функционировать без существенной поддержки AMPK. Но при хроническом стрессе диабета оставшаяся активность AMPK в нормальных подоцитах действует как тихий защитник, помогая им правильно сжигать жиры, защищать митохондрии и сдерживать воспалительные тревожные сигналы. Когда эта защитная сеть устраняется, обработка жиров и сахаров нарушается, митохондрии разрушаются, воспалительные пути вспыхивают, и рубцевание распространяется по фильтру почки. Эти результаты подкрепляют идею, что терапии, которые мягко усиливают активность AMPK или имитируют его защитные эффекты на метаболизм и воспаление, могут помочь замедлить или предотвратить диабетическую болезнь почек — укрепляя устойчивость подоцитов и их близких соседей, а не только изменяя уровень сахара в крови.
Цитирование: Srivastava, S.P., Kopasz-Gemmen, O., Kunamneni, A. et al. AMPK is dispensable for physiological podocyte and glomerular functions but prevents glomerular fibrosis in experimental diabetes. Cell Death Discov. 12, 204 (2026). https://doi.org/10.1038/s41420-026-03078-y
Ключевые слова: диабетическая болезнь почек, подоциты, AMPK, клубочковый фиброз, клеточный метаболизм