Clear Sky Science · ar
AMPK غير ضروري لوظائف الخلايا المصفِّية للكلى والغلوميرول الفيزيولوجية لكنه يمنع التليف الغلوميرولي في داء السكري التجريبي
لماذا تهم خلايا مرشح الكلى في داء السكري
تقوم كلىّنا بهدوء بترشيح الدم آلاف المرات يومياً، وجزء أساسي من هذا المرشح يتألف من خلايا تُدعى البودوسايت. تلتف هذه الخلايا حول أوعية دموية دقيقة في تراكيب تعرف بالغلو ميرولات، وتحافظ على البروتينات داخل الدم بينما تسمح للفضلات والماء بالمرور إلى البول. يطرح هذا البحث سؤالاً يبدو بسيطاً لكنه ذا تداعيات كبيرة على المصابين بالسكري: هل مفتاح استشعار الطاقة الأساسي في الخلايا، المسمى AMPK، يحمي فعلاً هذه الخلايا المصفِّية ويمنع تندب الكلى؟ تتبين الإجابة بأنها دقيقة — فـAMPK ليس ضرورياً لوظيفة الكلى اليومية، لكنه يصبح حاسماً عندما يضع السكري الجهاز تحت ضغط.
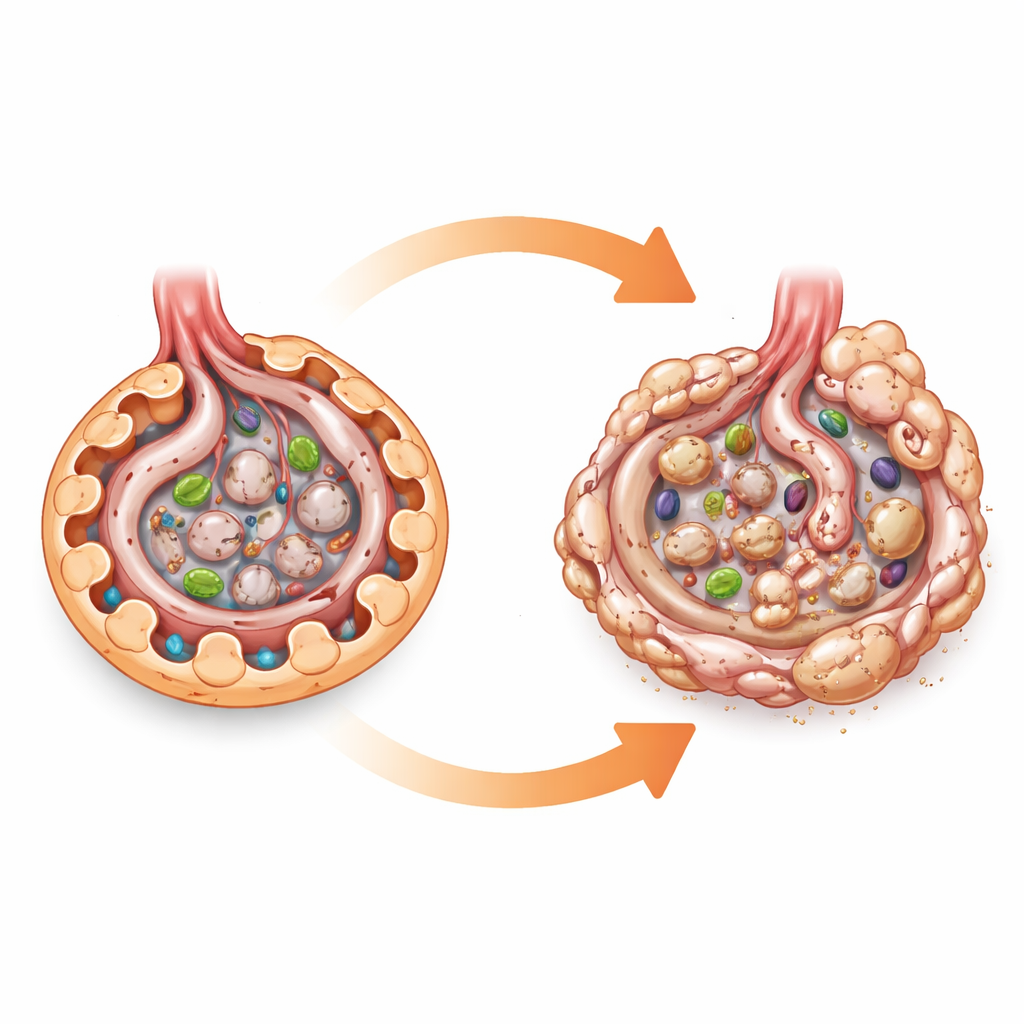
مقياس وقود خلوي تحت المجهر
يمكن التفكير في AMPK كمقياس وقود خلوي. عندما تنخفض الطاقة، يفعل عمليات تحرق الدهون والسكريات ويدعم أنظمة التنظيف مثل البلعمة الذاتية (autophagy)، التي تساعد الخلايا على إعادة تدوير المكونات البالية. وبما أن السكري يثقل خلايا الكلية بالسكر والمغذيات، افترض كثير من الباحثين أن انخفاض نشاط AMPK يَضُرُّ البودوسايت مباشرة ويدفع داء الكلى السكري. معظم هذا الاعتقاد استند إلى دراسات على خلايا مزروعة وحيوانات عولجت بأدوية تُنشط AMPK، والتي قد يكون لها تأثيرات أخرى متعددة. لاختبار دور AMPK بشكل أنقى، صمم المؤلفون فئراناً مهندسة جينياً تفتقر إلى وحدتي AMPK الرئيسيتين خصيصاً في البودوسايت، مع ترك AMPK سليماً في بقية الجسم.
كِلى تبدو طبيعية بشكل مفاجئ في غياب AMPK
عندما تمت متابعة هذه الفئران المهندَسة لمدة عامين على حمية عادية، بدا شكل كلىّها ووظيفتها مشابهين تماماً لأقرانها الطبيعيين. حافظ عدد البودوسايت على استقراره، وبنية الغلوميرولات الدقيقة بقيت سليمة، وفحوصات البول لم تُظهِر تسربَ بروتين زائد. حتى العمليات الأساسية التي يُعرف أن AMPK يؤثر عليها — مثل مسار النمو المسمى mTORC1 ونظام إعادة التدوير داخل الخلية — لم تُظهر اضطراباً واضحاً في هذه البودوسايت. هذا يوحي بأنه في حالة صحية ومغذاة جيداً، يمكن للبودوسايت أداء عملها دون الاعتماد على AMPK، ربما بالاستناد إلى مسارات احتياطية تقوم بوظائف مماثلة.
السكري يكشف نقاط ضعف مخفية
تغيَّرت الصورة بشكل حاد عند استحداث السكري، باستخدام نموذج شبيه بالنوع الأول ونموذج مركب من الدهون العالية وجرعة منخفضة من سم يحاكي بعض جوانب النوع الثاني من السكرى. تحت نفس مستويات السكر المرتفعة في الدم، طورت الفئران التي تفتقر إلى AMPK في البودوسايت إصابة كلوية أشد من الفئران السكرية الطبيعية. كانت غلوميرولاتها أكبر وأكثر ندباً، وتسربت كمية أكبر من الألبومين إلى البول، وهو علامة سريرية رئيسية على تلف الكلى. أظهر التلوين المفصل تراكماً أثقل للكولاجين وبروتينات "الإجهاد" في الغلوميرولات، مما يشير إلى تسارع التليف الغلوميرولي — أي استبدال النسيج المرشح الحساس تدريجياً بأنسجة ندبية صلبة.
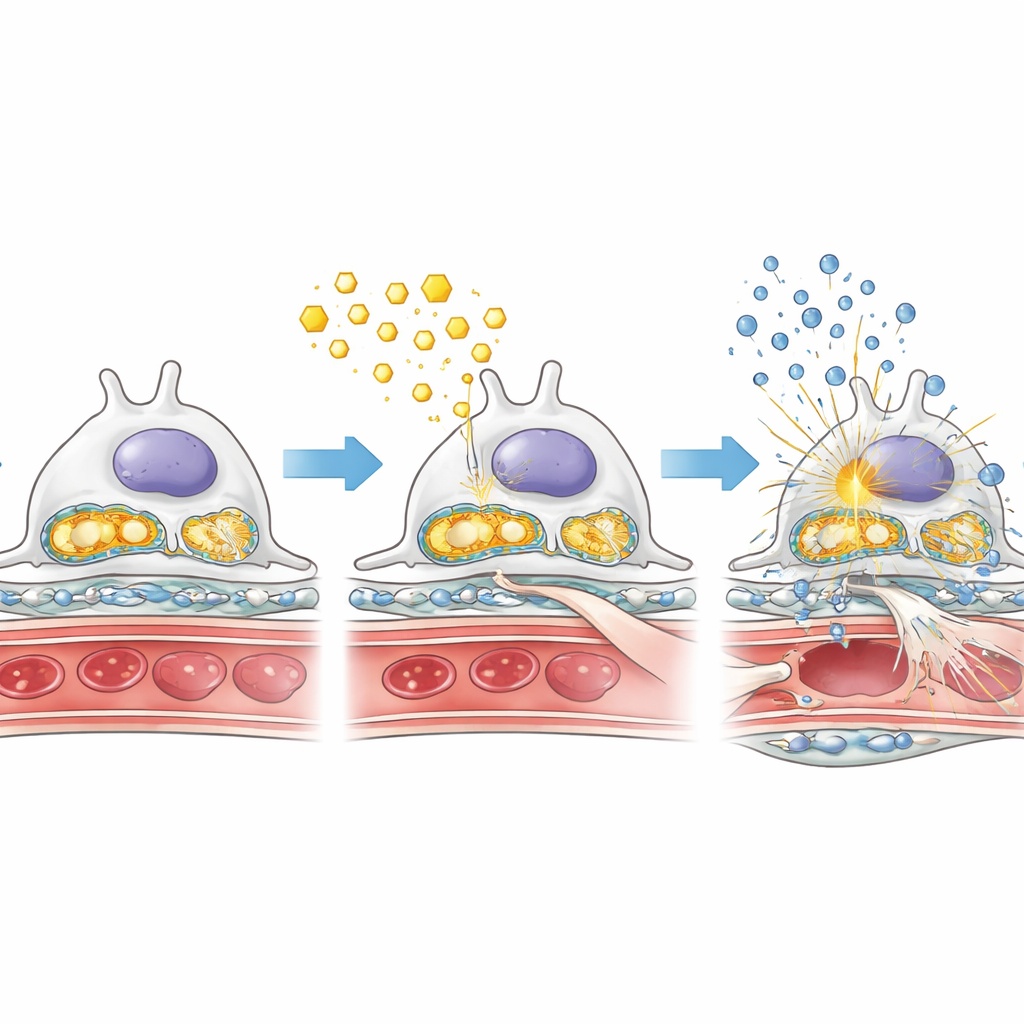
حمولة دهنية زائدة، محطات طاقة متضررة، وإنذارات التهابية
لفهم سبب تفاقم التلف عند غياب AMPK، فحص الباحثون عن قرب كيفية تعامل البودوسايت مع الدهون والسكريات في ظل ظروف سكرية. في الفئران السكرية التي تفتقر إلى AMPK في البودوسايت، تراكمت قطرات دهنية داخل الغلوميرولات، بينما انخفض إنزيم رئيسي لحرق الأحماض الدهنية. في الوقت نفسه، كانت الإنزيمات التي تقود تكسُّر السكر سريعاً أكثر نشاطاً، مما يوحي بتحول نحو أسلوب أيضي أقل كفاءة وأكثر شبهاً بالتخمّر الذي قد يهيّئ للتليف. كما تأثرت مصانع طاقة الخلية — الميتوكوندريا: انخفضت بروتيناتها الداعمة وتسربت مادتها الوراثية إلى سائِل الخلية. يبدو أن هذا الـDNA الميتوكوندري المتسرب يطلق نظام إنذار داخلي يعرف بمسار cGAS–STING، والذي بدوره ينشط مفاتيح التهابية مثل NF‑κB ويزيد إنتاج جزيئات الالتهاب. معاً تصنع هذه التغيرات مزيجاً ساماً من حمولة دهنية زائدة، تلف الميتوكوندريا، والالتهاب المزمن داخل مرشح الكلى.
تموجات من البودوسايت إلى الخلايا المجاورة
البودوسايت لا يعمل بمعزل؛ فهو يقبع مباشرة مقابل خلايا بطانية غلوميرولية (بطانة ومجرية) تبطّن جانب الدم من المرشح. وجدت الدراسة أنه عندما يغيب AMPK في البودوسايت أثناء السكري، تكون هذه الخلايا البطانية المجاورة أكثر عرضة لاعتماد حالة تشبه الخلايا الليفية، وهي عملية تسمى الانتقال البطاني إلى ميزنكيمال (endothelial‑to‑mesenchymal transition). في هذه الحالة تسهم بشكل أكثر فاعلية في تكوين الندب. أظهرت هذه الخلايا البطانية نفس بصمات الأيض المرصودة في البودوسايت: قدرة أقل على حرق الدهون واعتماد أكبر على تحلل الجلوكوز (اللاهوائي). يوحي ذلك بأن البودوسايت المتوتر يمكن أن يدفع الخلايا المجاورة بصورة غير مباشرة نحو سلوك ضار، مضخماً التليف عبر الغلوميرول كله.
ماذا يعني هذا لمرضى السكري
في الحياة اليومية، يبدو أن البودوسايت قادر على العمل دون الكثير من مساعدة AMPK. لكن تحت الضغط المزمن للسكري، يصبح نشاط AMPK الباقي في البودوسايت السليمة مدافعاً صامتًا، يساعدها على حرق الدهون بشكل صحيح، حماية ميتوكوندرياتها، والحفاظ على إنذارات الالتهاب مكبوحة. عندما يُزال هذا الشبك الأَمْنِي، يختل التعامل مع الدهون والسكريات، تنهار الميتوكوندريا، تتوهج مسارات الالتهاب، وينتشر التليف عبر مرشح الكلى. تدعم هذه النتائج الفكرة القائلة بأن العلاجات التي تعزز AMPK برفق، أو تحاكي تأثيراته الوقائية على الأيض والالتهاب، قد تساعد في إبطاء أو منع داء الكلى السكري — عبر تعزيز صمود البودوسايت وجيرانه المقربين بدل الاعتماد فقط على تعديل مستوى السكر في الدم.
الاستشهاد: Srivastava, S.P., Kopasz-Gemmen, O., Kunamneni, A. et al. AMPK is dispensable for physiological podocyte and glomerular functions but prevents glomerular fibrosis in experimental diabetes. Cell Death Discov. 12, 204 (2026). https://doi.org/10.1038/s41420-026-03078-y
الكلمات المفتاحية: داء الكلى السكري, الخلايا المسؤولة عن الترشيح (بودوسايت), AMPK, تليف الغلوميرول, الأيض الخلوي