Clear Sky Science · zh
炎性巨噬细胞来源的纤溶酶原激活物抑制剂-1通过抑制吞噬清除加剧炎症
当清理队伍出错时
我们的身体依赖免疫“清理队”在受伤后清除死亡和受损的细胞。这项研究揭示了一种名为PAI-1的小蛋白如何将这些有益的清理细胞变成持续炎症的推动者。通过阻断细胞碎片的安全处理,PAI-1使受损组织停留在缓慢愈合和慢性刺激的状态——这一见解可能为治疗肌肉损伤和其他炎症性疾病开辟新途径。
从有益的炎症到有害的肿胀
炎症本应是短暂的。组织受损时,免疫细胞迅速到达,清除碎片,然后参与重建健康结构。巨噬细胞是这个过程中关键的角色——它既能引发炎症,也能促进炎症消退。巨噬细胞通过一种称为吞噬清除(efferocytosis)的过程“吞噬”垂死细胞,受表面信号引导,这些信号标记了应被清除与应被保留的细胞。如果这一清除步骤失败,死亡细胞及其内容物会堆积,令组织暴露于危险信号中,从而推动与心脏病、糖尿病、自身免疫疾病乃至癌症相关的长期炎症。
聚焦肌肉损伤
为了解PAI-1在这一过程中的作用,研究者采用了成熟的骨骼肌损伤小鼠模型。向小鼠腿部肌肉注射毒素以造成受控损伤并随后同步修复。损伤早期,大量带有CCR2和Ly6C标志的炎性巨噬细胞涌入肌肉。这类巨噬细胞在损伤部位被发现是PAI-1的高产者。当在小鼠中敲除PAI-1基因,或用小分子药物阻断PAI-1活性时,受损的肌纤维清除更快,炎性信号下降,肌肉正常的蜂窝状结构恢复得更快。即便体内其他来源的PAI-1仍然存在,这些益处仍然显现,表明其有显著的局部效应。
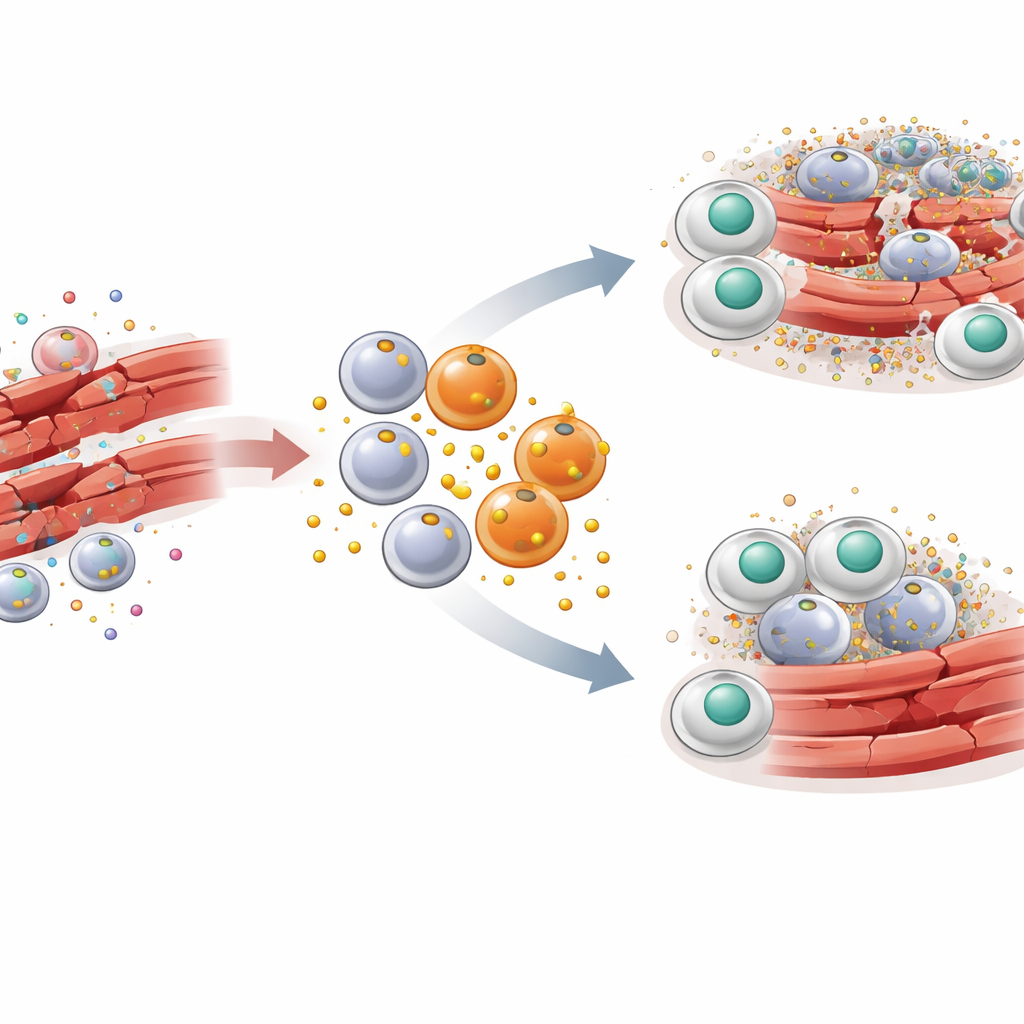
信号干扰者如何阻断细胞清除
关键发现是PAI-1充当了吞噬清除的某种信号干扰器。垂死细胞在其表面暴露一种称为钙网蛋白(calreticulin)的分子,作为“吃我”的标志。巨噬细胞带有识别钙网蛋白并触发吞噬的受体LRP-1。研究团队发现PAI-1也能与LRP-1结合——且与钙网蛋白相比亲和力更高。在细胞培养实验中,加入PAI-1降低了巨噬细胞吞噬死亡细胞的能力,而去除PAI-1或阻断其与LRP-1的结合则增强了这一清除过程。一种不能再附着到LRP-1的PAI-1突变体未能阻断吞噬清除,证实干扰作用发生在该受体处。实质上,PAI-1优先竞争“吃我”信号,使死亡细胞被遗弃、无法被清除。
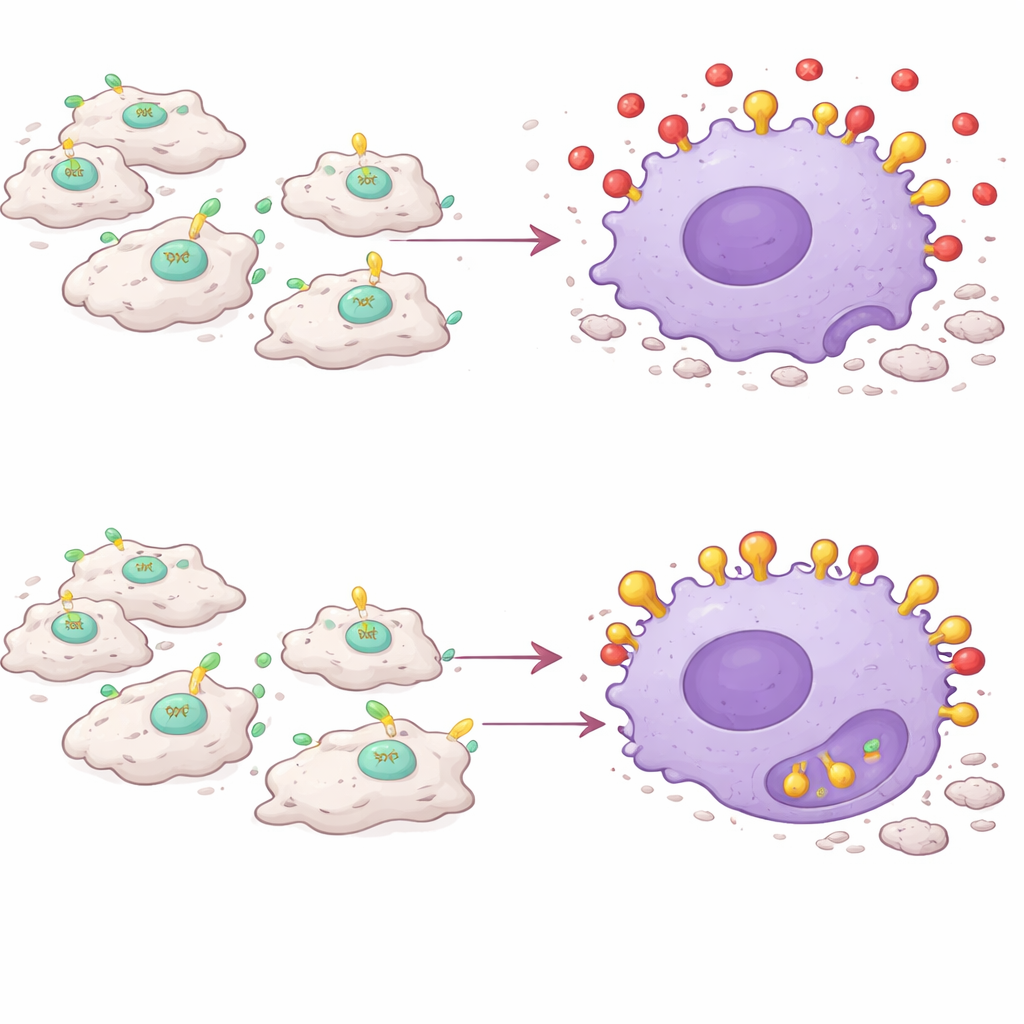
巨噬细胞反过来对抗自身任务
值得注意的是,重要的并不是任意来源的PAI-1,而是炎性巨噬细胞自身产生的PAI-1。当研究者选择性地仅在CCR2+Ly6C+巨噬细胞中删除PAI-1基因时,受损肌肉的愈合与全身PAI-1敲除动物相似:受损纤维染色减少,促炎信使水平降低,更多肌细胞再生。将富含PAI-1的炎性巨噬细胞移植到PAI-1缺失的小鼠体内足以恢复延长的炎症和延迟的愈合,即使机体其他部位缺乏PAI-1。在活体动物中,无论是基因删除还是药物抑制PAI-1均增加了巨噬细胞对示踪颗粒的吞噬,表明炎症期间吞噬活性更强或恢复得更好。
为治疗打开新路径
该研究表明,巨噬细胞来源的PAI-1阻断了死亡细胞的清除,把一种众所周知的凝血调节因子与炎症无法自行终止联系了起来。当PAI-1在巨噬细胞受体处挤兑正常的“吃我”信号时,碎片滞留、组织修复停滞。口服PAI-1抑制剂在小鼠中恢复了清理功能并加速了肌肉再生,提示了帮助组织在受伤后恢复的可行途径。鉴于不良的吞噬清除与高PAI-1水平是许多慢性炎症和与年龄相关疾病的常见特征,针对该通路或许未来能提供一类新型抗炎疗法——其作用方式不是简单抑制免疫反应,而是帮助机体完成愈合的最后阶段。
引用: Ibrahim, A.A., Miura, H., Terada, T. et al. Inflammatory macrophage-derived plasminogen activator inhibitor-1 exacerbates inflammation through efferocytosis inhibition. Cell Death Discov. 12, 195 (2026). https://doi.org/10.1038/s41420-026-03076-0
关键词: 炎症, 巨噬细胞, 肌肉修复, 细胞清除, PAI-1 抑制剂