Clear Sky Science · pl
Inflammacyjny inhibitor aktywatora plazminogenu-1 pochodzący od makrofagów pogarsza stan zapalny poprzez hamowanie eferocytozy
Kiedy załogi porządkowe zawodzą
Nasz organizm polega na „załogach porządkowych” układu odpornościowego, które usuwają martwe i uszkodzone komórki po urazie. To badanie ujawnia, jak jeden mały białkowy czynnik, zwany PAI-1, może przemienić te pomocne komórki porządkowe w źródło utrzymującego się zapalenia. Blokując bezpieczne usuwanie szczątków komórkowych, PAI-1 utrzymuje tkankę w stanie spowolnionego gojenia i przewlekłego podrażnienia — wgląd, który może otworzyć nowe możliwości leczenia uszkodzeń mięśni i innych chorób zapalnych.
Od pożytecznego stanu zapalnego do szkodliwego obrzęku
Stan zapalny ma być przemijający. Gdy tkanka ulega urazowi, komórki odpornościowe napływają, usuwają szczątki, a następnie pomagają odbudować zdrową strukturę. Kluczowym graczem w tym procesie jest makrofag, wszechstronna komórka, która może zarówno wywoływać zapalenie, jak i przyczyniać się do jego zakończenia. Makrofagi „pożerają” umierające komórki w procesie zwanym eferocytozą, kierując się sygnałami powierzchniowymi, które oznaczają, które komórki należy usunąć, a które pozostawić. Jeśli ten etap oczyszczania zawiedzie, martwe komórki i ich zawartość się kumulują, zalewając tkanki sygnałami niebezpieczeństwa, które mogą podtrzymywać długotrwałe zapalenie związane z chorobami serca, cukrzycą, chorobami autoimmunologicznymi, a nawet rakiem.
Bliższe spojrzenie na uraz mięśnia
Aby zrozumieć rolę PAI-1 w tej historii, badacze użyli dobrze znanego modelu mysiego urazu mięśni szkieletowych. Do mięśni nóg wstrzyknięto toksynę, by wywołać kontrolowane uszkodzenie, po którym następowała zsynchronizowana naprawa. Wczesnie po urazie do mięśnia napłynęła fala zapalnych makrofagów niosących markery o nazwach CCR2 i Ly6C. Te konkretne makrofagi okazały się być wydajnymi producentami PAI-1 bezpośrednio w miejscu urazu. Gdy gen PAI-1 został wyłączony u myszy lub gdy aktywność PAI-1 zablokowano małą cząsteczką, uszkodzone włókna mięśniowe oczyszczały się szybciej, sygnały zapalne malały, a typowa plastra miodu architektura mięśnia odtwarzała się szybciej. Te korzyści pojawiły się mimo obecności innych źródeł PAI-1 w organizmie, co wskazuje na silny lokalny efekt.
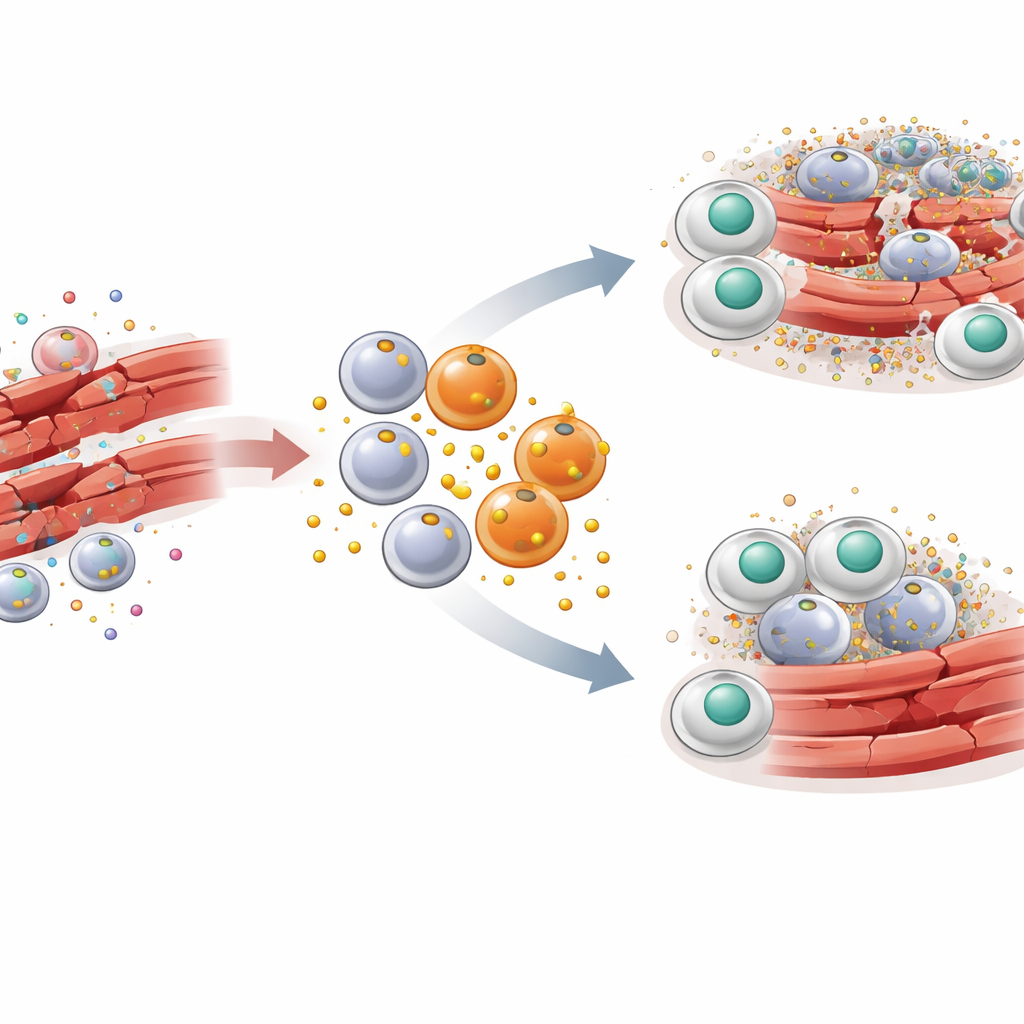
Jak „zagłuszacz” sygnałów blokuje komórkowe sprzątanie
Kluczowym odkryciem jest to, że PAI-1 działa jak rodzaj zagłuszacza sygnałów dla eferocytozy. Umierające komórki ujawniają na swojej powierzchni cząsteczkę zwaną kalretikulinem, która pełni funkcję flagi „zjedz mnie”. Makrofagi niosą receptor zwany LRP-1, który rozpoznaje kalretikulinę i uruchamia pochłonięcie umierającej komórki. Zespół odkrył, że PAI-1 również wiąże się z LRP-1 — i robi to z wyższym powinowactwem niż kalretikulina. W eksperymentach na hodowlach komórkowych dodanie PAI-1 zmniejszało zdolność makrofagów do pochłaniania martwych komórek, podczas gdy usunięcie PAI-1 lub zablokowanie jego wiązania z LRP-1 zwiększało to oczyszczanie. Mutant PAI-1, który nie potrafił już przyłączać się do LRP-1, nie blokował eferocytozy, co potwierdza, że interferencja zachodzi na poziomie tego receptora. W efekcie PAI-1 konkurując wypiera sygnały „zjedz mnie”, pozostawiając martwe komórki bez opieki i nieusunięte.
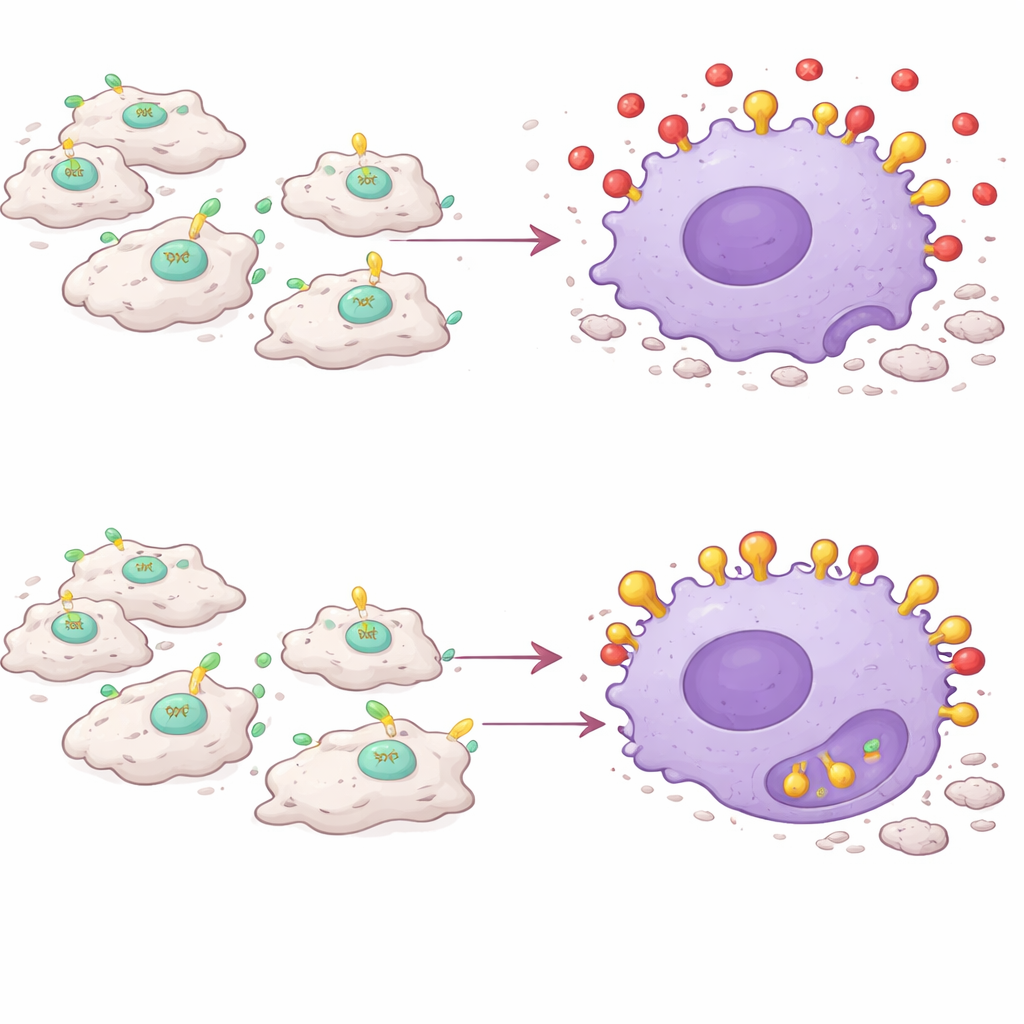
Makrofagi odwracają się od swojego zadania
Zaskakująco, nie liczy się każdy PAI-1, lecz ten produkowany przez zapalne makrofagi. Gdy badacze selektywnie usunęli gen PAI-1 jedynie w makrofagach CCR2+Ly6C+, uszkodzone mięśnie goiły się podobnie jak u myszy z pełnym brakiem PAI-1: mniej zabarwionych uszkodzonych włókien, niższe poziomy prozapalnych przekaźników i więcej zregenerowanych komórek mięśniowych. Przeszczepienie makrofagów zapalnych bogatych w PAI-1 do myszy pozbawionych PAI-1 wystarczyło, by przywrócić przedłużone zapalenie i opóźnione gojenie, mimo że reszta organizmu nie miała PAI-1. U żywych zwierząt zarówno genetyczne usunięcie, jak i farmakologiczne zahamowanie PAI-1 zwiększały pobieranie przez makrofagi cząstek znacznikowych, co wskazywało na bardziej aktywne zachowanie pochłaniania podczas zapalenia.
Otwarcie nowej ścieżki terapeutycznej
Pokażając, że PAI-1 pochodzący od makrofagów blokuje usuwanie martwych komórek, to badanie łączy dobrze znany regulator krzepnięcia z zawodzeniem mechanizmu wygaszania zapalenia. Kiedy PAI-1 wypiera normalne sygnały „zjedz mnie” przy receptorach makrofagów, szczątki utrzymują się, a naprawa tkanki zastyga. Lek hamujący PAI-1 podawany doustnie przywrócił porządki i przyspieszył regenerację mięśni u myszy, sugerując praktyczny sposób wspierania odzyskiwania tkanek po urazie. Ponieważ słaba eferocytoza i wysokie poziomy PAI-1 są częstymi cechami wielu przewlekłych stanów zapalnych i chorób związanych ze starzeniem, ukierunkowanie tej ścieżki może pewnego dnia dostarczyć nowej klasy terapii przeciwzapalnych, które nie polegają tylko na tłumieniu odpowiedzi immunologicznej, lecz pomagają organizmowi dokończyć proces gojenia.
Cytowanie: Ibrahim, A.A., Miura, H., Terada, T. et al. Inflammatory macrophage-derived plasminogen activator inhibitor-1 exacerbates inflammation through efferocytosis inhibition. Cell Death Discov. 12, 195 (2026). https://doi.org/10.1038/s41420-026-03076-0
Słowa kluczowe: zapalanie, makrofagi, naprawa mięśni, usuwanie komórek, inhibitor PAI-1