Clear Sky Science · pt
O inibidor do ativador de plasminogênio 1 (PAI-1) derivado de macrófagos inflamatórios agrava a inflamação ao inibir a eferocitose
Quando as equipes de limpeza falham
Nossos corpos dependem de “equipes de limpeza” do sistema imune para remover células mortas e danificadas após uma lesão. Este estudo revela como uma pequena proteína, chamada PAI-1, pode transformar essas células de limpeza em motoristas de inflamação persistente. Ao bloquear a eliminação segura dos detritos celulares, o PAI-1 mantém o tecido lesionado preso a um estado de cicatrização lenta e irritação crônica — um insight que pode abrir novas vias para tratar danos musculares e outras doenças inflamatórias.
Da inflamação útil ao inchaço prejudicial
A inflamação deveria ser temporária. Quando o tecido é lesionado, células imunes chegam em massa, removem os resíduos e ajudam a reconstruir a estrutura saudável. Um agente-chave nesse processo é o macrófago, uma célula versátil que pode tanto desencadear a inflamação quanto ajudar a resolvê-la. Os macrófagos “comem” células em morte por um processo conhecido como eferocitose, guiados por sinais de superfície que marcam quais células devem ser removidas e quais devem ser preservadas. Se essa etapa de limpeza falha, células mortas e seu conteúdo se acumulam, banhando os tecidos em sinais de perigo que podem alimentar uma inflamação duradoura associada a doenças cardíacas, diabetes, enfermidades autoimunes e até câncer.
Um olhar mais atento à lesão muscular
Para entender como o PAI-1 se encaixa nessa história, os pesquisadores usaram um modelo bem estabelecido de lesão do músculo esquelético em camundongos. Uma toxina foi injetada nos músculos da perna para causar dano controlado seguido de reparo sincronizado. Logo após a lesão, uma onda de macrófagos inflamatórios portando os marcadores CCR2 e Ly6C invadiu o músculo. Esses macrófagos específicos mostraram-se produtores profícuos de PAI-1 diretamente no local da lesão. Quando o gene do PAI-1 foi deletado em camundongos, ou quando a atividade do PAI-1 foi bloqueada com uma droga de pequena molécula, as fibras musculares danificadas foram limpas mais rapidamente, os sinais inflamatórios caíram e a arquitetura normal em favo de mel do músculo foi restaurada mais depressa. Esses benefícios apareceram mesmo com outras fontes de PAI-1 no organismo ainda presentes, indicando um efeito local pronunciado.
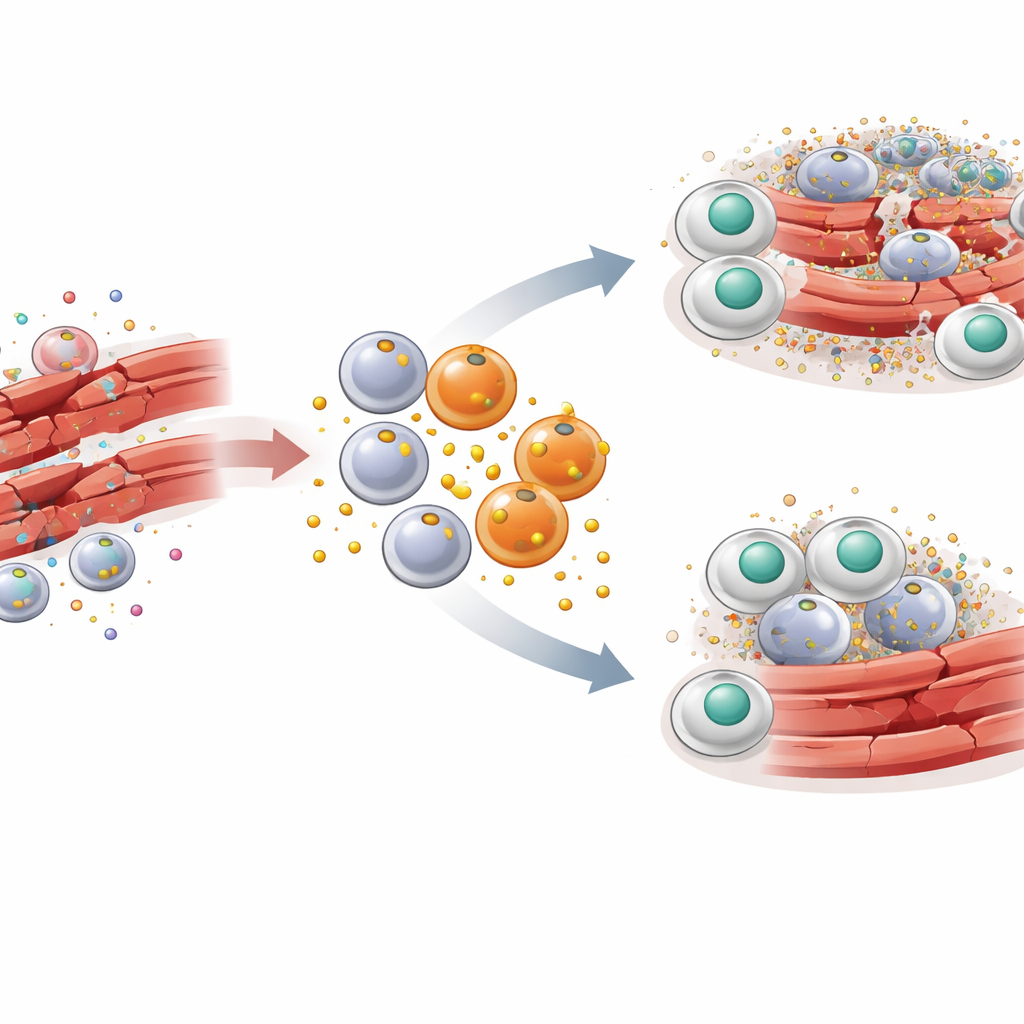
Como um bloqueador de sinais impede a limpeza celular
A descoberta central é que o PAI-1 atua como uma espécie de bloqueador de sinais para a eferocitose. Células em morte expõem uma molécula chamada calreticulina em sua superfície, que funciona como uma placa de “coma-me”. Os macrófagos carregam um receptor chamado LRP-1 que reconhece a calreticulina e desencadeia o engolfamento da célula em morte. A equipe descobriu que o PAI-1 também se liga ao LRP-1 — e o faz com afinidade maior que a calreticulina. Em experimentos em cultura celular, a adição de PAI-1 reduziu a capacidade dos macrófagos de engolir células mortas, enquanto a remoção do PAI-1 ou o bloqueio de sua ligação ao LRP-1 aumentou essa limpeza. Uma forma mutante do PAI-1 que não conseguia mais se ligar ao LRP-1 falhou em bloquear a eferocitose, confirmando que a interferência ocorre nesse receptor. Na prática, o PAI-1 supera os sinais de “coma-me”, deixando as células mortas abandonadas e não removidas.
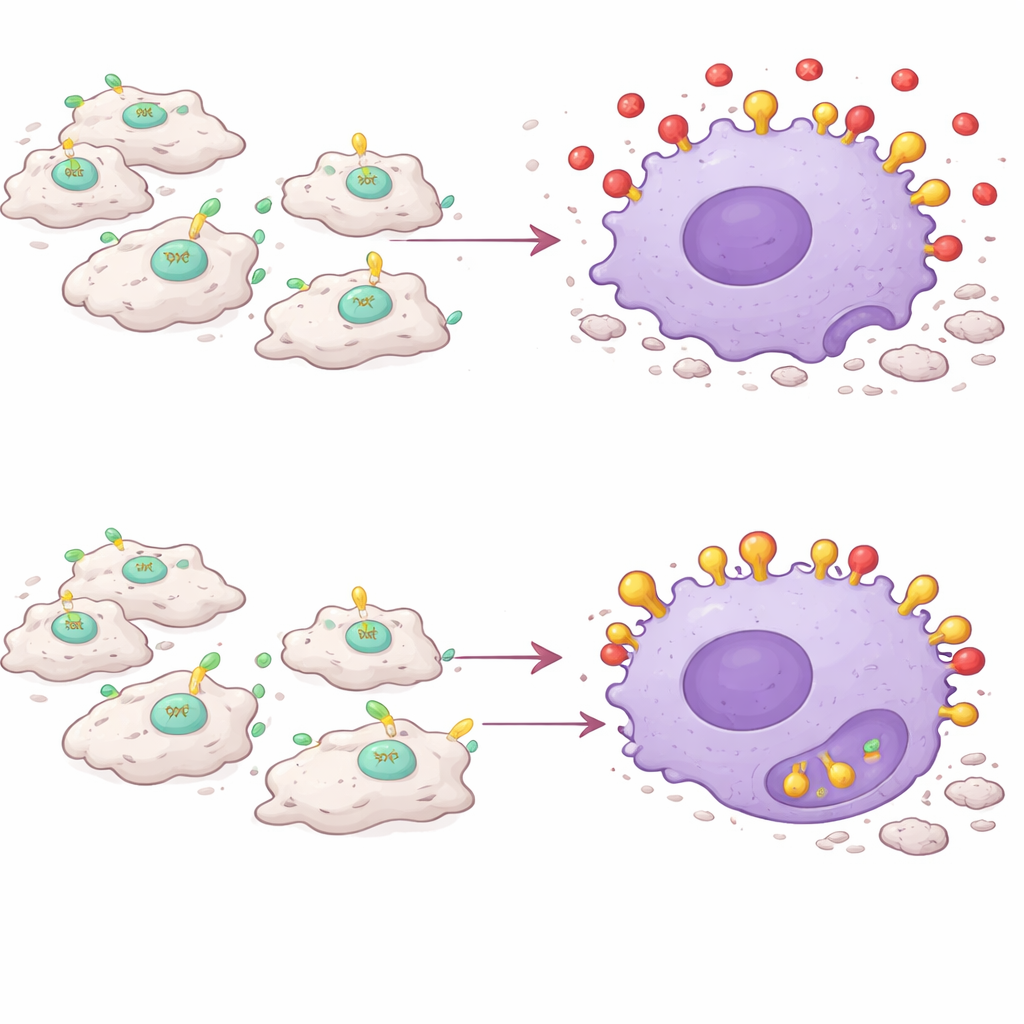
Macrófagos voltam-se contra sua própria tarefa
Surpreendentemente, não é qualquer PAI-1 que importa, mas o PAI-1 produzido pelos próprios macrófagos inflamatórios. Quando os pesquisadores deletaram seletivamente o gene do PAI-1 apenas em macrófagos CCR2+Ly6C+, os músculos lesionados cicatrizaram de forma semelhante aos observados em animais com nocaute total de PAI-1: menor coloração de fibras danificadas, níveis reduzidos de mediadores pró-inflamatórios e mais células musculares regeneradas. Transplantar macrófagos inflamatórios ricos em PAI-1 para camundongos deficientes em PAI-1 foi suficiente para restaurar a inflamação prolongada e a cicatrização retardada, mesmo que o resto do corpo não produzisse PAI-1. Em animais vivos, tanto a deleção genética quanto a inibição farmacológica do PAI-1 aumentaram a captação, por macrófagos, de partículas traçadoras, indicando comportamento de engolfamento mais ativo durante a inflamação.
Abrindo um novo caminho para o tratamento
Ao mostrar que o PAI-1 derivado de macrófagos bloqueia a remoção de células mortas, este estudo conecta um regulador conhecido da coagulação à falha da inflamação em se desligar. Quando o PAI-1 ocupa o lugar dos sinais normais de “coma-me” nos receptores dos macrófagos, os resíduos permanecem e o reparo tecidual estagna. Uma droga oral que inibe o PAI-1 restaurou a limpeza e acelerou a regeneração muscular em camundongos, sugerindo uma estratégia prática para ajudar tecidos a se recuperar após lesão. Como a eferocitose deficiente e níveis elevados de PAI-1 são características comuns de muitas condições inflamatórias crônicas e relacionadas ao envelhecimento, mirar essa via pode um dia oferecer uma nova classe de terapias anti-inflamatórias que não atuam apenas suprimindo respostas imunes, mas ajudando o corpo a completar o trabalho de cicatrização.
Citação: Ibrahim, A.A., Miura, H., Terada, T. et al. Inflammatory macrophage-derived plasminogen activator inhibitor-1 exacerbates inflammation through efferocytosis inhibition. Cell Death Discov. 12, 195 (2026). https://doi.org/10.1038/s41420-026-03076-0
Palavras-chave: inflamação, macrófagos, reparo muscular, limpeza celular, inibidor de PAI-1