Clear Sky Science · ru
Воспалительно активируемый макрофагами ингибитор плазминоген-активатора 1 усугубляет воспаление за счёт подавления эффероцитоза
Когда бригады по уборке ошибаются
Наш организм полагается на иммунные «бригады уборки», которые удаляют мёртвые и повреждённые клетки после травмы. В этом исследовании показано, как один небольшой белок — PAI-1 — может превратить эти полезные очистительные клетки в источник затяжного воспаления. Блокируя безопасную утилизацию клеточного мусора, PAI-1 удерживает повреждённую ткань в состоянии замедленного заживления и хронического раздражения — открытие, которое может помочь разработать новые подходы к лечению повреждений мышц и других воспалительных заболеваний.
От полезного воспаления к вредному отёку
Воспаление должно быть временным. При повреждении ткани в неё устремляются иммунные клетки, убирают обломки и затем помогают восстановить здоровую структуру. Ключевую роль в этом процессе играет макрофаг — универсальная клетка, способная как инициировать воспаление, так и способствовать его разрешению. Макрофаги «поедают» умирающие клетки в процессе, известном как ефероцитоз, ориентируясь по молекулам на поверхности, которые помечают, какие клетки следует удалить, а какие — оставить. Если этот этап очистки нарушается, мёртвые клетки и их содержимое накапливаются, заливая ткани сигнальными молекулами опасности, которые могут подпитывать длительное воспаление, связанное с сердечными заболеваниями, диабетом, аутоиммунными болезнями и даже раком.
Более внимательный взгляд на повреждение мышц
Чтобы понять, какую роль играет PAI-1, исследователи использовали хорошо изученную модель повреждения скелетных мышц у мышей. В мышечные волокна задней лапы вводили токсин, чтобы вызвать контролируемое повреждение с последующим синхронизированным восстановлением. Вскоре после травмы в мышцу пришла волна воспалительных макрофагов с маркерами CCR2 и Ly6C. Эти макрофаги оказались продуктивными источниками PAI-1 прямо в очаге повреждения. При нокауте гена PAI-1 у мышей или при блокаде его активности малой молекулой повреждённые мышечные волокна очищались быстрее, уровни провоспалительных сигналов снижались, и нормальная сотообразная архитектура мышц восстанавливалась быстрее. Эти преимущества проявлялись даже несмотря на наличие других источников PAI-1 в организме, что указывает на сильный локальный эффект.
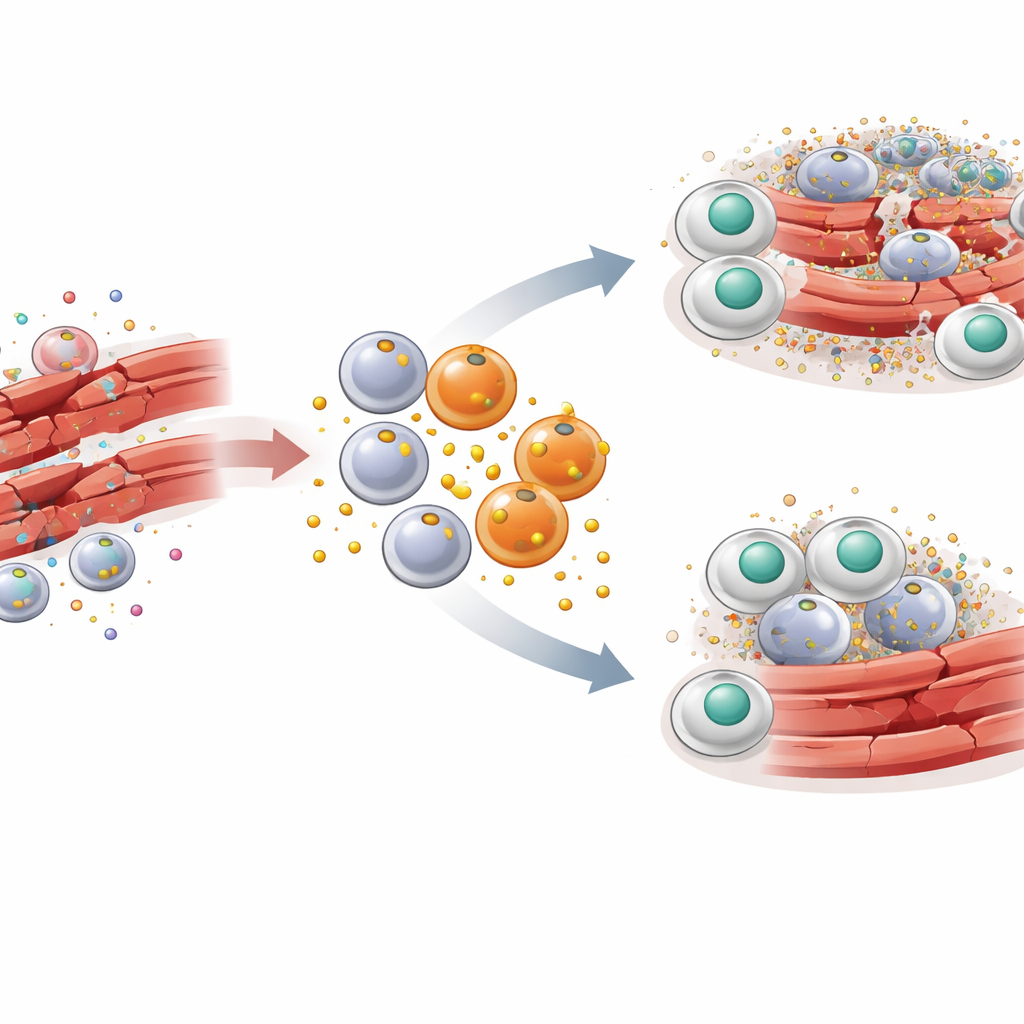
Как «глушилка» сигналов блокирует клеточную уборку
Ключевое открытие — PAI-1 действует как своего рода глушилка сигналов для ефероцитоза. Умирающие клетки выставляют на своей поверхности молекулу кальретикулин, которая служит флагом «съешь меня». Макрофаги несут рецептор LRP-1, который распознаёт кальретикулин и запускает поглощение умирающей клетки. Команда обнаружила, что PAI-1 также связывается с LRP-1 — и делает это с более высокой аффинностью, чем кальретикулин. В опытах на клеточных культурах добавление PAI-1 снижало способность макрофагов поглощать мёртвые клетки, тогда как удаление PAI-1 или блокада его связывания с LRP-1 усиливали эту очистку. Мутантная форма PAI-1, утратившая способность прикрепляться к LRP-1, не блокировала ефероцитоз, что подтвердило: вмешательство происходит на уровне этого рецептора. По сути, PAI-1 выигрывает конкуренцию у сигналов «съешь меня», оставляя мёртвые клетки необработанными и неубранными.
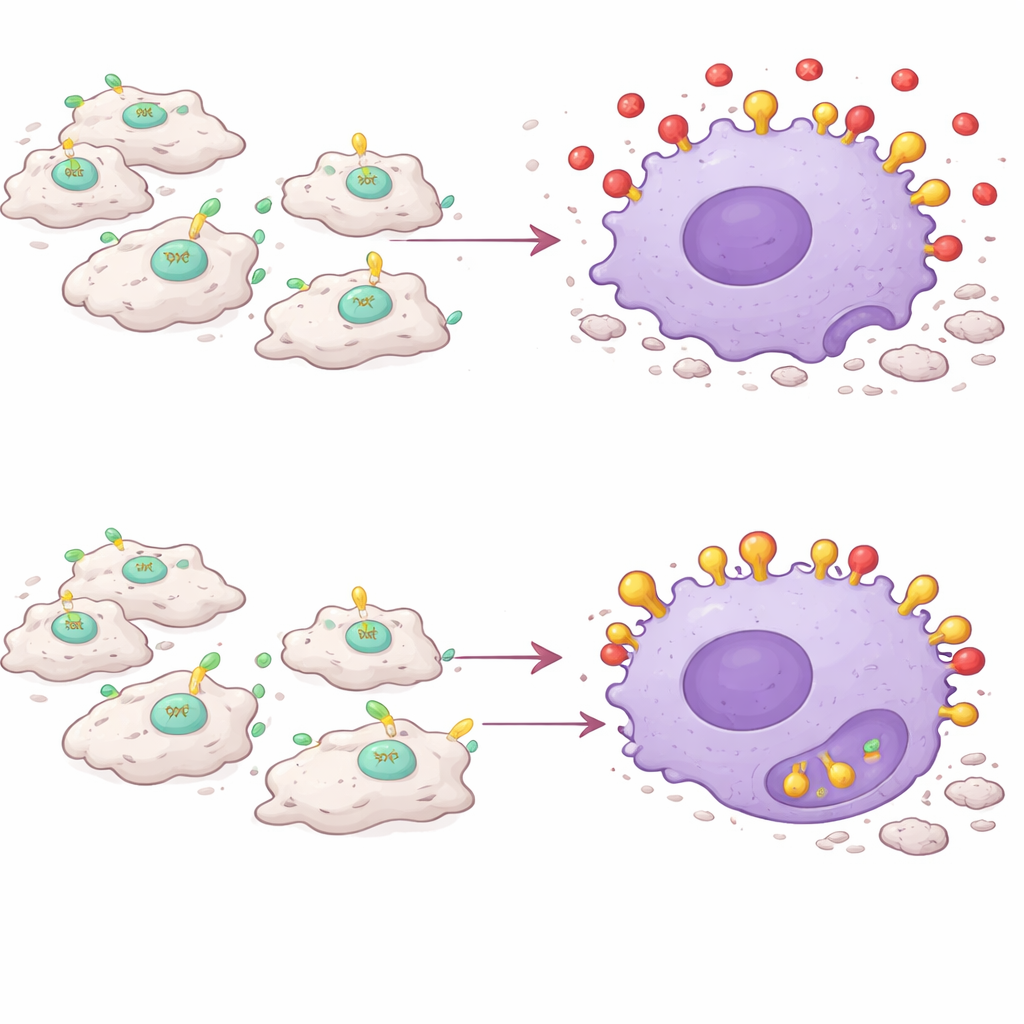
Макрофаги выступают против своей собственной задачи
Поразительно, что значение имеет не любой PAI-1, а именно тот, который вырабатывают воспалительные макрофаги. Когда исследователи селективно удаляли ген PAI-1 только в CCR2+Ly6C+ макрофагах, поражённые мышцы заживляли так же, как у животных с полным нокаутом PAI-1: меньше окрашивания повреждённых волокон, ниже уровни провоспалительных медиаторов и больше регенерировавших мышечных клеток. Пересадка воспалительных макрофагов, богатых PAI-1, в мышей с дефицитом PAI-1 была достаточна, чтобы восстановить затянутое воспаление и замедленное заживление, даже несмотря на отсутствие PAI-1 в остальном организме. In vivo как генетическое удаление, так и фармакологическая блокада PAI-1 увеличивали поглощение макрофагами трассерных частиц, указывая на более активное фагоцитарное поведение в условиях воспаления.
Открывая новый путь для лечения
Показав, что PAI-1, вырабатываемый макрофагами, блокирует очистку мёртвых клеток, это исследование связывает известный регулятор свертывания с неспособностью воспаления завершиться само по себе. Когда PAI-1 вытесняет нормальные сигналы «съешь меня» на рецепторах макрофагов, обломки остаются, и восстановление ткани тормозится. Пероральный препарат, ингибирующий PAI-1, восстановил уборку и ускорил регенерацию мышц у мышей, что наводит на мысль о практическом способе помочь тканям восстановиться после травмы. Поскольку плохой ефероцитоз и повышенные уровни PAI-1 — распространённые черты многих хронических воспалительных и возрастных состояний, таргетирование этого пути может в будущем предложить новый класс антивоспалительных терапий, которые действуют не просто путём подавления иммунного ответа, а помогая организму завершить процесс заживления.
Цитирование: Ibrahim, A.A., Miura, H., Terada, T. et al. Inflammatory macrophage-derived plasminogen activator inhibitor-1 exacerbates inflammation through efferocytosis inhibition. Cell Death Discov. 12, 195 (2026). https://doi.org/10.1038/s41420-026-03076-0
Ключевые слова: воспаление, макрофаги, восстановление мышц, очистка клеток, ингибитор PAI-1