Clear Sky Science · es
El inhibidor del activador del plasminógeno 1 derivado de macrófagos inflamatorios agrava la inflamación al inhibir la eferocitosis
Cuando los equipos de limpieza fallan
Nuestros cuerpos dependen de «equipos de limpieza» inmunitarios para eliminar las células muertas y dañadas tras una lesión. Este estudio revela cómo una pequeña proteína, llamada PAI-1, puede convertir a esas células de limpieza útiles en motores de una inflamación persistente. Al bloquear la eliminación segura de los restos celulares, PAI-1 mantiene el tejido lesionado en un estado de curación lenta y malestar crónico, una idea que podría abrir nuevas vías para tratar daños musculares y otras enfermedades inflamatorias.
De la inflamación útil a la hinchazón dañina
La inflamación debería ser temporal. Cuando el tejido se daña, las células inmunitarias acuden, eliminan los desechos y ayudan a reconstruir la estructura sana. Un actor clave en este proceso es el macrófago, una célula versátil que puede tanto desencadenar inflamación como contribuir a su resolución. Los macrófagos «se comen» las células moribundas en un proceso conocido como eferocitosis, guiados por señales en la superficie que indican qué células deben retirarse y cuáles deben permanecer. Si este paso de limpieza falla, las células muertas y su contenido se acumulan, bañando los tejidos en señales de peligro que pueden alimentar una inflamación duradera vinculada a enfermedades cardíacas, diabetes, dolencias autoinmunes e incluso cáncer.
Una mirada más cercana a la lesión muscular
Para entender cómo encaja PAI-1 en esta historia, los investigadores usaron un modelo de ratón bien establecido de lesión del músculo esquelético. Se inyectó una toxina en los músculos de la pierna para causar un daño controlado seguido de una reparación sincronizada. Al principio, tras la lesión, una oleada de macrófagos inflamatorios con marcadores llamados CCR2 y Ly6C invadió el músculo. Estos macrófagos en particular resultaron ser productores prolíficos de PAI-1 justo en el sitio de la lesión. Cuando se eliminó el gen de PAI-1 en ratones, o cuando la actividad de PAI-1 se bloqueó con una pequeña molécula, las fibras musculares dañadas se limpiaron más rápido, las señales inflamatorias disminuyeron y la arquitectura normal en panal del músculo se restableció con mayor rapidez. Estos beneficios aparecieron incluso cuando otras fuentes de PAI-1 en el organismo seguían presentes, lo que apunta a un efecto local potente.
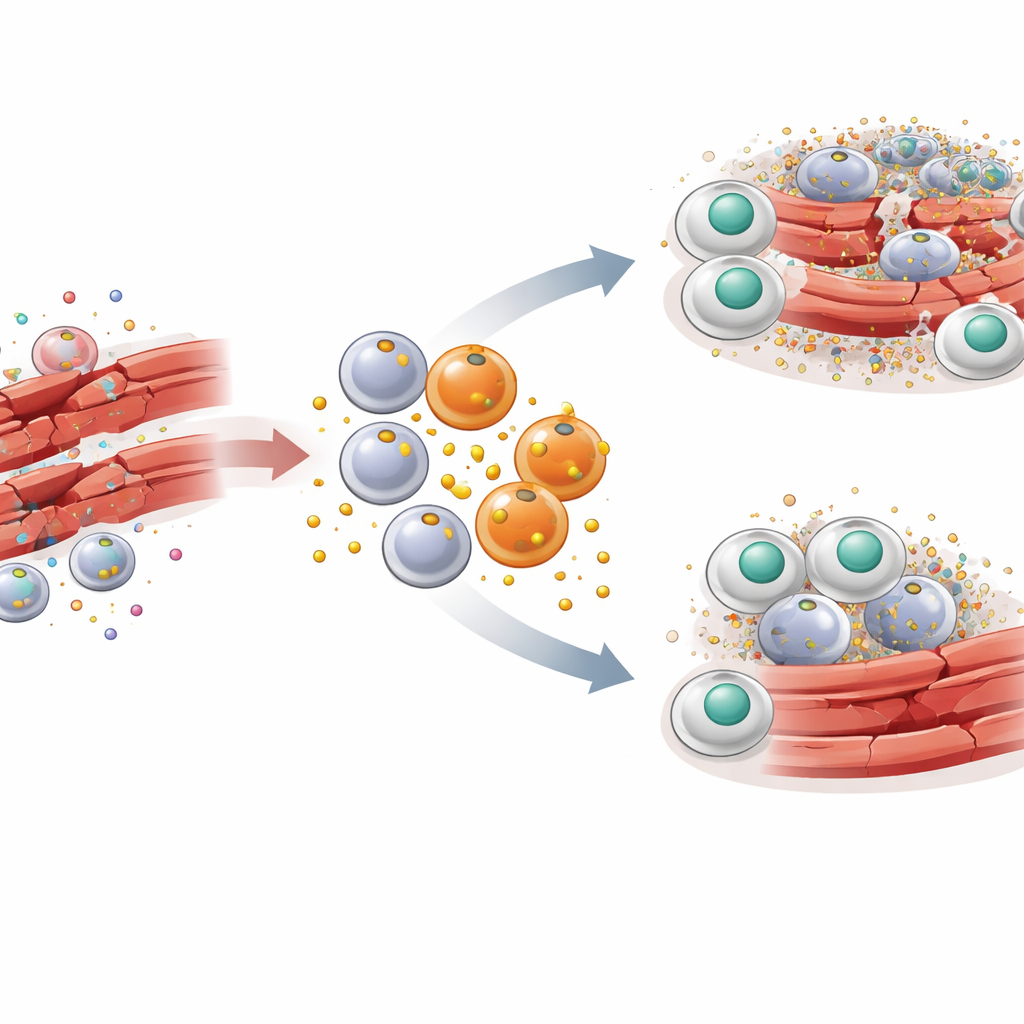
Cómo un inhibidor de señales bloquea la limpieza celular
El hallazgo clave es que PAI-1 actúa como una especie de inhibidor de señales para la eferocitosis. Las células moribundas exponen en su superficie una molécula llamada calreticulina, que sirve como una bandera de «cómeme». Los macrófagos portan un receptor llamado LRP-1 que reconoce la calreticulina y desencadena el engullimiento de la célula moribunda. El equipo encontró que PAI-1 también se une a LRP-1—y lo hace con mayor afinidad que la calreticulina. En experimentos con cultivos celulares, la adición de PAI-1 redujo la capacidad de los macrófagos para engullir células muertas, mientras que eliminar PAI-1 o bloquear su unión a LRP-1 potenció esta limpieza. Una forma mutante de PAI-1 que ya no podía adherirse a LRP-1 no logró bloquear la eferocitosis, confirmando que la interferencia ocurre en este receptor. En efecto, PAI-1 compite con las señales de «cómeme», dejando a las células muertas varadas y sin eliminar.
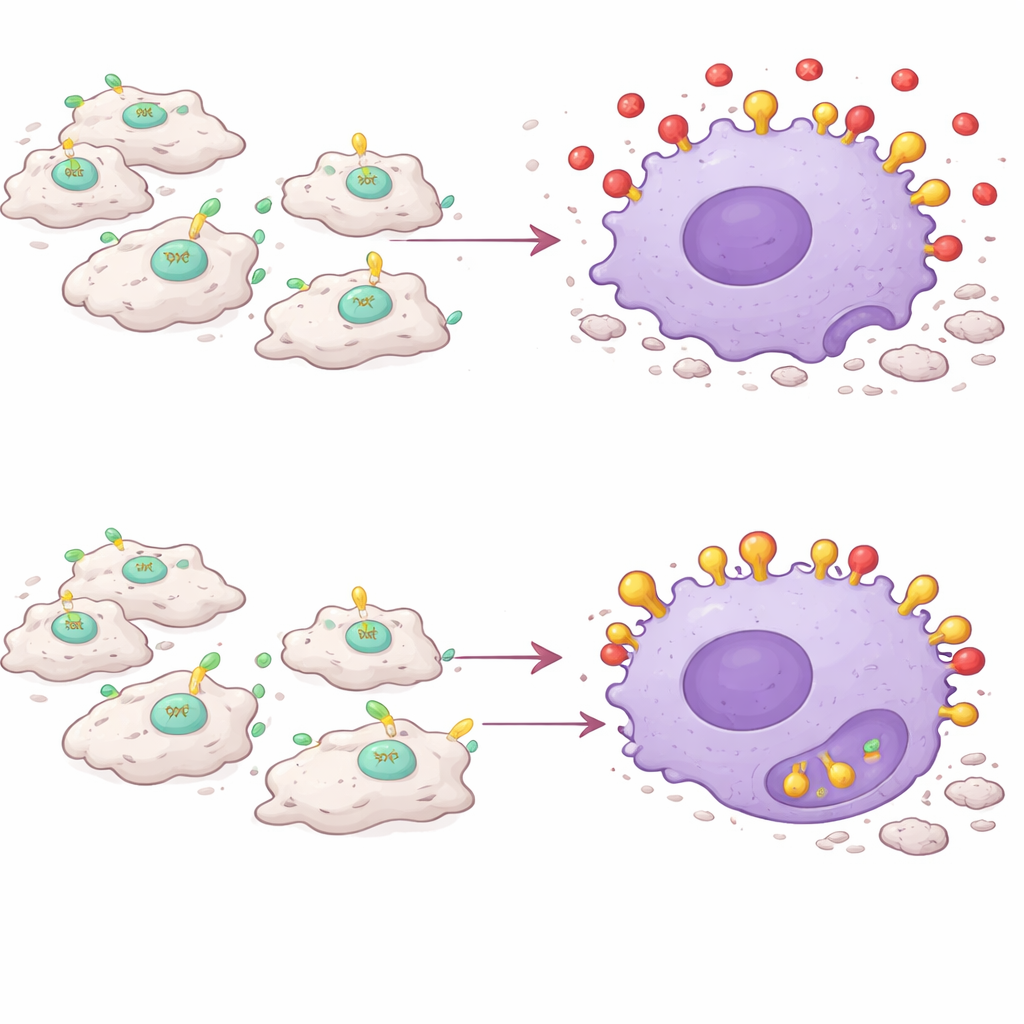
Los macrófagos se vuelven contra su propia tarea
Lo llamativo es que no se trata de cualquier PAI-1, sino del PAI-1 producido por los propios macrófagos inflamatorios. Cuando los investigadores eliminaron selectivamente el gen de PAI-1 solo en macrófagos CCR2+Ly6C+, los músculos lesionados sanaron de forma similar a los de animales con eliminación completa de PAI-1: menos tinción de fibras dañadas, niveles más bajos de mensajeros proinflamatorios y más células musculares regeneradas. Trasplantar macrófagos inflamatorios ricos en PAI-1 a ratones deficientes en PAI-1 fue suficiente para restaurar la inflamación prolongada y la curación retrasada, aunque el resto del organismo careciera de PAI-1. En animales vivos, tanto la eliminación genética como la inhibición farmacológica de PAI-1 aumentaron la captación por parte de macrófagos de partículas trazadoras, lo que indica un comportamiento de engullimiento más activo durante la inflamación.
Abrir un nuevo camino para el tratamiento
Al mostrar que el PAI-1 derivado de macrófagos bloquea la eliminación de células muertas, este estudio vincula un regulador de la coagulación bien conocido con la incapacidad de la inflamación para apagarse por sí misma. Cuando PAI-1 desplaza las señales normales de «cómeme» en los receptores de los macrófagos, los desechos permanecen y la reparación tisular se estanca. Un fármaco que inhibe PAI-1, administrado por vía oral, restableció la limpieza y aceleró la regeneración muscular en ratones, sugiriendo una vía práctica para ayudar a los tejidos a recuperarse tras una lesión. Dado que una mala eferocitosis y niveles altos de PAI-1 son características comunes en muchas condiciones inflamatorias crónicas y relacionadas con la edad, dirigir esta vía podría algún día ofrecer una nueva clase de terapias antiinflamatorias que no actúen simplemente atenuando las respuestas inmunitarias, sino ayudando al cuerpo a completar la tarea de curación.
Cita: Ibrahim, A.A., Miura, H., Terada, T. et al. Inflammatory macrophage-derived plasminogen activator inhibitor-1 exacerbates inflammation through efferocytosis inhibition. Cell Death Discov. 12, 195 (2026). https://doi.org/10.1038/s41420-026-03076-0
Palabras clave: inflamación, macrófagos, reparación muscular, limpieza celular, inhibidor de PAI-1