Clear Sky Science · he
מעכב הפלסמינוגן-1 שמקורו במקרופאגים דלקתיים מחמיר דלקת על ידי עיכוב אפרוציטוזה
כשצוותי הניקיון טועים
גופנו מסתמך על "צוותי ניקיון" חיסוניים כדי לפנות תאים מתים ופגועים לאחר פגיעה. המחקר הזה מגלה כיצד חלבון קטן אחד, המכונה PAI-1, יכול להפוך את תאי הניקיון האלה ממועילים למניעים של דלקת מתמשכת. על ידי חסימת הסילוק הבטוח של שברי תאים, PAI-1 משאיר את הרקמה הפגועה במצב של ריפוי איטי וגירוי כרוני — תובנה שעשויה לפתוח דרכים חדשות לטיפול בנזק לשריר ובמחלות דלקתיות אחרות.
מדלקת מועילה לנפיחות מזיקה
דלקת נועדה להיות זמנית. כאשר רקמה נפגעת, תאים חיסוניים מתריעים, מסירים שברי תאים ולאחר מכן מסייעים בבניית מבנה בריא מחדש. שחקן מרכזי בתהליך זה הוא המקרופאג, תא רב-תכליתי היכול לעורר דלקת וגם לסייע בסיומה. מקרופאגים "אוכלים" תאים מתים בתהליך הנקרא אפרוציטוזה, המונחה על ידי אותות על פני השטח שמסמנים אילו תאים יש להסיר ואילו יש להשאיר. אם שלב הניקוי הזה נכשל, תאים מתים ותוכנם נערמים, ומשאירים את הרקמות מוצפות באותות סכנה שיכולים להזין דלקת ממושכת הקשורה למחלות לב, סוכרת, מצבי אוטואימוניות ואפילו סרטן.
מבט קרוב יותר על פגיעה בשריר
כדי להבין היכן משתלב PAI-1 בסיפור הזה, החוקרים השתמשו במודל עכבר מבוסס היטב של פגיעה בשריר השלד. הוחדר רעלן לשרירי הרגל כדי לגרום לנזק מבוקר ולאחריו תיקון מסונכרן. זמן קצר לאחר הפגיעה, גל של מקרופאגים דלקתיים הנושאים סמנים הקרויים CCR2 ו-Ly6C שטפו את השריר. מקרופאגים אלה התגלו כמפיקים שופעים של PAI-1 ממש באתר הפגיעה. כאשר גן PAI-1 הושבת בעכברים, או כאשר פעילות PAI-1 נחסמה בעזרת תרופה קט מולקולרית, סיבי שריר פגועים ניקו מהר יותר, אותות דלקת ירדו, ומבנה השריר דמוי הכוורת שוחזר מהר יותר. התועלות האלה הופיעו למרות שמקורות אחרים של PAI-1 בגוף נותרו נוכחים, מה שמרמז על אפקט מקומי חזק.
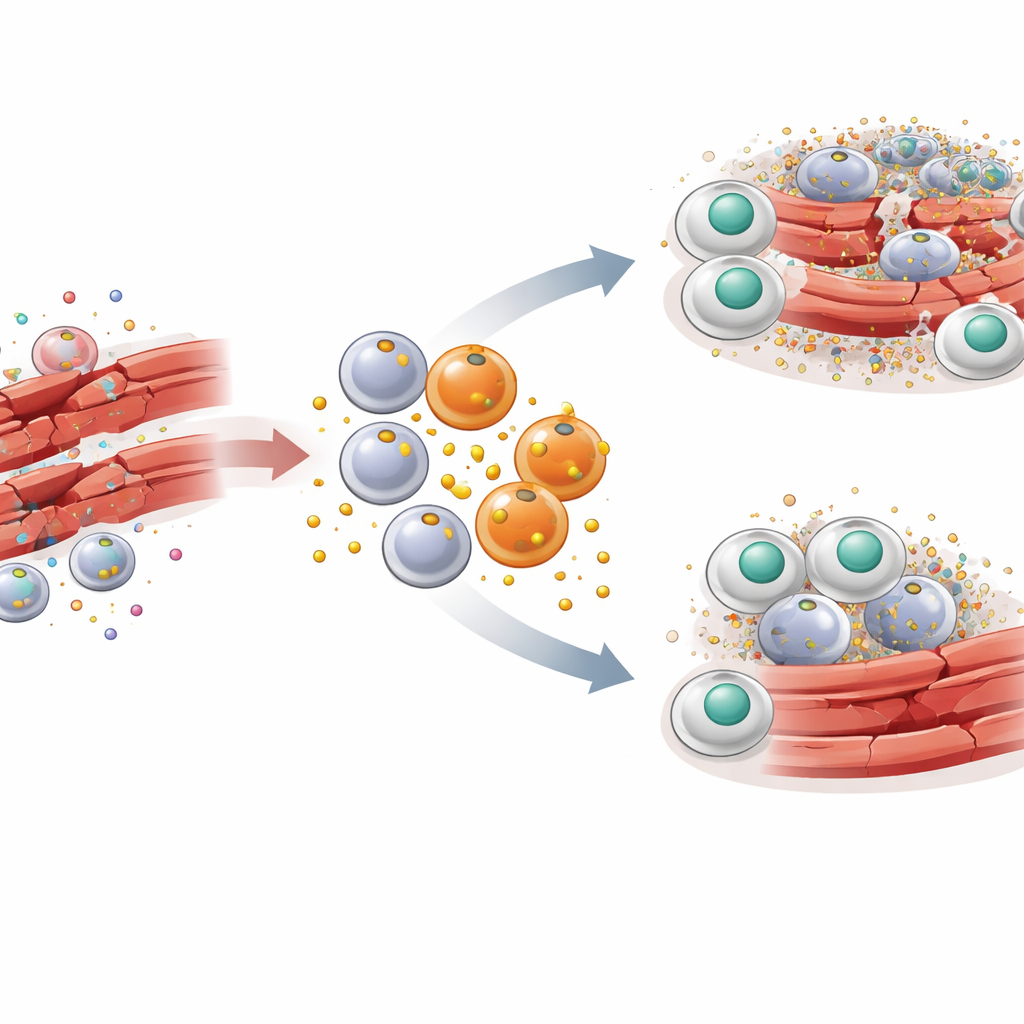
כיצד ג'אמר אותות חוסם את ניקוי התאים
הממצא המרכזי הוא ש-PAI-1 פועל כמעין ג'אמר אותות לאפרוציטוזה. תאים מתים חושפים מולקולה בשם קלרטיקולין על פני השטח שלהם, המשמשת כדגל "אכל אותי". מקרופאגים נושאים רצפטור הנקרא LRP-1 שמזהה את הקלרטיקולין ומפעיל בליעה של התא המת. החוקרים מצאו ש-PAI-1 גם נקשר ל-LRP-1 — ועושה זאת בעלות זיקה גבוהה יותר מאשר קלרטיקולין. בניסויי תרבית תאים, הוספת PAI-1 הקטינה את יכולת המקרופאגים לבלוע תאים מתים, בעוד שהסרת PAI-1 או חסימת הקשירה שלו ל-LRP-1 חיזקה את הניקוי הזה. צורת מוטנטית של PAI-1 שלא יכלה להיצמד ל-LRP-1 נכשלה בבלימת האפרוציטוזה, מה שאושש שההתערבות מתרחשת על הרצפטור הזה. במעשׂה, PAI-1 מתחרה על אותות "אכל אותי", ומשאירה תאים מתים נטושים ללא סילוק.
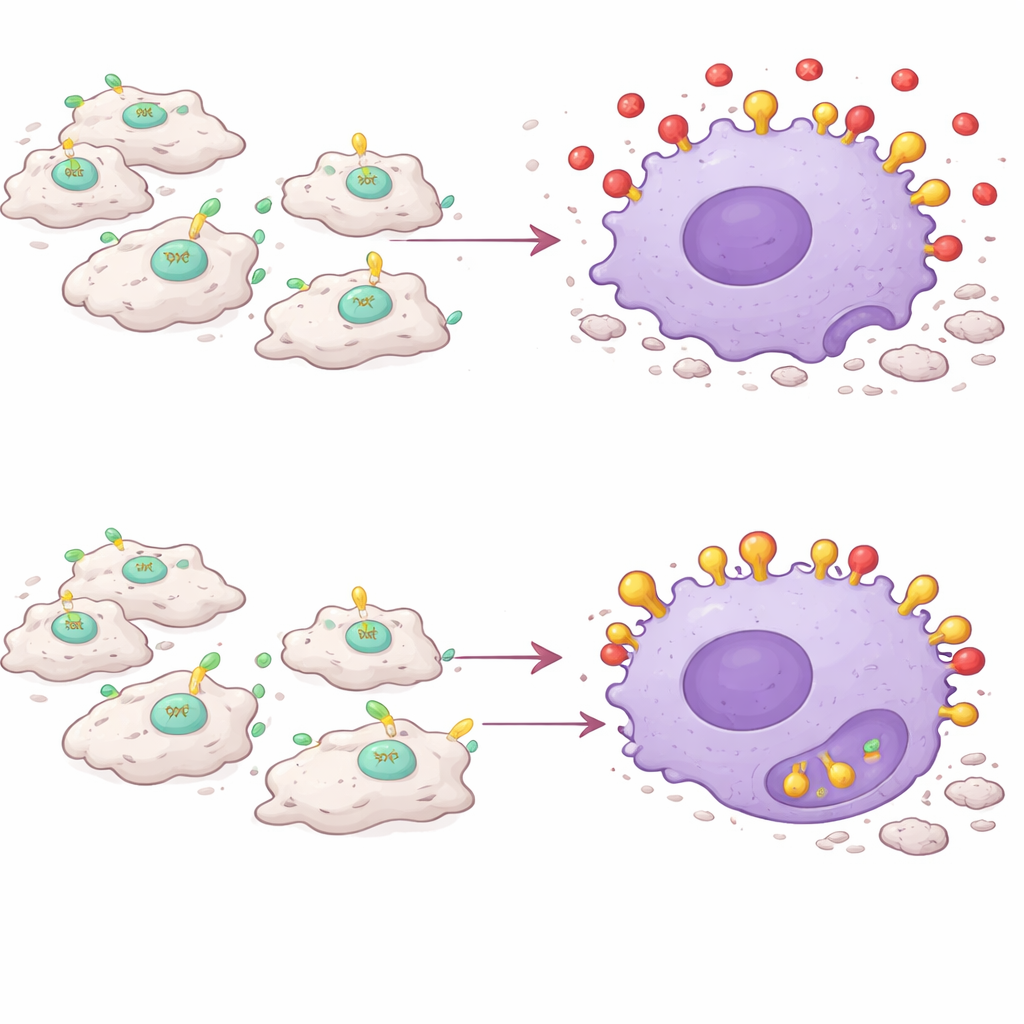
מקרופאגים פונים נגד משימתם
מרשים במיוחד הוא שלא כל PAI-1 משנה את המצב, אלא דווקא ה-PAI-1 שמיוצר על ידי מקרופאגים דלקתיים עצמם. כאשר החוקרים מחקו באופן סלקטיבי את גן PAI-1 רק במקרופאגים CCR2+Ly6C+, השרירים הפגועים התאוששו בדומה לאלה בעכברי נוקאאוט מלא של PAI-1: צביעה מופחתת של סיבים פגועים, רמות נמוכות יותר של מטילים פרו-דלקתיים, ויותר תאים שריריים מתחדשים. השתלת מקרופאגים דלקתיים עשירים ב-PAI-1 לעכברים חסרי PAI-1 הספיקה להשיב דלקת ממושכת ועיכוב בריפוי, למרות ששאר הגוף היה חסר PAI-1. בחיות חיות, הן השמטה גנטית והן עיכוב תרופתי של PAI-1 הגדילו את קליטת חלקיקי סימון על ידי מקרופאגים, מה שמעיד על פעילות בליעה מוגברת במהלך הדלקת.
פתיחת נתיב טיפולי חדש
על ידי הצגת כך ש-PAI-1 שמקורו במקרופאגים חוסם את סילוק התאים המתים, המחקר מקשר בין ווסת קרישה מוכר לבין כישלון סגירתה של הדלקת. כאשר PAI-1 דוחק החוצה את אותות ה"אכל אותי" הרגילים ברצפטורים של מקרופאגים, השיירים נמשכים ותיקון הרקמה נעצר. תרופה שמעכבת PAI-1 שניתנה דרך הפה החזירה את פעולת הניקוי וזרזה את התחדשות השריר בעכברים, מה שמרמז על דרך מעשית לסייע לרקמות להתאושש לאחר פגיעה. כיוון שאפרוציטוזה לקויה ורמות גבוהות של PAI-1 הן תכונות נפוצות של מצבים דלקתיים כרוניים ומחלות הקשורות להזדקנות, מיקוד במסלול זה עשוי יום אחד להציע מחלקה חדשה של טיפולים אנטי-דלקתיים שאינם מסתפקים בדיכוי תגובות חיסוניות, אלא מסייעים לגוף לסיים את מלאכת הריפוי.
ציטוט: Ibrahim, A.A., Miura, H., Terada, T. et al. Inflammatory macrophage-derived plasminogen activator inhibitor-1 exacerbates inflammation through efferocytosis inhibition. Cell Death Discov. 12, 195 (2026). https://doi.org/10.1038/s41420-026-03076-0
מילות מפתח: דלקת, מקרופאגים, תיקון שריר, ניקוי תאים, מעכב PAI-1