Clear Sky Science · de
Durch entzündliche Makrophagen stammender Plasminogenaktivator-Inhibitor‑1 verschärft Entzündungen durch Hemmung der Efferocytose
Wenn die Aufräumtruppen fehlgehen
Unser Körper ist auf Immun‑„Aufräumtruppen“ angewiesen, die nach Verletzungen tote und geschädigte Zellen beseitigen. Diese Studie zeigt, wie ein kleines Protein namens PAI‑1 jene hilfreichen Aufräumzellen in Treiber anhaltender Entzündung verwandeln kann. Indem PAI‑1 die sichere Entsorgung zellulärer Überreste blockiert, hält es verletztes Gewebe in einem Zustand langsamer Heilung und chronischer Reizung – eine Einsicht, die neue Wege zur Behandlung von Muskelschäden und anderen entzündlichen Erkrankungen eröffnen könnte.
Von nützlicher Entzündung zu schädlicher Schwellung
Entzündung ist eigentlich vorübergehend gedacht. Bei Gewebsschäden eilen Immunzellen herbei, räumen Trümmer weg und unterstützen den Wiederaufbau gesunder Strukturen. Ein Schlüsselakteur dabei ist der Makrophage, eine vielseitige Zelle, die sowohl Entzündungen auslösen als auch zu ihrer Beendigung beitragen kann. Makrophagen „fressen“ sterbende Zellen in einem Prozess, der als Efferocytose bekannt ist, gesteuert von Oberflächen‑Signalen, die markieren, welche Zellen entfernt werden sollen und welche unberührt bleiben. Scheitert dieser Räumungsschritt, sammeln sich tote Zellen und deren Inhalte an und fluten das Gewebe mit Gefahrensignalen, die langanhaltende Entzündungen antreiben können — verbunden mit Herzkrankheiten, Diabetes, Autoimmunerkrankungen und sogar Krebs.
Ein genauerer Blick auf Muskelverletzung
Um zu verstehen, welche Rolle PAI‑1 in diesem Prozess spielt, verwendeten die Forschenden ein gut etabliertes Mausmodell für Skelettmuskelverletzung. Ein Toxin wurde in Beinmuskeln injiziert, um kontrollierte Schäden zu erzeugen, gefolgt von synchroner Reparatur. Kurz nach der Verletzung strömte eine Welle entzündlicher Makrophagen mit den Markern CCR2 und Ly6C in den Muskel ein. Diese speziellen Makrophagen erwiesen sich als ergiebige Produzenten von PAI‑1 direkt an der Verletzungsstelle. Wurde das PAI‑1‑Gen in Mäusen ausgeschaltet oder die Aktivität von PAI‑1 mit einem kleinen Molekül gehemmt, klärten beschädigte Muskelfasern schneller, entzündliche Signale sanken und die normale, wabenartige Architektur des Muskels stellte sich schneller wieder her. Diese Vorteile traten auf, obwohl andere PAI‑1‑Quellen im Körper weiterhin vorhanden waren, was auf eine starke lokale Wirkung hinweist.
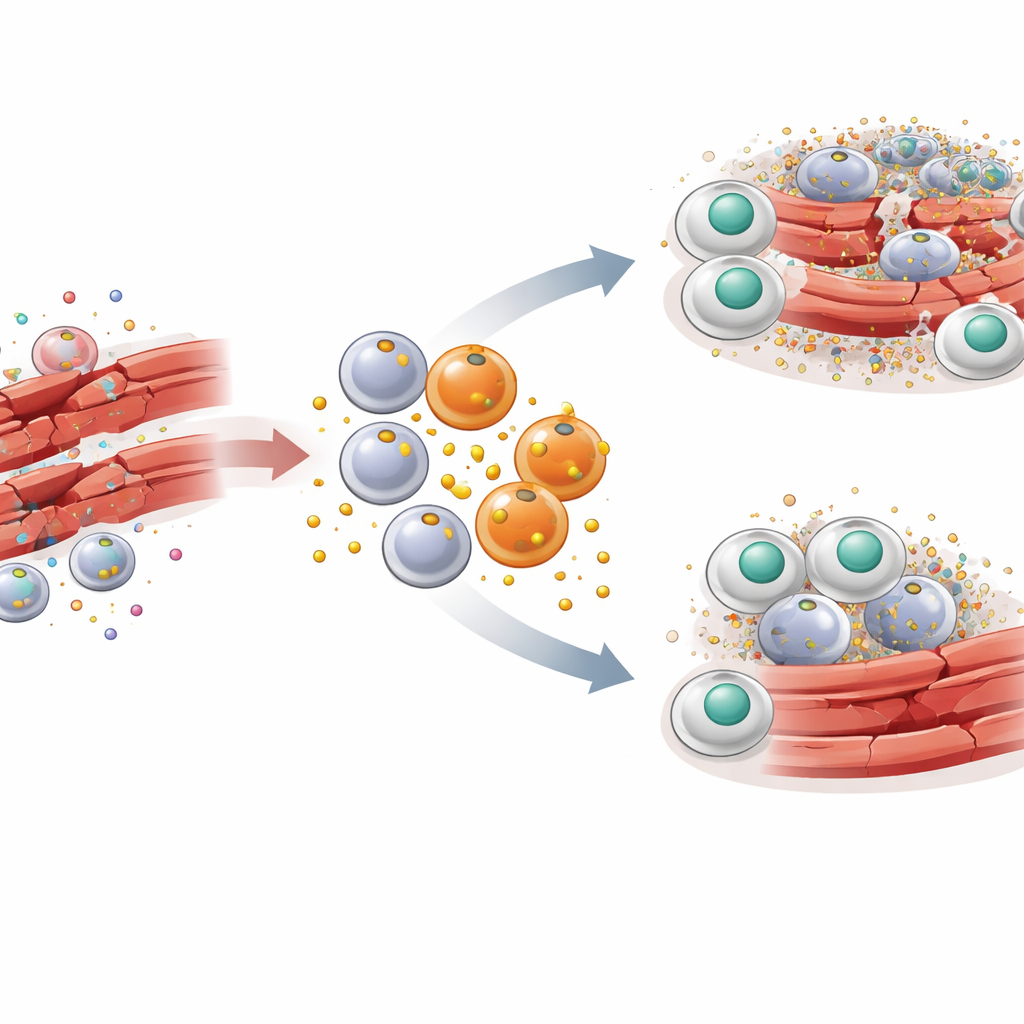
Wie ein Signalstörer die zellulare Räumung blockiert
Die zentrale Entdeckung ist, dass PAI‑1 wie ein Signalstörer für die Efferocytose wirkt. Sterbende Zellen präsentieren ein Molekül namens Calreticulin auf ihrer Oberfläche, das als „Iss mich“-Flagge dient. Makrophagen tragen einen Rezeptor namens LRP‑1, der Calreticulin erkennt und die Verschlingung der sterbenden Zelle auslöst. Das Team fand heraus, dass PAI‑1 ebenfalls an LRP‑1 bindet — und dies mit höherer Affinität als Calreticulin. In Zellkulturversuchen reduzierte zugefügtes PAI‑1 die Fähigkeit von Makrophagen, tote Zellen aufzunehmen, während das Entfernen von PAI‑1 oder das Blockieren seiner Bindung an LRP‑1 diese Räumung verbesserte. Eine Mutante von PAI‑1, die nicht mehr an LRP‑1 andocken konnte, scheiterte daran, die Efferocytose zu blockieren, was bestätigt, dass die Interferenz an diesem Rezeptor stattfindet. Effektiv übertrumpft PAI‑1 die „Iss mich“-Signale, sodass tote Zellen zurückbleiben und nicht beseitigt werden.
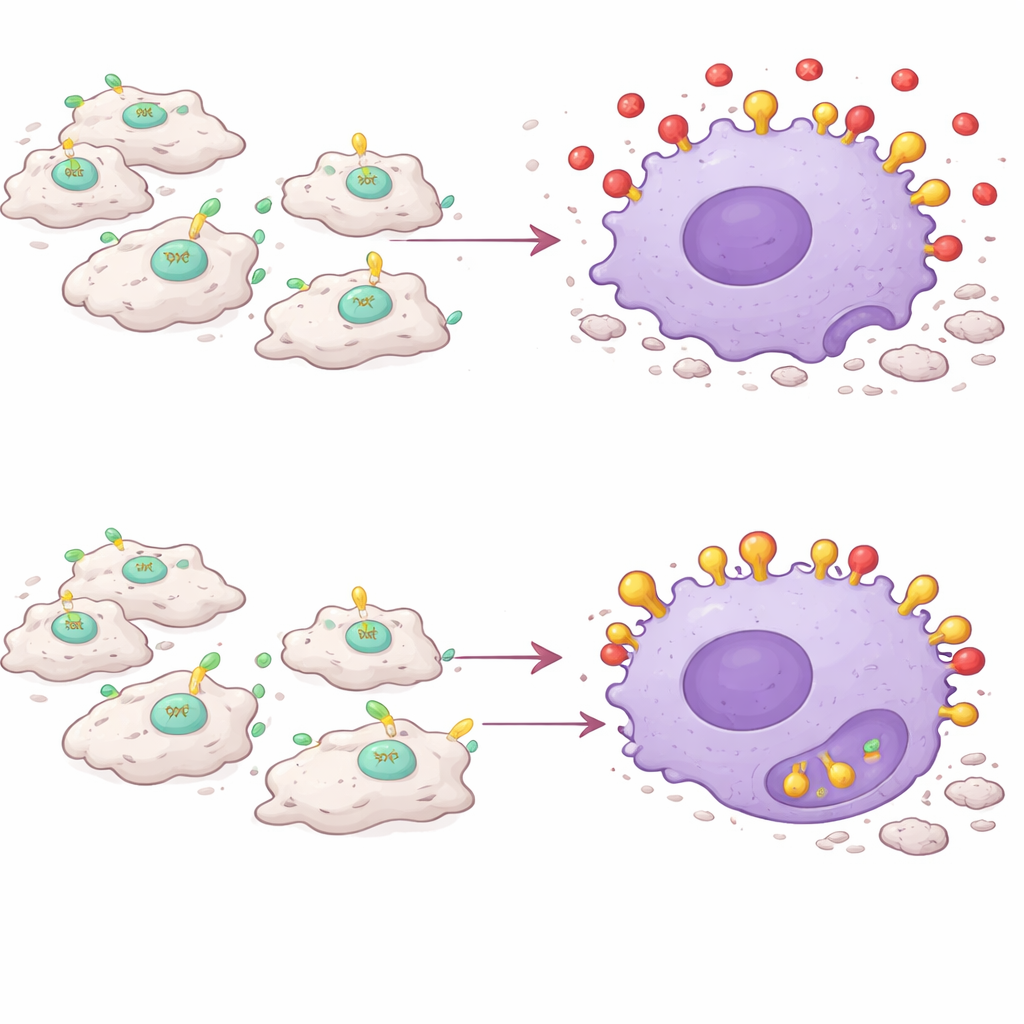
Makrophagen wenden sich gegen ihre eigene Aufgabe
Bemerkenswerterweise ist nicht irgendein PAI‑1 ausschlaggebend, sondern das PAI‑1, das von entzündlichen Makrophagen selbst produziert wird. Als die Forschenden gezielt das PAI‑1‑Gen nur in CCR2+Ly6C+ Makrophagen löschten, heilten verletzte Muskeln ähnlich wie in vollständigen PAI‑1‑Nulltieren: weniger Färbung geschädigter Fasern, geringere Werte pro‑entzündlicher Botenstoffe und mehr regenerierte Muskelzellen. Die Transplantation PAI‑1‑reicher entzündlicher Makrophagen in PAI‑1‑defiziente Mäuse reichte aus, um anhaltende Entzündung und verzögerte Heilung wiederherzustellen, obwohl der Rest des Körpers kein PAI‑1 aufwies. In lebenden Tieren führten sowohl genetische Deletion als auch medikamentöse Hemmung von PAI‑1 zu einer erhöhten Aufnahme von Markerkügelchen durch Makrophagen, was auf aktiveres Verschlingungsverhalten während der Entzündung hinweist.
Ein neuer Behandlungsansatz öffnet sich
Indem gezeigt wird, dass von Makrophagen stammendes PAI‑1 die Beseitigung toter Zellen blockiert, verbindet diese Studie einen bekannten Gerinnungsregulator mit dem Versagen der Entzündung, sich selbst zu beenden. Wenn PAI‑1 die normalen „Iss mich“-Signale an Makrophagen‑Rezeptoren verdrängt, verbleiben Trümmer und die Gewebereparatur kommt ins Stocken. Ein oral verabreichbares Medikament, das PAI‑1 hemmt, stellte in Mäusen die Räumung wieder her und beschleunigte die Muskelregeneration, was auf einen praktikablen Weg hindeutet, das Gewebe nach Verletzung zu unterstützen. Da mangelhafte Efferocytose und hohe PAI‑1‑Spiegel gemeinsame Merkmale vieler chronischer entzündlicher und altersbedingter Erkrankungen sind, könnte die gezielte Beeinflussung dieses Weges eines Tages eine neue Klasse von Anti‑Entzündungs‑Therapien bieten, die nicht bloß die Immunantwort dämpfen, sondern dem Körper helfen, die Heilung abzuschließen.
Zitation: Ibrahim, A.A., Miura, H., Terada, T. et al. Inflammatory macrophage-derived plasminogen activator inhibitor-1 exacerbates inflammation through efferocytosis inhibition. Cell Death Discov. 12, 195 (2026). https://doi.org/10.1038/s41420-026-03076-0
Schlüsselwörter: Entzündung, Makrophagen, Muskelreparatur, Zellräumung, PAI‑1‑Inhibitor