Clear Sky Science · it
L’inibitore dell’attivatore del plasminogeno 1 derivato da macrofagi infiammatori peggiora l’infiammazione bloccando l’efferocitosi
Quando le squadre di pulizia sbagliano
I nostri corpi dipendono da “squadre di pulizia” immunitarie che rimuovono cellule morte e danneggiate dopo un’infortunio. Questo studio rivela come una piccola proteina, chiamata PAI-1, possa trasformare queste cellule di pulizia utili in promotrici di infiammazione persistente. Bloccando lo smaltimento sicuro dei detriti cellulari, PAI-1 mantiene il tessuto lesionato in uno stato di guarigione lenta e irritazione cronica — un risultato che potrebbe aprire nuove strade per trattare il danno muscolare e altre malattie infiammatorie.
Dall’infiammazione utile al gonfiore dannoso
L’infiammazione dovrebbe essere temporanea. Quando un tessuto è lesionato, le cellule immunitarie accorrono, rimuovono i detriti e aiutano a ricostruire una struttura sana. Un attore chiave in questo processo è il macrofago, una cellula versatile che può sia scatenare l’infiammazione sia contribuire alla sua risoluzione. I macrofagi “mangiano” le cellule morenti in un processo noto come efferocitosi, guidato da segnali di superficie che indicano quali cellule devono essere rimosse e quali lasciate intatte. Se questo passaggio di pulizia fallisce, le cellule morte e i loro contenuti si accumulano, immergendo i tessuti in segnali di pericolo che possono alimentare un’infiammazione prolungata associata a malattie cardiache, diabete, patologie autoimmuni e persino cancro.
Uno sguardo più da vicino alla lesione muscolare
Per capire come PAI-1 si inserisca in questa storia, i ricercatori hanno utilizzato un modello murino ben consolidato di lesione del muscolo scheletrico. Una tossina è stata iniettata nei muscoli della gamba per causare un danno controllato seguito da una riparazione sincronizzata. Nelle fasi iniziali dopo la lesione, un’ondata di macrofagi infiammatori con marcatori chiamati CCR2 e Ly6C ha invaso il muscolo. Questi macrofagi si sono rivelati produttori prolifici di PAI-1 proprio nel sito della lesione. Quando il gene del PAI-1 è stato eliminato nei topi, o quando l’attività di PAI-1 è stata bloccata con una piccola molecola, le fibre muscolari danneggiate sono state rimosse più rapidamente, i segnali infiammatori sono diminuiti e l’architettura normale del muscolo, simile a un alveare, si è ristabilita più velocemente. Questi benefici sono comparsi nonostante altre fonti di PAI-1 nel corpo fossero ancora presenti, indicando un forte effetto locale.
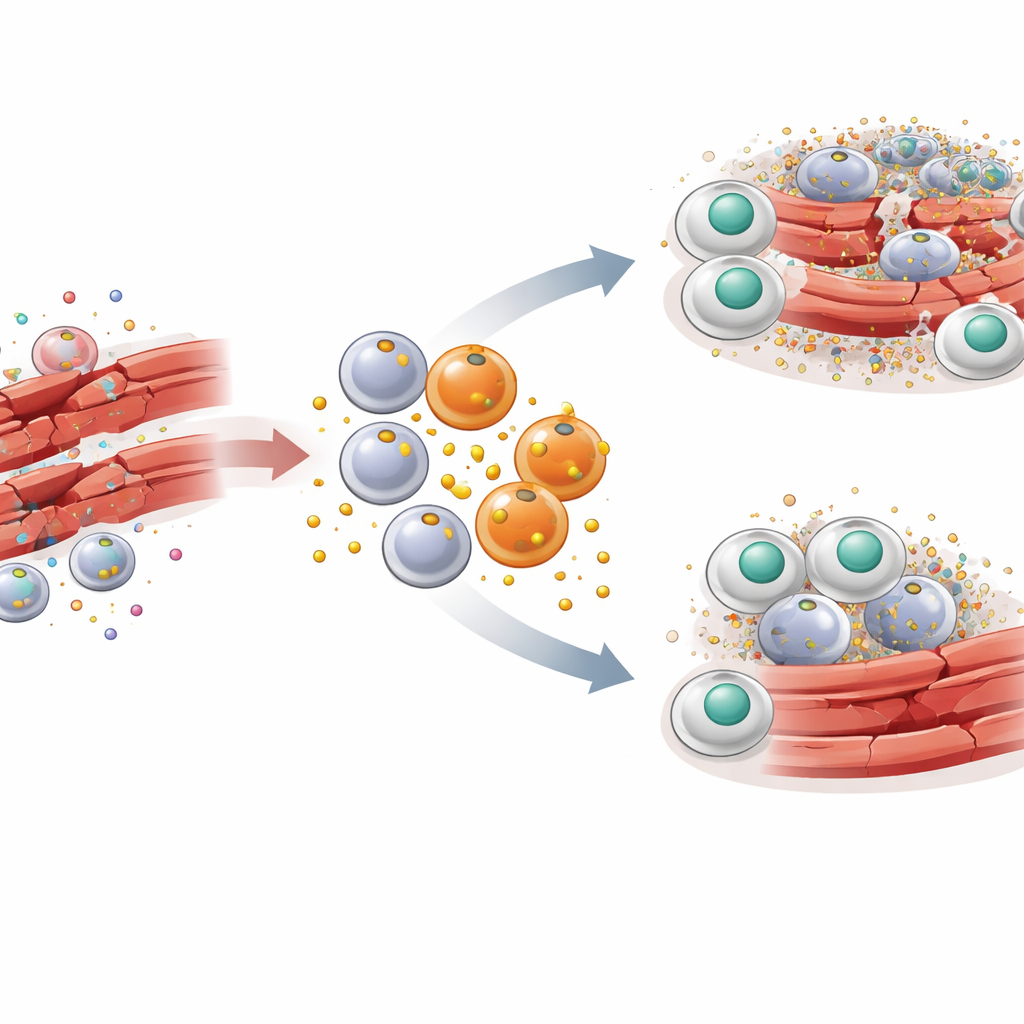
Come un disturbatore di segnali blocca la pulizia cellulare
La scoperta fondamentale è che PAI-1 agisce come una specie di disturbatore di segnali per l’efferocitosi. Le cellule morenti espongono una molecola chiamata calreticulina sulla loro superficie, che funge da bandiera “mangiami”. I macrofagi portano un recettore chiamato LRP-1 che riconosce la calreticulina e innesca l’inglobamento della cellula morente. Il gruppo ha scoperto che PAI-1 si lega anche a LRP-1 — e lo fa con affinità maggiore rispetto alla calreticulina. In esperimenti in coltura cellulare, l’aggiunta di PAI-1 ha ridotto la capacità dei macrofagi di ingerire cellule morte, mentre la rimozione di PAI-1 o il blocco del suo legame con LRP-1 ha potenziato questa pulizia. Una forma mutante di PAI-1 che non poteva più attaccarsi a LRP-1 non è riuscita a bloccare l’efferocitosi, confermando che l’interferenza avviene a livello di questo recettore. In pratica, PAI-1 compete con i segnali “mangiami”, lasciando le cellule morte isolate e non rimosse.
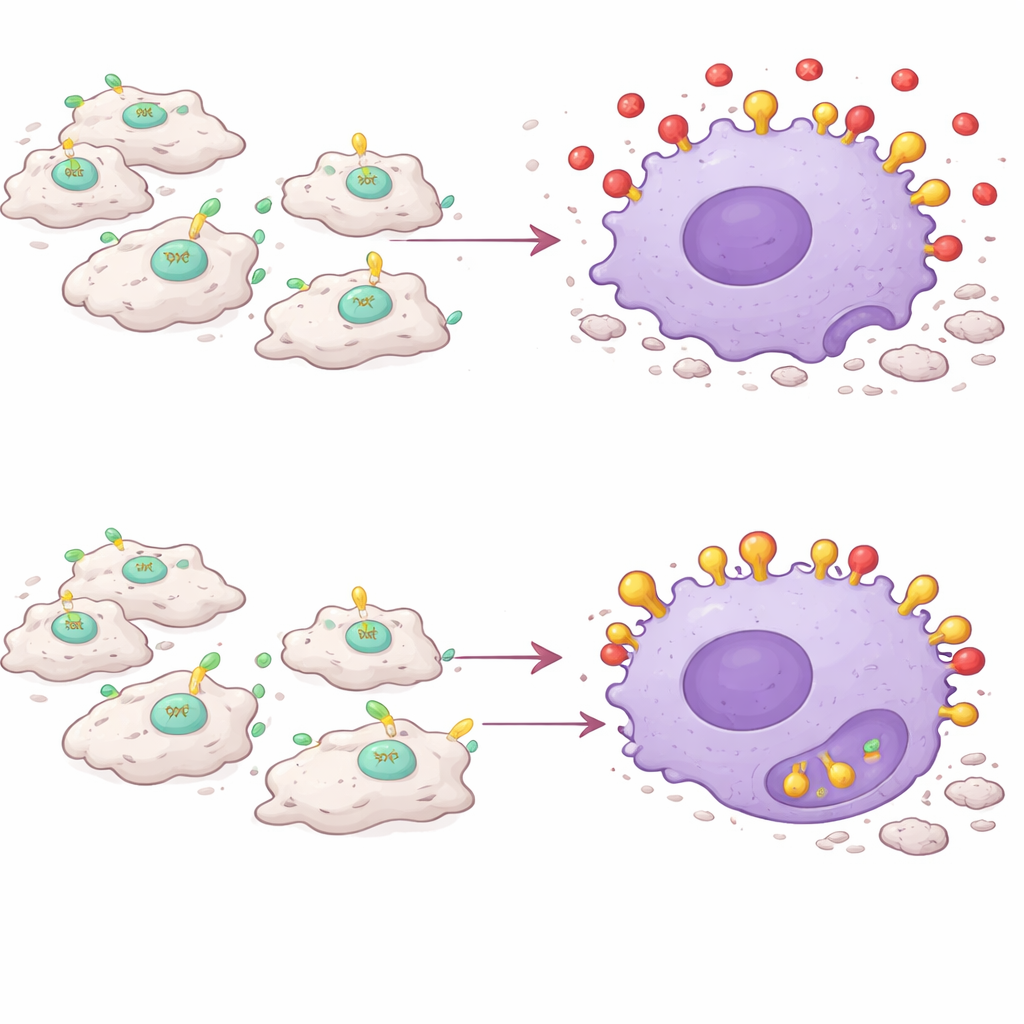
I macrofagi si voltano contro il proprio compito
Colpisce il fatto che non è qualsiasi PAI-1 a essere importante, ma il PAI-1 prodotto dagli stessi macrofagi infiammatori. Quando i ricercatori hanno eliminato selettivamente il gene del PAI-1 solo nei macrofagi CCR2+Ly6C+, i muscoli lesionati hanno guarito in modo molto simile a quelli di animali con il PAI-1 completamente inattivato: minore presenza di fibre danneggiate, livelli più bassi di messaggeri pro-infiammatori e più cellule muscolari rigenerate. Trapiantare macrofagi infiammatori ricchi di PAI-1 in topi privi di PAI-1 è stato sufficiente a ripristinare l’infiammazione prolungata e la guarigione ritardata, nonostante il resto del corpo fosse privo di PAI-1. Negli animali vivi, sia la delezione genetica sia l’inibizione farmacologica di PAI-1 hanno aumentato l’assorbimento da parte dei macrofagi di particelle traccianti, indicando un comportamento di inglobamento più attivo durante l’infiammazione.
Aprire una nuova strada per il trattamento
Dimostrando che il PAI-1 derivato dai macrofagi blocca la rimozione delle cellule morte, questo studio collega un noto regolatore della coagulazione al fallimento dell’infiammazione nel spegnersi da sola. Quando PAI-1 soffoca i normali segnali “mangiami” sui recettori dei macrofagi, i detriti persistono e la riparazione tissutale si arresta. Un farmaco che inibisce PAI-1, somministrato per via orale, ha ripristinato la pulizia e accelerato la rigenerazione muscolare nei topi, suggerendo un modo pratico per aiutare i tessuti a recuperare dopo una lesione. Poiché una scarsa efferocitosi e livelli elevati di PAI-1 sono caratteristiche comuni di molte condizioni infiammatorie croniche e legate all’età, colpire questa via potrebbe un giorno offrire una nuova classe di terapie anti-infiammatorie che non si limitano ad attenuare la risposta immunitaria, ma aiutano l’organismo a portare a termine il processo di guarigione.
Citazione: Ibrahim, A.A., Miura, H., Terada, T. et al. Inflammatory macrophage-derived plasminogen activator inhibitor-1 exacerbates inflammation through efferocytosis inhibition. Cell Death Discov. 12, 195 (2026). https://doi.org/10.1038/s41420-026-03076-0
Parole chiave: infiammazione, macrofagi, riparazione muscolare, eliminazione cellulare, inibitore PAI-1