Clear Sky Science · sv
Inflammatoriskt makrofagderiverat plasminogenaktivatorhämmare-1 förvärrar inflammation genom hämning av efferocytos
När städlagren går fel
Våra kroppar är beroende av immunsystemets ”städbesättningar” för att avlägsna döda och skadade celler efter skada. Denna studie visar hur ett litet protein, kallat PAI-1, kan förvandla dessa hjälpsamma städceller till drivkrafter bakom kvarstående inflammation. Genom att blockera säker bortforsling av cellulärt skräp håller PAI-1 den skadade vävnaden fast i ett tillstånd av långsam läkning och kronisk irritation — en insikt som kan öppna nya vägar för behandling av muskelskador och andra inflammatoriska sjukdomar.
Från hjälpsam inflammation till skadlig svullnad
Inflammation är tänkt att vara övergående. När vävnad skadas rusar immunceller till platsen, avlägsnar skräp och hjälper sedan återuppbygga frisk struktur. En central aktör i denna process är makrofagen, en mångsidig cell som både kan starta inflammation och bidra till dess upplösning. Makrofager ”äter” döende celler i en process kallad efferocytos, styrd av ytsignaler som markerar vilka celler som ska tas bort och vilka som ska lämnas i fred. Om detta rensningssteg misslyckas, byggs döda celler och deras innehåll upp och badar vävnader i alarmsignaler som kan driva långvarig inflammation kopplad till hjärtsjukdom, diabetes, autoimmuna sjukdomar och till och med cancer.
Närmare granskning av muskelskada
För att förstå hur PAI-1 passar in i denna berättelse använde forskarna en väletablerad musmodell för skelettmuskelskada. Ett toxin injicerades i benmuskler för att orsaka kontrollerad skada följd av synkroniserad reparation. Tidigt efter skadan flödade en våg av inflammatoriska makrofager märkta med CCR2 och Ly6C in i muskeln. Dessa särskilda makrofager visade sig vara produktiva producenter av PAI-1 direkt vid skadestället. När PAI-1-genen stängdes av hos möss, eller när PAI-1:s aktivitet blockerades med ett småmolekylärt läkemedel, rensades skadade muskelfibrer snabbare, inflammatoriska signaler minskade och den normala honungsnitts-lika muskelarkitekturen återställdes snabbare. Dessa fördelar syntes trots att andra källor till PAI-1 i kroppen fortfarande fanns, vilket pekar på en stark lokal effekt.
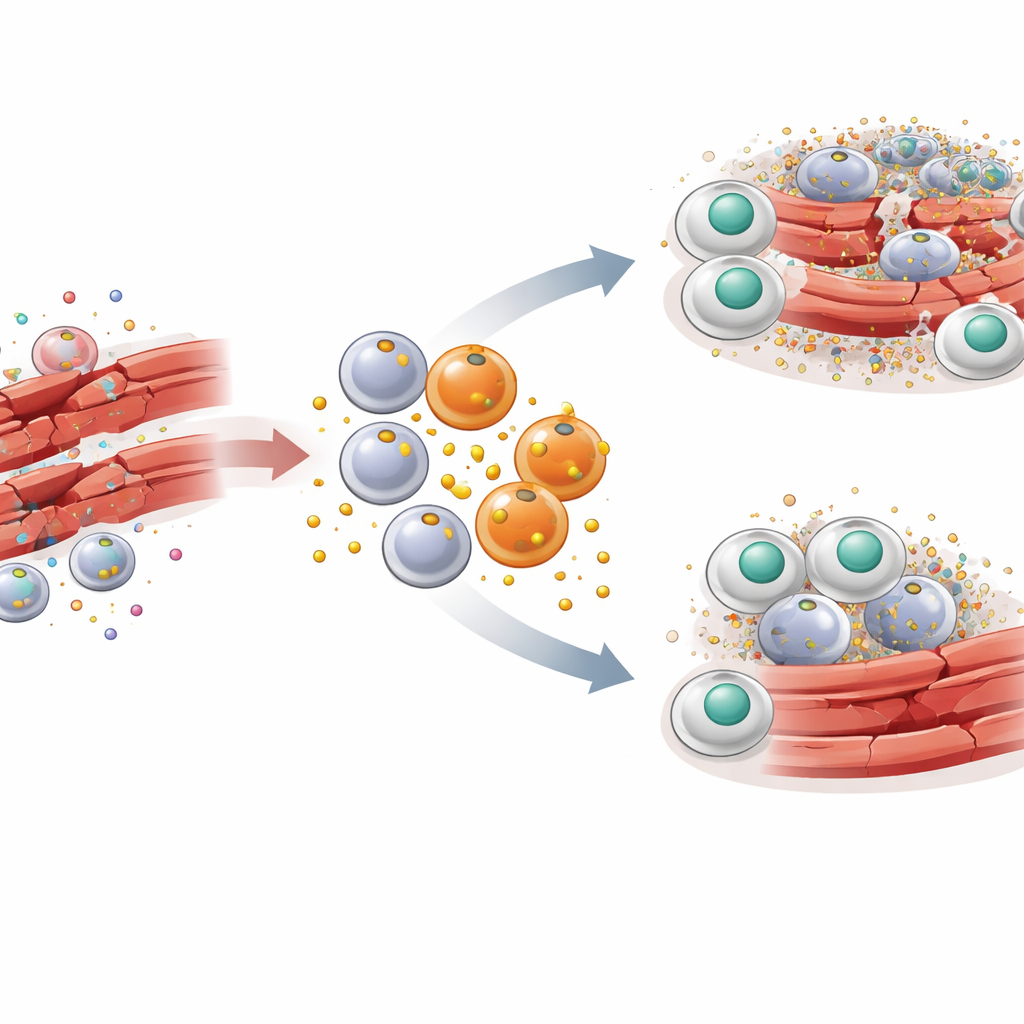
Hur en signalstörning blockerar cellulär sanering
Huvudupptäckten är att PAI-1 fungerar som en slags signalstörning för efferocytos. Döende celler exponerar ett molekylärt protein kallat kalretikulin på sin yta, vilket tjänar som en ”ät mig”-flagga. Makrofager bär en receptor kallad LRP-1 som känner igen kalretikulin och utlöser inneslutning av den döende cellen. Teamet fann att PAI-1 också binder till LRP-1 — och gör det med högre affinitet än kalretikulin. I cellkulturförsök minskade tillsats av PAI-1 makrofagernas förmåga att svälja döda celler, medan borttagning av PAI-1 eller blockering av dess bindning till LRP-1 ökade denna sanering. En mutant form av PAI-1 som inte längre kunde fästa vid LRP-1 misslyckades med att blockera efferocytos, vilket bekräftar att störningen sker vid denna receptor. I praktiken konkurrerar PAI-1 ut ”ät mig”-signalerna, vilket lämnar döda celler strandsatta och orensade.
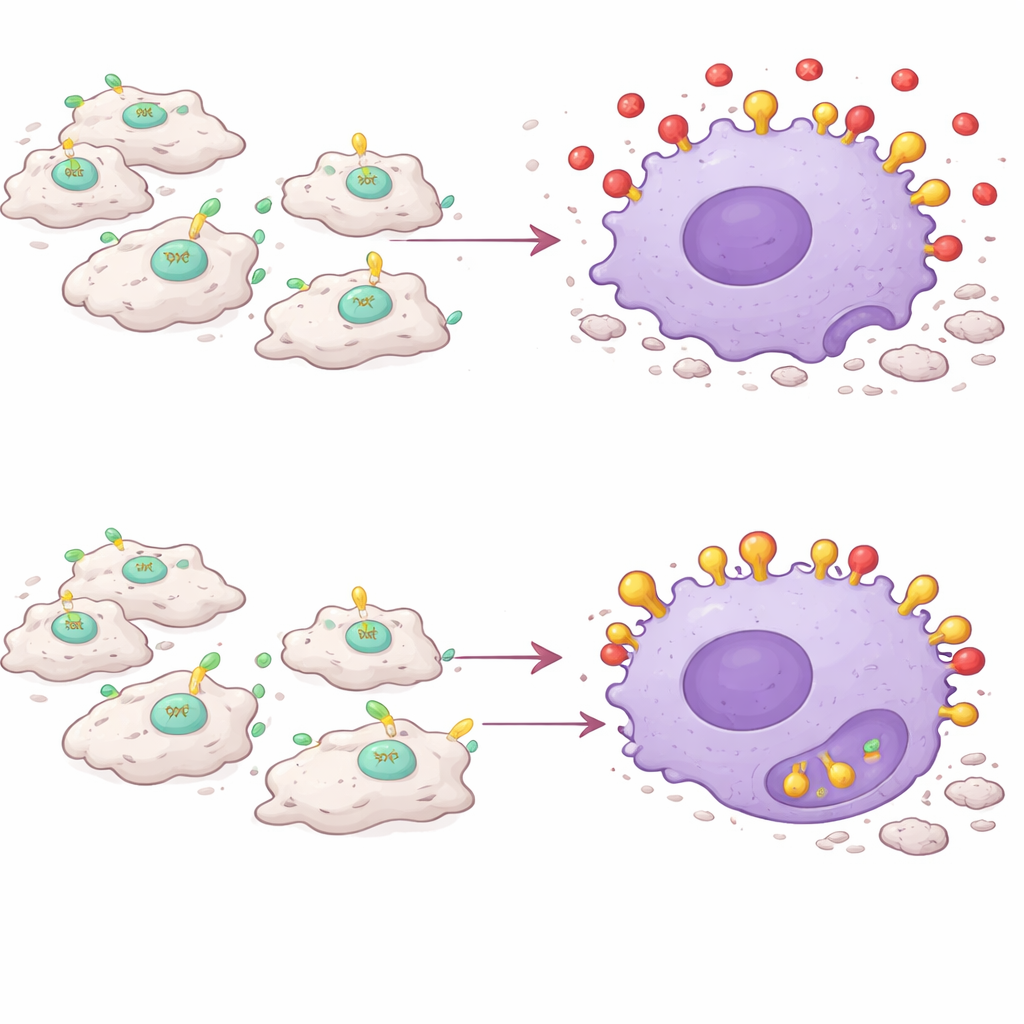
Makrofager vänder sig mot sin egen uppgift
Slående nog är det inte vilken PAI-1 som helst som spelar roll, utan PAI-1 som produceras av de inflammatoriska makrofagerna själva. När forskarna selektivt raderade PAI-1-genen endast i CCR2+Ly6C+ makrofager läkte skadade muskler i hög grad som hos hela PAI-1-utsläckta djur: mindre färgning av skadade fibrer, lägre nivåer av proinflammatoriska budbärare och fler regenererade muskelceller. Att transplantera PAI-1–rika inflammatoriska makrofager till PAI-1–deficienta möss var tillräckligt för att återställa långvarig inflammation och fördröjd läkning, även om resten av kroppen saknade PAI-1. Hos levande djur ökade både genetisk deletion och läkemedelshämning av PAI-1 makrofagernas upptag av spårpartiklar, vilket indikerar mer aktivt inneslutningsbeteende under inflammation.
Öppnar en ny behandlingsväg
Genom att visa att makrofag-deriverad PAI-1 blockerar rensning av döda celler kopplar denna studie en välkänd koagulationsregulator till inflammations oförmåga att stänga av sig själv. När PAI-1 tränger ut de normala ”ät mig”-signalerna vid makrofagreceptorer kvarstår skräpet och vävnadsreparationen dröjer. Ett läkemedel som hämmar PAI-1, givet oralt, återställde städningen och påskyndade muskelregeneration hos möss, vilket antyder ett praktiskt sätt att hjälpa vävnader återhämta sig efter skada. Eftersom dålig efferocytos och höga PAI-1-nivåer är vanliga inslag i många kroniska inflammatoriska och åldersrelaterade tillstånd, kan mål mot denna väg en dag erbjuda en ny klass antiinflammatoriska terapier som inte bara dämpar immunsvaret utan hjälper kroppen att slutföra läkningsarbetet.
Citering: Ibrahim, A.A., Miura, H., Terada, T. et al. Inflammatory macrophage-derived plasminogen activator inhibitor-1 exacerbates inflammation through efferocytosis inhibition. Cell Death Discov. 12, 195 (2026). https://doi.org/10.1038/s41420-026-03076-0
Nyckelord: inflammation, makrofager, muskulär reparation, cellsanering, PAI-1-hämmare