Clear Sky Science · fr
L’inhibiteur de l’activateur du plasminogène 1 dérivé des macrophages inflammatoires aggrave l’inflammation en inhibant l’efférocytose
Quand les équipes de nettoyage se trompent
Notre organisme dépend d’« équipes de nettoyage » immunitaires pour éliminer les cellules mortes et endommagées après une blessure. Cette étude montre comment une petite protéine, appelée PAI‑1, peut transformer ces cellules utiles en agents qui entretiennent une inflammation persistante. En bloquant l’évacuation sûre des débris cellulaires, le PAI‑1 empêche les tissus blessés de guérir correctement et les maintient dans un état de cicatrisation lente et d’irritation chronique — une découverte qui pourrait ouvrir de nouvelles voies pour traiter les lésions musculaires et d’autres maladies inflammatoires.
D’une inflammation utile à un gonflement nocif
L’inflammation est censée être temporaire. Lorsqu’un tissu est blessé, des cellules immunitaires affluent, retirent les débris, puis contribuent à reconstruire une structure saine. Un acteur clé de ce processus est le macrophage, une cellule polyvalente capable à la fois de déclencher et d’achever l’inflammation. Les macrophages « mangent » les cellules mourantes dans un processus appelé efférocytose, guidés par des signaux de surface qui indiquent quelles cellules doivent être éliminées et lesquelles doivent être préservées. Si cette phase de nettoyage échoue, les cellules mortes et leur contenu s’accumulent, inondant les tissus de signaux de danger qui peuvent alimenter une inflammation durable liée aux maladies cardiaques, au diabète, aux maladies auto-immunes, et même au cancer.
Regard rapproché sur une lésion musculaire
Pour comprendre le rôle du PAI‑1 dans cette histoire, les chercheurs ont utilisé un modèle murin bien établi de lésion du muscle squelettique. Une toxine a été injectée dans les muscles de la jambe pour provoquer des dégâts contrôlés suivis d’une réparation synchronisée. Peu après la blessure, une vague de macrophages inflammatoires portant les marqueurs CCR2 et Ly6C a envahi le muscle. Ces macrophages se sont révélés être des producteurs prolifiques de PAI‑1 directement sur le site de la lésion. Lorsque le gène codant le PAI‑1 a été supprimé chez les souris, ou lorsque l’activité du PAI‑1 a été bloquée par un petit médicament, les fibres musculaires endommagées ont été éliminées plus rapidement, les signaux inflammatoires ont diminué et l’architecture normale en nid d’abeille du muscle s’est rétablie plus vite. Ces effets positifs sont apparus même si d’autres sources de PAI‑1 dans l’organisme restaient présentes, ce qui suggère un effet local puissant.
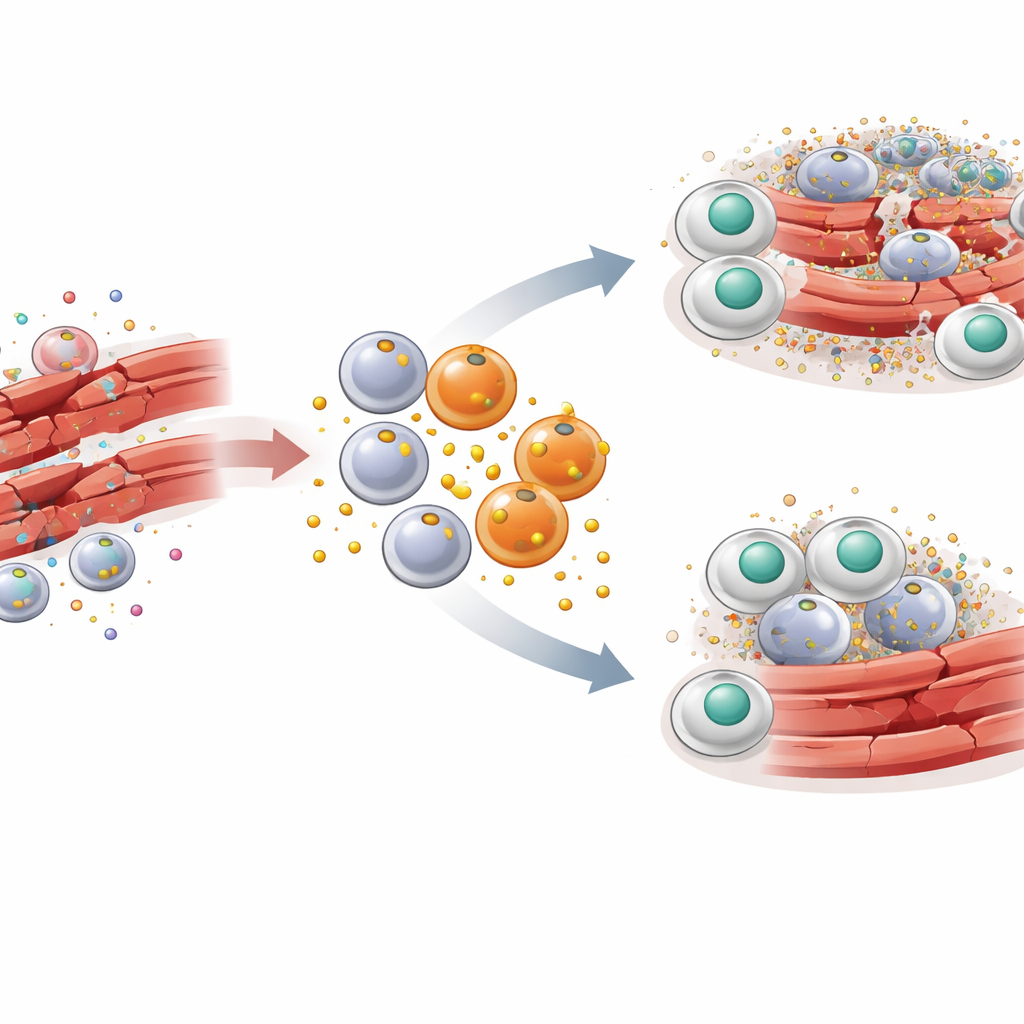
Comment un brouilleur de signaux bloque le nettoyage cellulaire
La découverte clé est que le PAI‑1 agit comme une sorte de brouilleur des signaux de l’efférocytose. Les cellules mourantes exposent une molécule appelée calréticuline à leur surface, qui sert de signal « mange‑moi ». Les macrophages portent un récepteur nommé LRP‑1 qui reconnaît la calréticuline et déclenche l’engloutissement de la cellule mourante. L’équipe a trouvé que le PAI‑1 se lie aussi à LRP‑1 — et avec une affinité supérieure à celle de la calréticuline. Dans des expériences en culture cellulaire, l’ajout de PAI‑1 réduisait la capacité des macrophages à ingérer des cellules mortes, tandis que l’élimination du PAI‑1 ou le blocage de sa liaison à LRP‑1 renforçait ce nettoyage. Une forme mutante du PAI‑1 incapable de se fixer à LRP‑1 n’a pas bloqué l’efférocytose, confirmant que l’interférence se produit à ce récepteur. En pratique, le PAI‑1 concurrence les signaux « mange‑moi », laissant les cellules mortes isolées et non éliminées.
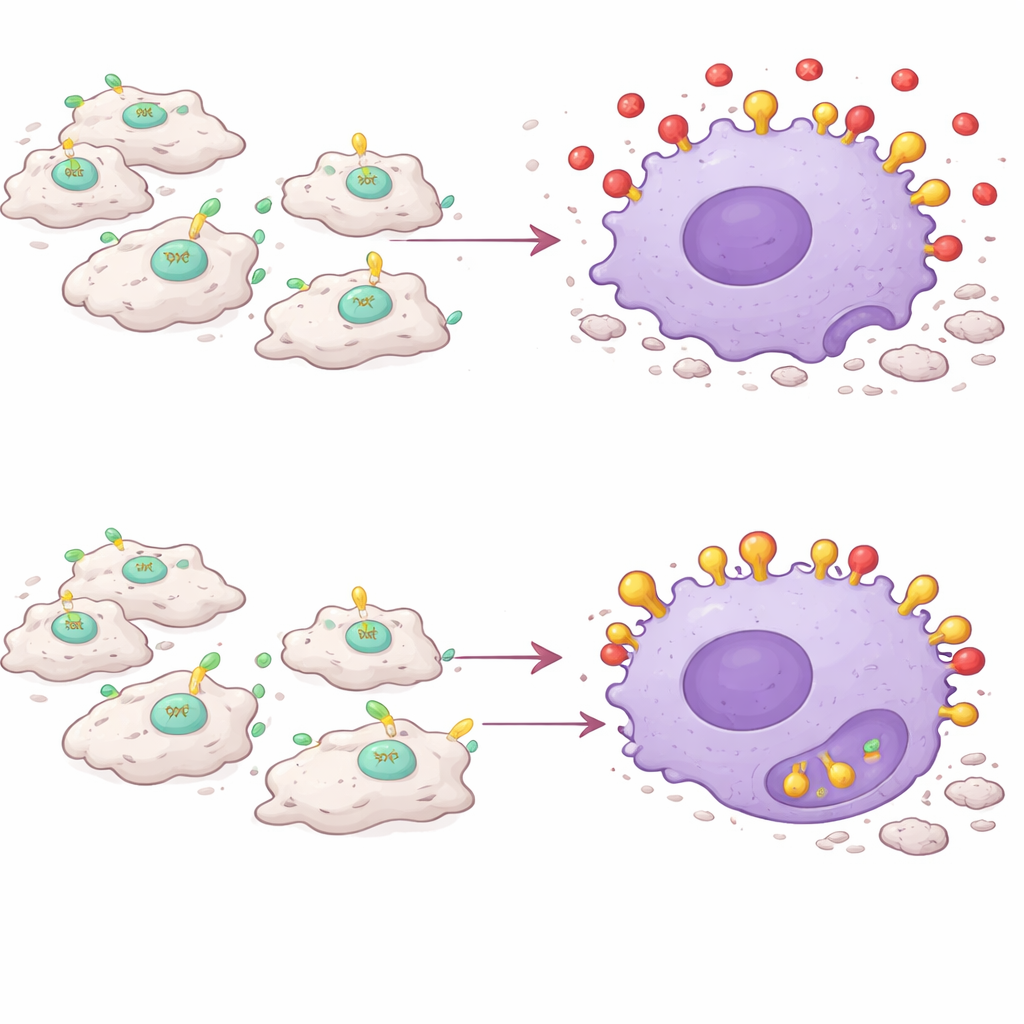
Les macrophages se retournent contre leur propre mission
Fait frappant, ce n’est pas n’importe quel PAI‑1 qui compte, mais le PAI‑1 produit par les macrophages inflammatoires eux‑mêmes. Lorsque les chercheurs ont supprimé sélectivement le gène PAI‑1 uniquement dans les macrophages CCR2+Ly6C+, les muscles blessés ont guéri de la même manière que chez les animaux avec suppression totale du PAI‑1 : moins de marquage des fibres endommagées, des niveaux plus faibles de messagers pro‑inflammatoires et davantage de cellules musculaires régénérées. La transplantation de macrophages inflammatoires riches en PAI‑1 dans des souris déficientes en PAI‑1 a suffi à rétablir une inflammation prolongée et un retard de cicatrisation, même si le reste de l’organisme manquait de PAI‑1. In vivo, tant la suppression génétique que l’inhibition pharmacologique du PAI‑1 ont augmenté la prise par les macrophages de particules traceuses, indiquant un comportement d’engloutissement plus actif pendant l’inflammation.
Ouvrir une nouvelle voie thérapeutique
En montrant que le PAI‑1 d’origine macrophagique bloque l’élimination des cellules mortes, cette étude relie un régulateur de la coagulation bien connu à l’incapacité de l’inflammation à s’éteindre. Lorsque le PAI‑1 éclipse les signaux « mange‑moi » normaux aux récepteurs des macrophages, les débris persistent et la réparation tissulaire stagne. Un médicament inhibiteur du PAI‑1, administré par voie orale, a rétabli le nettoyage et accéléré la régénération musculaire chez la souris, suggérant une voie pratique pour aider les tissus à récupérer après une blessure. Parce que la mauvaise efférocytose et des niveaux élevés de PAI‑1 sont des caractéristiques communes à de nombreuses affections inflammatoires chroniques et liées à l’âge, cibler cette voie pourrait un jour offrir une nouvelle classe de thérapies anti‑inflammatoires qui n’agissent pas en supprimant simplement les réponses immunitaires, mais en aidant l’organisme à mener à bien le processus de guérison.
Citation: Ibrahim, A.A., Miura, H., Terada, T. et al. Inflammatory macrophage-derived plasminogen activator inhibitor-1 exacerbates inflammation through efferocytosis inhibition. Cell Death Discov. 12, 195 (2026). https://doi.org/10.1038/s41420-026-03076-0
Mots-clés: inflammation, macrophages, réparation musculaire, élimination cellulaire, inhibiteur de PAI‑1