Clear Sky Science · nl
Ontstekingsbevorderende door macrofagen geproduceerde plasminogeenactivatorremmer-1 verergert ontsteking door remming van efferocytose
Wanneer de opruimploegen het fout doen
Ons lichaam vertrouwt op immuunsysteem–“opruimploegen” om dode en beschadigde cellen na een verwonding te verwijderen. Deze studie laat zien hoe één klein eiwit, PAI-1 genoemd, die nuttige opruimploegen kan veranderen in aanjagers van aanhoudende ontsteking. Door de veilige verwijdering van celresten te blokkeren, houdt PAI-1 beschadigd weefsel gevangen in een toestand van traag herstel en chronische irritatie — een inzicht dat nieuwe behandelrichtingen voor spierbeschadiging en andere ontstekingsziekten zou kunnen openen.
Van nuttige ontsteking naar schadelijke zwelling
Ontsteking is bedoeld als een tijdelijke reactie. Wanneer weefsel beschadigd raakt, haasten immuuncellen zich naar de plek, ruimen puin op en helpen vervolgens de gezonde structuur te herstellen. Een sleutelspeler in dit proces is de macrofaag, een veelzijdige cel die zowel ontsteking kan opwekken als helpen beëindigen. Macrofagen “eten” stervende cellen in een proces dat efferocytose heet, geleid door signalen op het celoppervlak die aangeven welke cellen verwijderd moeten worden en welke met rust gelaten moeten worden. Als deze opruimstap faalt, hopen dode cellen en hun inhoud zich op en dompelen ze weefsels onder in alarmsignalen die langdurige ontsteking kunnen aanwakkeren — gekoppeld aan hartziekten, diabetes, auto-immuunziekten en zelfs kanker.
Een nadere blik op spierletsel
Om te begrijpen hoe PAI-1 in dit verhaal past, gebruikten de onderzoekers een goed gecontroleerd muismodel voor skeletspierletsel. Een toxine werd in de beenspieren geïnjecteerd om gecontroleerde schade te veroorzaken gevolgd door synchroon herstel. Vroeg na de verwonding overspoelde een golf van inflammatoire macrofagen, met de merkers CCR2 en Ly6C, de spier. Deze specifieke macrofagen bleken op die plaats veel PAI-1 te produceren. Wanneer het PAI-1-gen bij muizen werd uitgeschakeld, of wanneer de activiteit van PAI-1 werd geblokkeerd met een klein-molecuulmedicijn, werden beschadigde spiervezels sneller opgeruimd, daalden ontstekingssignalen en werd de normale honingraatachtige architectuur van de spier sneller hersteld. Deze voordelen traden op ondanks dat andere bronnen van PAI-1 in het lichaam nog aanwezig waren, wat wijst op een sterk lokaal effect.
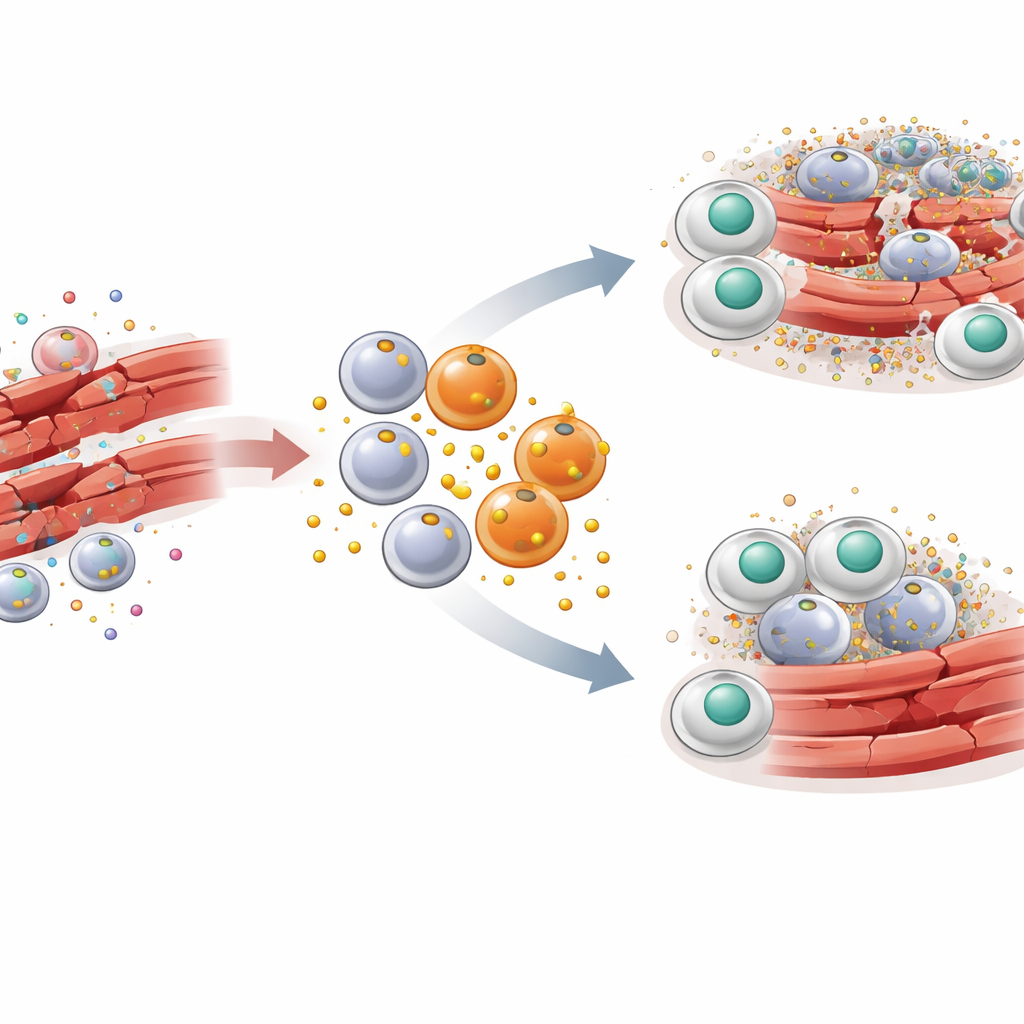
Hoe een signaalstoorzender de cellulaire opruiming blokkeert
De belangrijkste ontdekking is dat PAI-1 werkt als een soort signaalstoorzender voor efferocytose. Stervende cellen tonen een molecuul genaamd calreticuline op hun oppervlak, dat fungeert als een "eet mij"-vlag. Macrofagen dragen een receptor genaamd LRP-1 die calreticuline herkent en de opname van de stervende cel in gang zet. Het team ontdekte dat PAI-1 ook aan LRP-1 bindt — en dat met een hogere affiniteit dan calreticuline. In kweekexperimenten verminderde het toevoegen van PAI-1 het vermogen van macrofagen om dode cellen te verteren, terwijl het verwijderen van PAI-1 of het blokkeren van zijn binding aan LRP-1 deze opruiming verbeterde. Een gemuteerde vorm van PAI-1 die niet langer aan LRP-1 kon hechten, faalde in het blokkeren van efferocytose, wat bevestigt dat de interferentie bij deze receptor plaatsvindt. PAI-1 concurreert in feite de "eet mij"-signalen uit, waardoor dode cellen achterblijven en niet worden opgeruimd.
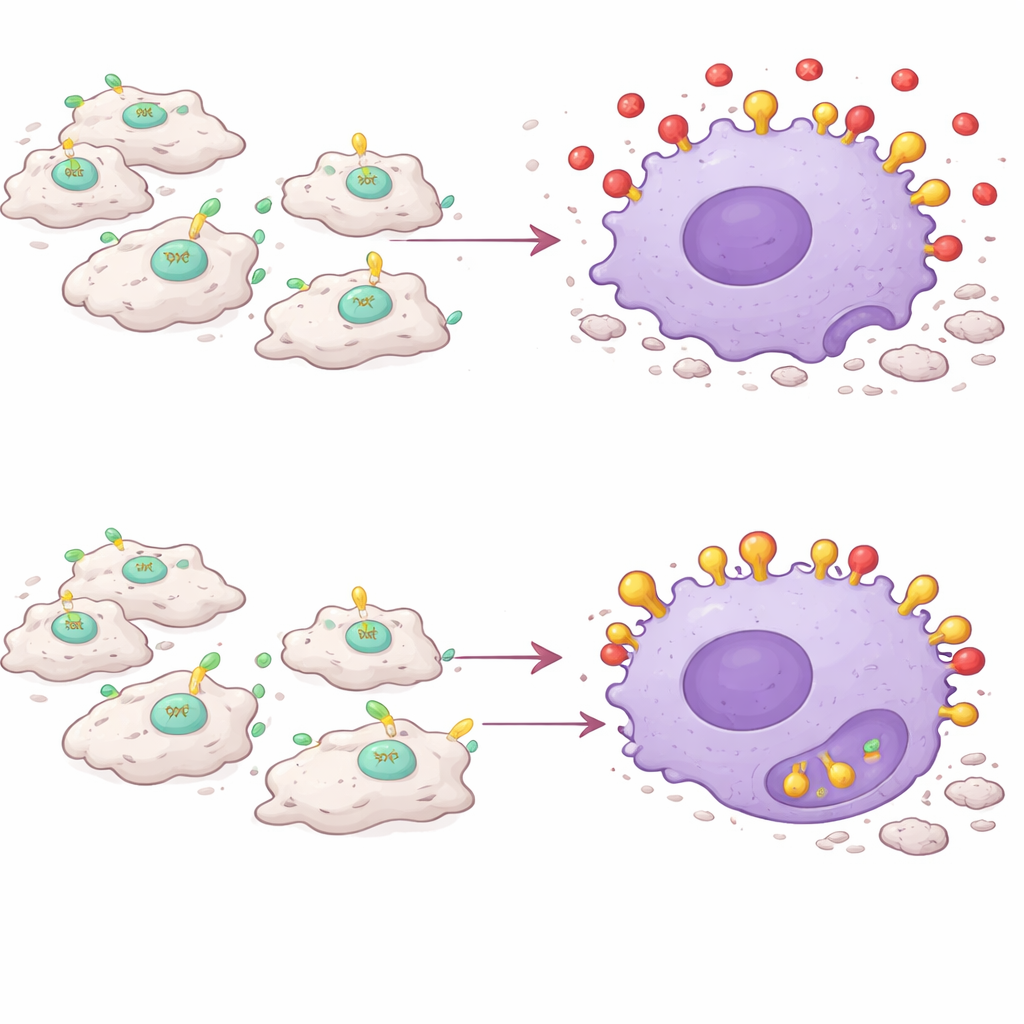
Macrofagen keren zich tegen hun eigen taak
Opmerkelijk is dat het niet zomaar elk PAI-1 is dat ertoe doet, maar specifiek het PAI-1 dat door inflammatoire macrofagen zelf wordt geproduceerd. Toen de onderzoekers het PAI-1-gen selectief verwijderden alleen in CCR2+Ly6C+ macrofagen, genazen beschadigde spieren op vergelijkbare wijze als bij volledige PAI-1-knockoutdieren: minder kleuring van beschadigde vezels, lagere niveaus van pro-inflammatoire boodschappers en meer geregenereerde spiercellen. Het transplanteren van PAI-1-rijke inflammatoire macrofagen in PAI-1-deficiënte muizen was voldoende om langdurige ontsteking en vertraagd herstel te herstellen, ook al miste de rest van het lichaam PAI-1. In levende dieren verhoogden zowel genetische verwijdering als medicinale remming van PAI-1 de opname van tracerdeeltjes door macrofagen, wat duidt op een actiever inslikgedrag tijdens ontsteking.
Een nieuwe weg voor behandeling openen
Door aan te tonen dat door macrofagen geproduceerd PAI-1 de opruiming van dode cellen blokkeert, koppelt deze studie een bekende stollingsregelaar aan het falen van ontsteking om zichzelf uit te schakelen. Wanneer PAI-1 de normale "eet mij"-signalen bij macrofaagreceptoren verdringt, blijven resten liggen en stokt weefselherstel. Een oraal toegediend medicijn dat PAI-1 remt, herstelde de opruiming en versnelde spierregeneratie bij muizen, wat wijst op een praktische manier om weefsels te helpen herstellen na letsel. Omdat slechte efferocytose en hoge PAI-1-niveaus veelvoorkomende kenmerken zijn van vele chronische ontstekings- en leeftijdsgebonden aandoeningen, kan het gericht aanpakken van deze route mogelijk op termijn een nieuwe klasse anti-inflammatoire therapieën opleveren die niet simpelweg het immuunsysteem dempen, maar het lichaam helpen de genezing daadwerkelijk af te ronden.
Bronvermelding: Ibrahim, A.A., Miura, H., Terada, T. et al. Inflammatory macrophage-derived plasminogen activator inhibitor-1 exacerbates inflammation through efferocytosis inhibition. Cell Death Discov. 12, 195 (2026). https://doi.org/10.1038/s41420-026-03076-0
Trefwoorden: ontsteking, macrofagen, spierherstel, celopruiming, PAI-1 remmer