Clear Sky Science · zh
一种诱导PAAoptosis的ERRα靶向新化合物,用于对抗血液与实体肿瘤
这项新癌症研究的重要性
抗癌药通常试图关闭肿瘤细胞的单一弱点,但癌细胞常常适应并产生耐药性。本研究描述了一种新的实验性药物,称为PAMT‑001,它以截然不同的方式攻击癌细胞:通过压垮它们的能量工厂并同时触发多种细胞死亡机制。该工作提出了一种针对血液癌和实体肿瘤(包括对标准化疗反应减弱的类型)的新策略。
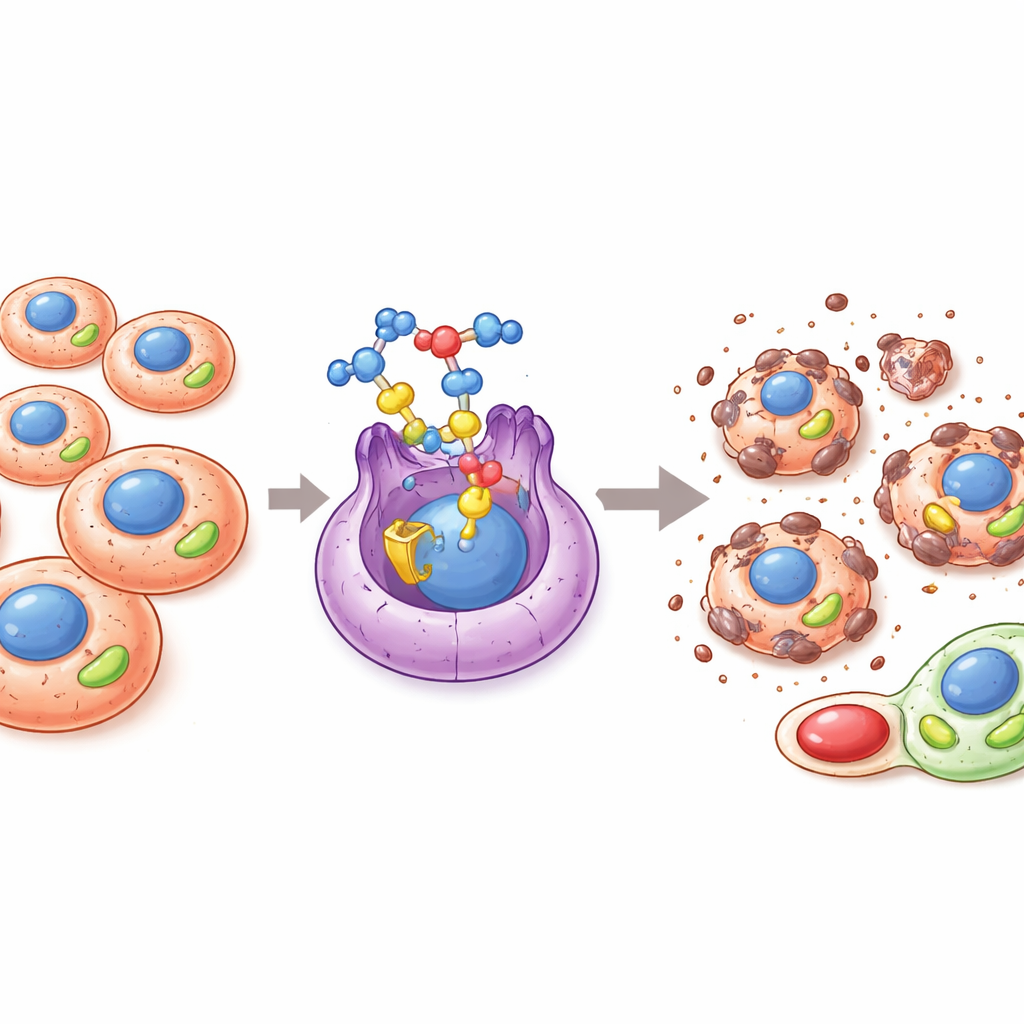
推动癌症生长的隐秘开关
许多癌症通过重编程能量的生成与利用来促进生长、扩散并抵抗治疗。一个关键参与者是被称为ERRα的蛋白质,它是细胞核内的一种分子开关,控制参与线粒体能量产生和氧化还原平衡的基因。当ERRα过度活跃时,肿瘤可以提升线粒体产能、清除有害的氧化副产物、维持类干细胞样的癌细胞并更好地在低氧或药物暴露等恶劣环境中存活。因此,ERRα已成为切断肿瘤能量优势的新型疗法的有吸引力靶点。
设计更聪明的癌症抑制剂
研究人员从一种较早的ERRα抑制分子XCT‑790出发,化学改造并构建了一系列相关化合物。在十二个候选物中,PAMT‑001成为最强效的致癌细胞剂,尽管在体外结合测试中它对ERRα的亲和力实际上比XCT‑790略低。计算机建模和报告基因检测显示,PAMT‑001能够嵌入ERRα中与共激活因子PGC1α相互作用的相同区域,而PGC1α可增强ERRα对线粒体基因的调控。通过干扰这种相互作用,PAMT‑001更有效地关闭由ERRα驱动的代谢程序,特别是在依赖该轴生存的细胞中。
切断细胞的动力工厂
PAMT‑001进入白血病和实体瘤细胞后,强烈扰乱线粒体功能。基因表达分析显示氧化磷酸化相关基因被广泛抑制,实时测量的氧气消耗显示基础与最大呼吸以及ATP生成显著下降。显微镜下,处理后的线粒体出现肿胀、形态异常,参与能量反应的内褶(嵴)变宽或丢失。这些损伤导致活性氧(ROS)过量产生,活性氧是具有化学活性的分子,会损伤线粒体及相邻的内质网(细胞的蛋白折叠中心)。抗氧化剂能部分挽救细胞存活,证实氧化爆发是该药物效应的关键驱动因素。
三条死亡路线而非一条
PAMT‑001并不依赖单一致死开关,而是并行激活若干受控的死亡程序。它触发经典的内源性凋亡:线粒体释放细胞色素c,执行酶(半胱天冬酶)被切割并激活,细胞膜出现典型的隆起;泛半胱天冬酶抑制剂能显著减弱该效应。同时,该药诱导强烈自噬,双膜囊泡形成并吞噬受损线粒体及其他细胞成分。用自噬抑制剂或敲除关键自噬基因阻断此过程会减少细胞死亡并降低应激信号,表明在此情境下自噬被过度激活且有害而非保护性。最后,PAMT‑001驱动一种剧烈的细胞死亡形式——焦亡:细胞膜出现孔洞,细胞内容物外泄,名为gasdermin E的蛋白被切割生成形成孔洞的片段。焦亡、凋亡与自噬性细胞死亡共同构成作者所称的“PAAoptosis”,即癌细胞的协调性多途径崩溃。

对难治性癌症的希望
PAMT‑001不仅在细胞培养中有效。在结肠癌和急性髓性白血病的小鼠模型中,该药减缓了肿瘤生长,降低了骨髓中的白血病细胞,并通过影像学显示总体癌症负担下降,同时对体重或正常细胞没有明显伤害。来自急性髓性白血病患者的样本普遍比健康血细胞更易受PAMT‑001影响,携带NPM1基因突变的白血病——常与高线粒体活性相关——尤为易感。该药还能杀死对阿糖胞苷耐药的白血病细胞和对EGFR靶向药耐药的肺癌细胞,提示其对线粒体代谢的广泛攻击和多途径诱导细胞死亡或有助于克服治疗耐药。
对未来癌症治疗的意义
这项工作将PAMT‑001引入视为一种原型药物——通过靶向能量调控开关并迫使肿瘤进入PAAoptosis(一种结合三种破坏性死亡程序的状态)。通过破坏能量供应并同时压迫多条关键系统,此类药物或能减少癌细胞进化出耐药性的空间。尽管PAMT‑001本身仍需在安全性、剂量与长期效应方面进行更多测试,该研究指向了利用癌细胞独特能量需求并以多路径细胞死亡来阻止顽固肿瘤反弹的治疗方向。
引用: Seo, W., Heo, Y., Tran, K.V. et al. A novel PAAoptosis-inducing ERRα-targeting compound for combating hematopoietic and solid cancers. Cell Death Discov. 12, 188 (2026). https://doi.org/10.1038/s41420-026-03010-4
关键词: 癌症代谢, 线粒体, ERRα, 耐药, 细胞死亡途径