Clear Sky Science · ar
مركب جديد يستهدف ERRα ويحفز موت PAAptosis لمكافحة السرطانات الدموية والصلبة
لماذا تهم هذه الدراسة الجديدة حول السرطان
تميل أدوية السرطان عادةً إلى استهداف نقطة ضعف واحدة في خلايا الورم، لكن السرطانات غالبًا ما تتكيف وتصبح مقاومة. تصف هذه الدراسة دواءً تجريبيًا جديدًا يُدعى PAMT‑001، يهاجم الخلايا السرطانية بطريقة مختلفة جذريًا: عن طريق إغراق مصانع الطاقة لديها وتحفيز عدة أنواع من موت الخلية في آن واحد. تشير النتائج إلى استراتيجية جديدة لمواجهة كل من سرطانات الدم والأورام الصلبة، بما في ذلك الأشكال التي لم تعد تستجيب جيدًا للعلاج الكيميائي التقليدي.
مفتاح مخفي يغذي نمو السرطان
تعيد العديد من السرطانات برمجة كيفية إنتاجها للطاقة واستخدامها لتتمكن من النمو والانتشار ومقاومة العلاج. أحد اللاعبين الرئيسيين في هذا التحول الأيضي هو بروتين يعرف باسم ERRα، وهو نوع من المفاتيح الجزيئية داخل نواة الخلية يتحكم في جينات مرتبطة بإنتاج الطاقة في الميتوكوندريا وتوازن الأكسدة والاختزال. عندما يكون ERRα مفرط النشاط، يمكن للأورام تعزيز إنتاج الميتوكوندريا للطاقة، والتخلص من نفايات الأكسجين الضارة، والحفاظ على خلايا شبيهة بالجذور داخل الورم، والنجاة بشكل أفضل في ظروف قاسية مثل نقص الأكسجين أو التعرض للأدوية. لهذا السبب، حظي ERRα باهتمام كهدف واعد لعلاجات جديدة تهدف إلى قطع ميزات الطاقة لدى الورم.
تصميم مثبط ذك smarter للسرطان
انطلق الباحثون من جزيء قديم يثبط ERRα يسمى XCT‑790، وأعادوا تصميمه كيميائيًا لإنشاء عائلة من المركبات ذات الصلة. من بين اثني عشر مرشحًا، برز PAMT‑001 كالأقوى في قتل الخلايا السرطانية، رغم أنه في الاختبارات المخبرية يربط ERRα بقوة أقل قليلًا من XCT‑790. أظهرت نمذجة حاسوبية وتجارب مراسل أن PAMT‑001 يمكنه الالتصاق بنفس منطقة ERRα التي تتفاعل عادةً مع بروتين منشط مشارك يُدعى PGC1α، والذي يعزز بشدة سيطرة ERRα على جينات الميتوكوندريا. من خلال التدخل في هذه الشراكة، يغلق PAMT‑001 برامج الأيض المدفوعة بـ ERRα بشكل أكثر فاعلية، لا سيما في الخلايا التي تعتمد اعتمادًا كبيرًا على هذا المحور للبقاء.
جوع مصانع طاقة الخلية
بمجرد دخولها خلايا اللوكيميا والأورام الصلبة، يعيق PAMT‑001 وظائف الميتوكوندريا بشدة. كشفت تحليلات التعبير الجيني عن كبح واسع لجينات الفسفرة التأكسدية، وأظهرت قياسات استهلاك الأكسجين الحية انخفاضًا ملحوظًا في التنفس الأساسي والذروي وكذلك إنتاج ATP. تحت المجهر، بدت الميتوكوندريا في الخلايا المعالجة متضخمة ومشوهة، مع طيات داخلية (الطيات الكرستالية) متسعة أو مفقودة، حيث تحدث تفاعلات توليد الطاقة. يؤدي هذا التلف إلى إنتاج زائد لأنواع الأكسجين التفاعلية، وهي جزيئات كيميائية عدوانية تضغط على كل من الميتوكوندريا والشبكة البطانية (الشبكة الإندوبلازمية) المجاورة، مركز طي البروتينات في الخلية. أنقذت مضادات الأكسدة البقاء الجزئي للخلايا، مؤكدة أن هذا التفجر التأكسدي هو محرك رئيسي لتأثيرات الدواء.
ثلاثة مسارات موت بدلاً من واحد
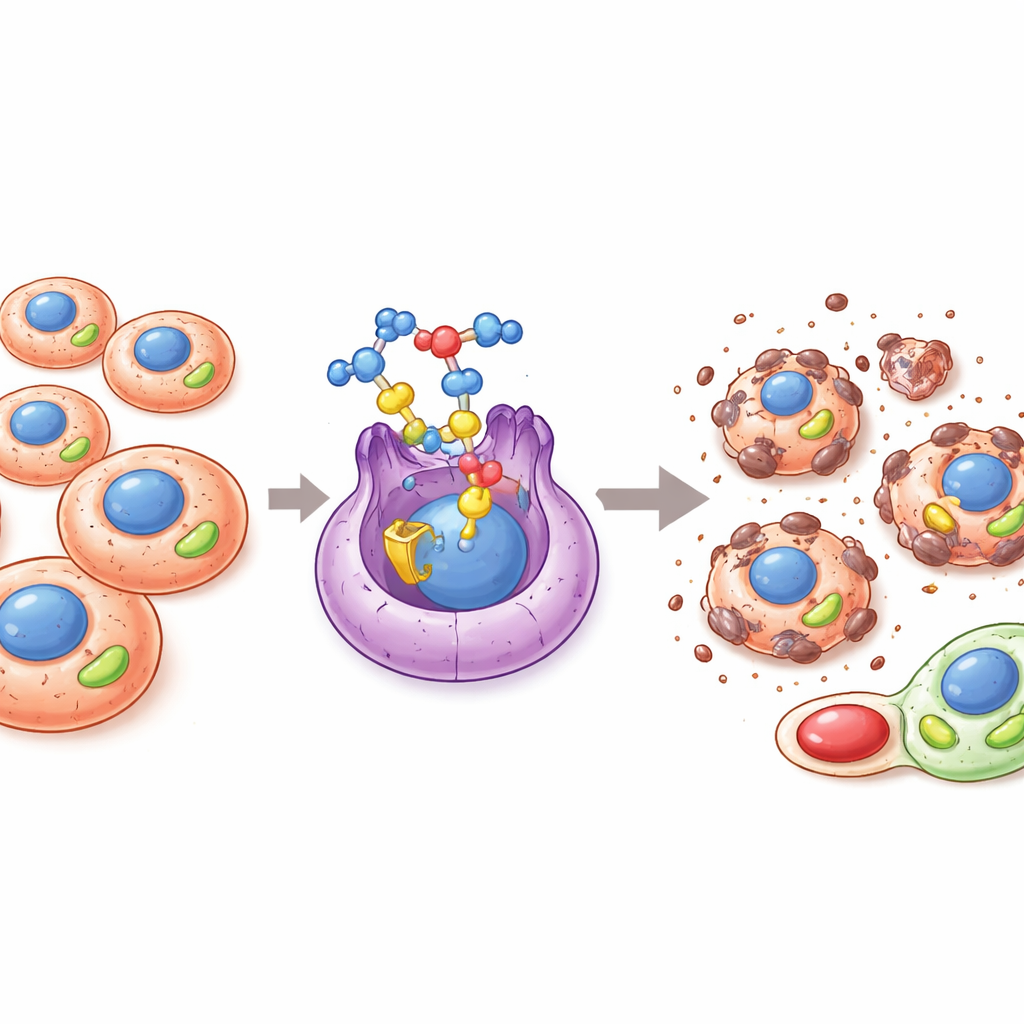
بدلاً من الاعتماد على مفتاح قتل واحد، ينشط PAMT‑001 عدة برامج موت منظمة بالتوازي. يحفز مسار الموت المبرمج الداخلي التقليدي: تطلق الميتوكوندريا السيتوكروم c، وتُقص وتُفعل إنزيمات التنفيذ المسماة الكاسبازات، وتظهر أغشية الخلايا نتوءات مميزة؛ وتقلل مثبطات الكاسباز الشاملة هذا التأثير بشكل كبير. وفي الوقت نفسه، يثير الدواء تحللًا ذاتيًا قويًا (autophagy)، حيث تتشكل أكياس مزدوجة الغشاء وتبتلع الميتوكوندريات التالفة ومحتويات أخرى من الخلية. يؤدي حجب هذه العملية بمثبطات التحلل الذاتي أو تعطيل جين رئيسي فيها إلى تقليل موت الخلايا وخفض إشارات الإجهاد، مما يشير إلى أن التحلل الذاتي في هذا السياق يصبح مفرطًا وضارًا بدلًا من أن يكون وقائيًا. أخيرًا، يدفع PAMT‑001 نوعًا متفجرًا من الموت يسمى البيروبτοςيس (pyroptosis): تفتح مسام في غشاء الخلية، وتتسرب المحتويات، ويُقص بروتين يُدعى غاسدرمين E إلى شظية قادرة على تكوين مسام. معًا، تتحد البيروبتوسيس والابوبتوسيس والموت الخلوي المرتبط بالتحلل الذاتي لتشكل ما يسميه المؤلفون «PAAoptosis»، انهيارًا منسقًا ومتعدد المسارات للخلية السرطانية.

أمل في مواجهة السرطانات صعبة المعالجة
لم يعمل PAMT‑001 فقط في الأطباق المخبرية. في نماذج الفئران لسرطان القولون واللوكيميا النخاعية الحادة، أبطأ الدواء نمو الأورام، وخفض خلايا اللوكيميا في نقي العظام، وقلل العبء السرطاني الكلي كما قاسته التصويرات، وكل ذلك دون أذى واضح لوزن الجسم أو للخلايا الطبيعية. كانت عينات من مرضى اللوكيميا النخاعية الحادة أكثر حساسية عمومًا تجاه PAMT‑001 مقارنة بخلايا الدم السليمة، وكانت اللوكيميات التي تحمل طفرات في الجين المسمى NPM1—المرتبطة غالبًا بارتفاع نشاط الميتوكوندريا—عرضة بشكل خاص. كما قتل الدواء خلايا اللوكيميا المقاومة للسيتارابين وخلايا سرطان الرئة المقاومة لعقار يستهدف EGFR، مما يوحي بأن هجومه الواسع على استقلاب الميتوكوندريا وموت الخلايا متعدد المسارات قد يساعد على التغلب على مقاومة العلاج.
ماذا يعني هذا لرعاية السرطان في المستقبل
تقدم هذه الدراسة PAMT‑001 كنموذج أولي لنوع جديد من أدوية السرطان يستهدف مفتاح التحكم بالطاقة ويجبر الأورام على الدخول في حالة PAAoptosis، مزيج من ثلاثة برامج موت مدمرة. من خلال تقويض مصدر الطاقة وإجهاد عدة أنظمة حيوية في آن واحد، قد تترك هذه الأدوية للخلايا السرطانية مجالًا أقل لتطوير المقاومة. وعلى الرغم من أن PAMT‑001 نفسه سيحتاج إلى مزيد من الاختبارات المتعلقة بالسلامة والجرعات والتأثيرات طويلة الأمد، تشير الدراسة إلى مسارات علاجية تستغل المطالب الطاقية الفريدة للخلايا السرطانية وتستخدم موت الخلايا متعدد المسارات وسيلة لمنع الأورام العنيدة من الانتكاس.
الاستشهاد: Seo, W., Heo, Y., Tran, K.V. et al. A novel PAAoptosis-inducing ERRα-targeting compound for combating hematopoietic and solid cancers. Cell Death Discov. 12, 188 (2026). https://doi.org/10.1038/s41420-026-03010-4
الكلمات المفتاحية: استقلاب السرطان, الميتوكوندريا, ERR ألفا, مقاومة الأدوية, مسارات موت الخلية