Clear Sky Science · pl
Nowy związek wywołujący PAAoptozę ukierunkowany na ERRα w walce z nowotworami krwi i guzami litymi
Dlaczego to nowe badanie nad rakiem ma znaczenie
Leki przeciwnowotworowe zwykle próbują zablokować jedno słabe ogniwo w komórkach guza, ale nowotwory często adaptują się i stają się oporne. To badanie opisuje nowy eksperymentalny związek, nazwany PAMT‑001, który atakuje komórki nowotworowe w zupełnie inny sposób: przez przytłoczenie ich „elektrowni” i uruchomienie kilku rodzajów śmierci komórkowej jednocześnie. Praca sugeruje nową strategię zwalczania zarówno nowotworów krwi, jak i guzów litych, w tym postaci, które przestały dobrze reagować na standardową chemioterapię.
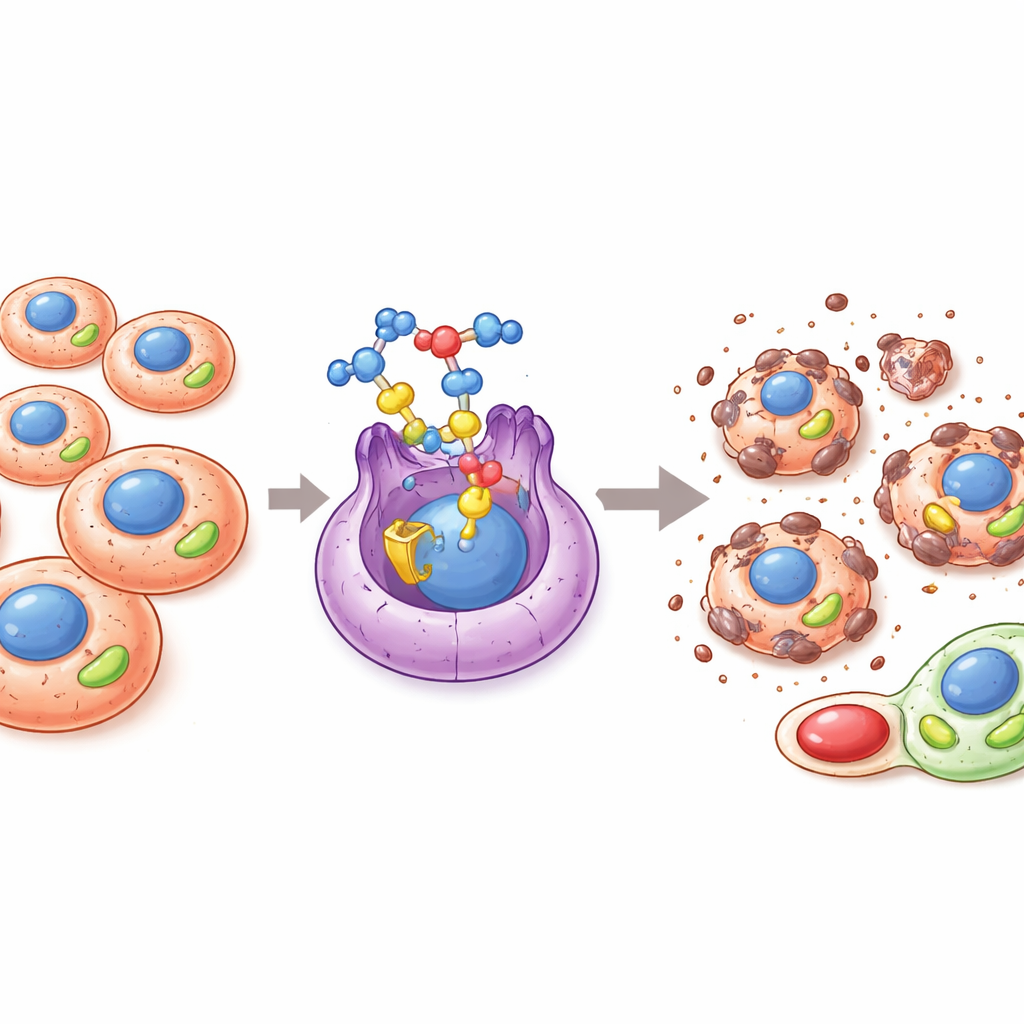
Ukryty przełącznik napędzający wzrost nowotworu
Wiele nowotworów przebudowuje sposób wytwarzania i wykorzystywania energii, aby rosnąć, przerzucać się i opierać leczeniu. Kluczowym graczem w tej metabolicznej reorganizacji jest białko znane jako ERRα, rodzaj molekularnego przełącznika w jądrze komórkowym, który kontroluje geny zaangażowane w produkcję energii w mitochondriach i równowagę redoks. Gdy ERRα jest nadmiernie aktywny, guzy mogą zwiększać wydajność mitochondriów, usuwać szkodliwe produkty tlenu, utrzymywać komórki o cechach podobnych do komórek macierzystych i lepiej przetrwać trudne warunki, takie jak niskie stężenie tlenu czy ekspozycja na leki. Z tego powodu ERRα zyskał zainteresowanie jako obiecujący cel nowych terapii przeciwnowotworowych, które mają odciąć energetyczne przewagi guza.
Projektowanie inteligentniejszego blokeru nowotworowego
Naukowcy zaczęli od starszej cząsteczki blokującej ERRα, XCT‑790, i chemicznie przeprojektowali ją, tworząc rodzinę powiązanych związków. Spośród dwunastu kandydatów najskuteczniejszy okazał się PAMT‑001 w zabijaniu komórek nowotworowych, choć w testach in vitro wiązał się z ERRα nieco słabiej niż XCT‑790. Modele komputerowe i testy reporterowe wykazały, że PAMT‑001 może wpasować się w ten sam obszar ERRα, który zwykle wchodzi w interakcję z koregulatorem PGC1α, wzmacniającym kontrolę ERRα nad genami mitochondrialnymi. Przeszkadzając tej współpracy, PAMT‑001 skuteczniej wyłącza programy metaboliczne napędzane przez ERRα, szczególnie w komórkach silnie zależnych od tej osi dla przetrwania.
Głodzenie elektrowni komórkowej
Po wejściu do komórek białaczki i guzów litych PAMT‑001 silnie zaburza funkcję mitochondriów. Analizy ekspresji genów ujawniły szeroką supresję genów związanych z fosforylacją oksydacyjną, a pomiary zużycia tlenu na żywo pokazały wyraźny spadek podstawowego i maksymalnego oddychania oraz produkcji ATP. W mikroskopie mitochondria w leczonych komórkach stały się spuchnięte i zdeformowane, z rozmytymi lub zanikającymi grzebieniami mitochondrialnymi — wewnętrznymi fałdami, w których zachodzą reakcje energetyczne. To uszkodzenie prowadzi do nadmiernej produkcji reaktywnych form tlenu, które są chemicznie agresywnymi cząsteczkami obciążającymi zarówno mitochondria, jak i sąsiadujący retikulum endoplazmatyczne, centrum fałdowania białek w komórce. Przeciwutleniacze częściowo ratowały przeżywalność komórek, potwierdzając, że to wybuchowe utlenianie jest kluczowym motorem działania leku.
Trzy drogi śmierci zamiast jednej
Zamiast opierać się na jednym przełączniku zabijającym, PAMT‑001 aktywuje równolegle kilka regulowanych programów śmierci. Wywołuje klasyczną apoptozę wewnętrzną: mitochondria uwalniają cytochrom c, enzymy egzekucyjne zwane kaspazami są cięte i aktywowane, a błony komórkowe wykazują charakterystyczne pęcherzykowanie; inhibitory pan‑kaspaz znacznie osłabiają ten efekt. Jednocześnie lek silnie indukuje autofagię, w której tworzą się podwójne błony pochłaniające uszkodzone mitochondria i inne składniki komórki. Zablokowanie tego procesu za pomocą inhibitorów autofagii lub wyłączenie kluczowego genu autofagii zmniejsza śmierć komórek i obniża sygnały stresowe, co wskazuje, że w tym kontekście autofagia staje się nadmiernie aktywna i szkodliwa, a nie ochronna. Wreszcie PAMT‑001 wywołuje zapalny rodzaj śmierci zwany pyroptozą: w błonie komórkowej otwierają się pory, zawartość wycieka, a białko gasdermin E jest cięte do fragmentu tworzącego pory. Razem pyroptoza, apoptoza i śmierć autofagiczna łączą się w to, co autorzy nazywają „PAAoptozą”, skoordynowanym, wieloszlakowym zapadnięciem się komórki nowotworowej.

Obietnica dla trudnych do leczenia nowotworów
PAMT‑001 nie działał tylko w hodowlach. W modelach mysim raka jelita grubego i ostrej białaczki szpikowej lek spowalniał wzrost guza, zmniejszał liczbę komórek białaczkowych w szpiku kostnym i obniżał ogólny ciężar nowotworu oceniany obrazowo, wszystko to bez oczywistych szkód dla masy ciała czy komórek normalnych. Próbki od pacjentów z ostrą białaczką szpikową były generalnie bardziej wrażliwe na PAMT‑001 niż zdrowe komórki krwi, a białaczki niosące mutacje w genie NPM1 — często związane z wysoką aktywnością mitochondrialną — były szczególnie podatne. Lek również zabijał komórki białaczki oporne na cytarabinę i komórki raka płuc oporne na lek ukierunkowany na EGFR, co sugeruje, że jego szerokie uderzenie w metabolizm mitochondrialny i wieloszlakowe indukowanie śmierci komórkowej może pomóc przełamać oporność na terapię.
Co to oznacza dla przyszłej opieki nad chorymi na raka
Ta praca przedstawia PAMT‑001 jako prototyp nowego rodzaju leku przeciwnowotworowego, który celuje w przełącznik kontrolujący energię i zmusza guzy do PAAoptozy — mieszaniny trzech destrukcyjnych programów śmierci. Podkopując źródło zasilania i jednocześnie obciążając kilka kluczowych systemów, takie leki mogą zostawić komórkom nowotworowym mniej przestrzeni do rozwoju oporności. Choć sam PAMT‑001 będzie wymagał dalszych badań nad bezpieczeństwem, dawkowaniem i długoterminowymi skutkami, badanie wskazuje na terapie wykorzystujące unikalne potrzeby energetyczne komórek nowotworowych i stosujące wielodrogowe wywoływanie śmierci komórkowej jako sposób na powstrzymanie uporczywych guzów przed odradzaniem się.
Cytowanie: Seo, W., Heo, Y., Tran, K.V. et al. A novel PAAoptosis-inducing ERRα-targeting compound for combating hematopoietic and solid cancers. Cell Death Discov. 12, 188 (2026). https://doi.org/10.1038/s41420-026-03010-4
Słowa kluczowe: metabolizm nowotworu, mitochondria, ERR alfa, oporność na leki, szlaki śmierci komórkowej