Clear Sky Science · pt
Um novo composto que induz PAAoptose e mira ERRα para combater cânceres hematopoiéticos e sólidos
Por que este novo estudo sobre câncer é importante
Medicamentos contra o câncer geralmente tentam fechar um único ponto fraco nas células tumorais, mas os cânceres frequentemente se adaptam e se tornam resistentes. Este estudo descreve um novo fármaco experimental, chamado PAMT‑001, que ataca as células cancerosas de maneira bem diferente: sobrecarregando suas fábricas de energia e acionando simultaneamente vários tipos de morte celular. O trabalho sugere uma estratégia nova para enfrentar tanto cânceres hematológicos quanto tumores sólidos, incluindo formas que já não respondem bem à quimioterapia padrão.
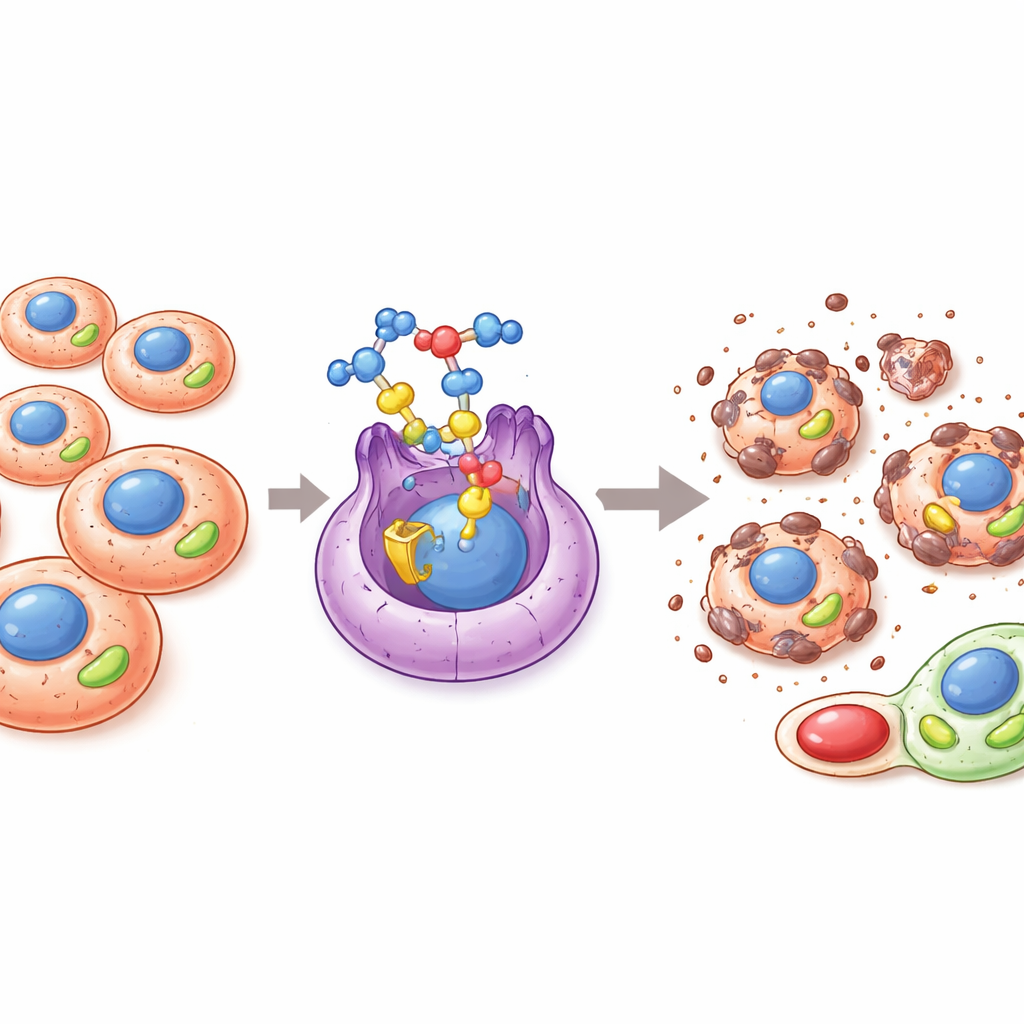
Um interruptor oculto que alimenta o crescimento do câncer
Muitos cânceres redesenham a forma como produzem e usam energia para crescer, se espalhar e resistir ao tratamento. Um ator-chave nessa reprogramação metabólica é uma proteína conhecida como ERRα, um tipo de interruptor molecular no núcleo celular que controla genes envolvidos na produção de energia mitocondrial e no balanço redox. Quando o ERRα está excessivamente ativo, os tumores podem aumentar sua produção mitocondrial, eliminar subprodutos oxidativos nocivos, manter células cancerosas com características de estirpe e sobreviver melhor a condições adversas como baixo oxigênio ou exposição a drogas. Por isso, o ERRα atraiu atenção como um alvo promissor para novas terapias que visam cortar as vantagens energéticas do tumor.
Desenhando um bloqueador cancerígeno mais inteligente
Os pesquisadores partiram de uma molécula bloqueadora de ERRα mais antiga, XCT‑790, e a redesenharam quimicamente para criar uma família de compostos relacionados. De doze candidatos, PAMT‑001 emergiu como o mais potente para matar células cancerosas, embora de fato se ligue ao ERRα um pouco menos fortemente que o XCT‑790 em testes de laboratório. Modelagem computacional e ensaios com repórteres mostraram que PAMT‑001 pode acomodar‑se na mesma região do ERRα que normalmente interage com uma proteína coativadora chamada PGC1α, que turboalimenta o controle do ERRα sobre genes mitocondriais. Ao interferir nessa parceria, PAMT‑001 interrompe de forma mais eficaz os programas metabólicos dirigidos por ERRα, especialmente em células que dependem fortemente desse eixo para sobreviver.
Privando as usinas de energia da célula
Uma vez dentro de células de leucemia e de tumores sólidos, PAMT‑001 perturba fortemente a função mitocondrial. Análises de expressão gênica revelaram ampla supressão de genes da fosforilação oxidativa, e medições ao vivo do consumo de oxigênio mostraram uma queda marcada na respiração basal e máxima, bem como na produção de ATP. Ao microscópio, as mitocôndrias em células tratadas tornaram‑se inchadas e deformadas, com cristas — dobras internas onde ocorrem reações energéticas — alargadas ou perdidas. Esse dano leva à produção excessiva de espécies reativas de oxigênio, moléculas quimicamente agressivas que sobrecarregam tanto as mitocôndrias quanto o retículo endoplasmático vizinho, o centro de dobramento de proteínas da célula. Antioxidantes resgataram parcialmente a sobrevivência celular, confirmando que esse estouro oxidativo é um motor chave dos efeitos do fármaco.
Três rotas de morte em vez de uma
Em vez de depender de um único botão de morte, PAMT‑001 ativa vários programas regulados de morte em paralelo. Ele desencadeia a apoptose intrínseca clássica: as mitocôndrias liberam citocromo c, enzimas executoras chamadas caspases são clivadas e ativadas, e as membranas celulares exibem o blebbing característico; inibidores pan‑caspase atenuam substancialmente esse efeito. Ao mesmo tempo, o fármaco induz forte autofagia, na qual sacos de dupla membrana se formam e englobam mitocôndrias danificadas e outros conteúdos celulares. Bloquear esse processo com inibidores de autofagia ou desativando um gene-chave de autofagia reduz a morte celular e diminui os sinais de estresse, indicando que, nesse contexto, a autofagia fica hiperativada e prejudicial em vez de protetora. Finalmente, PAMT‑001 promove uma forma inflamável de morte chamada piroptose: poros se abrem na membrana celular, conteúdos vazam, e uma proteína chamada gasdermina E é clivada em um fragmento formador de poros. Juntas, piroptose, apoptose e morte por autofagia combinam‑se no que os autores chamam de “PAAoptose”, um colapso coordenado de múltiplas vias de morte da célula cancerosa.

Promessa para cânceres difíceis de tratar
PAMT‑001 não funcionou apenas em placas de cultura. Em modelos murinos de câncer de cólon e leucemia mieloide aguda, o fármaco retardou o crescimento tumoral, reduziu células leucêmicas na medula óssea e diminuiu a carga geral de câncer medida por imagem, tudo sem dano aparente ao peso corporal ou às células normais. Amostras de pacientes com leucemia mieloide aguda foram geralmente mais sensíveis ao PAMT‑001 do que células sanguíneas saudáveis, e leucemias com mutações no gene NPM1 — frequentemente associadas a alta atividade mitocondrial — foram especialmente vulneráveis. O fármaco também matou células leucêmicas resistentes à citarabina e células de câncer de pulmão resistentes a uma droga direcionada ao EGFR, sugerindo que seu ataque amplo ao metabolismo mitocondrial e à morte celular por múltiplas vias pode ajudar a superar resistência ao tratamento.
O que isso significa para o cuidado futuro do câncer
Este trabalho apresenta o PAMT‑001 como um protótipo de um novo tipo de fármaco anticâncer que mira um interruptor que controla a energia e força os tumores a entrarem em PAAoptose, uma mistura de três programas destrutivos de morte. Ao minar a fonte de energia e estressar vários sistemas vitais ao mesmo tempo, tais fármacos podem deixar menos espaço para que as células cancerosas evoluam resistência. Embora o próprio PAMT‑001 precise de mais testes sobre segurança, dosagem e efeitos a longo prazo, o estudo aponta para terapias que exploram as demandas energéticas únicas das células cancerosas e usam a morte celular por múltiplas rotas como forma de impedir que tumores persistentes voltem a crescer.
Citação: Seo, W., Heo, Y., Tran, K.V. et al. A novel PAAoptosis-inducing ERRα-targeting compound for combating hematopoietic and solid cancers. Cell Death Discov. 12, 188 (2026). https://doi.org/10.1038/s41420-026-03010-4
Palavras-chave: metabolismo do câncer, mitocôndrias, ERR alfa, resistência a medicamentos, vias de morte celular