Clear Sky Science · nl
Een nieuw PAAoptose-inducerend compound dat ERRα-targeting toepast voor de bestrijding van hematologische en solide kankers
Waarom deze nieuwe kankerstudie ertoe doet
Kankergeneesmiddelen richten zich meestal op één zwakke plek in tumorcellen, maar tumoren passen zich vaak aan en worden resistent. Deze studie beschrijft een nieuw experimenteel middel, PAMT‑001 genoemd, dat kankercellen op een heel andere manier aanvalt: het overweldigt hun energiefabrieken en activeert tegelijk meerdere vormen van celdood. Het werk suggereert een frisse strategie voor de aanpak van zowel bloedkankers als solide tumoren, inclusief vormen die niet langer goed reageren op standaardchemotherapie.
Een verborgen schakel die kankergroei voedt
Veel kankers herprogrammeren hun energieproductie en -gebruik om te groeien, uit te zaaien en behandeling te weerstaan. Een belangrijke speler in deze metabole herinrichting is een eiwit dat bekendstaat als ERRα, een soort moleculaire schakel in de celkern die genen regelt die betrokken zijn bij mitochondriale energieproductie en redox‑balans. Wanneer ERRα overactief is, kunnen tumoren hun mitochondriale output verhogen, schadelijke zuurstofbijproducten wegvangen, stamcelachtige kankercellen in stand houden en beter overleven onder zware omstandigheden zoals lage zuurstof of medicijnblootstelling. Daarom is ERRα als doelwit voor nieuwe kankertherapieën die de energievoordelen van de tumor willen afknijpen, in het vizier gekomen.
Het ontwerpen van een slimmer kankermiddel
De onderzoekers begonnen met een ouder ERRα‑blokkerend molecuul, XCT‑790, en herontwi er pen het chemisch om een familie verwante verbindingen te creëren. Van twaalf kandidaten bleek PAMT‑001 het meest krachtig in het doden van kankercellen, zelfs al bindt het in labtests iets minder sterk aan ERRα dan XCT‑790. Computermodellering en reporterassays toonden aan dat PAMT‑001 zich kan nestelen in hetzelfde gebied van ERRα dat normaal gesproken interacteert met een co‑activator‑eiwit genaamd PGC1α, dat ERRα’s controle over mitochondriale genen versterkt. Door deze samenwerking te verstoren, schakelt PAMT‑001 ERRα‑gedreven metabole programma’s effectiever uit, vooral in cellen die sterk afhankelijk zijn van deze as voor hun overleving.
De energiecentrales van de cel uithongeren
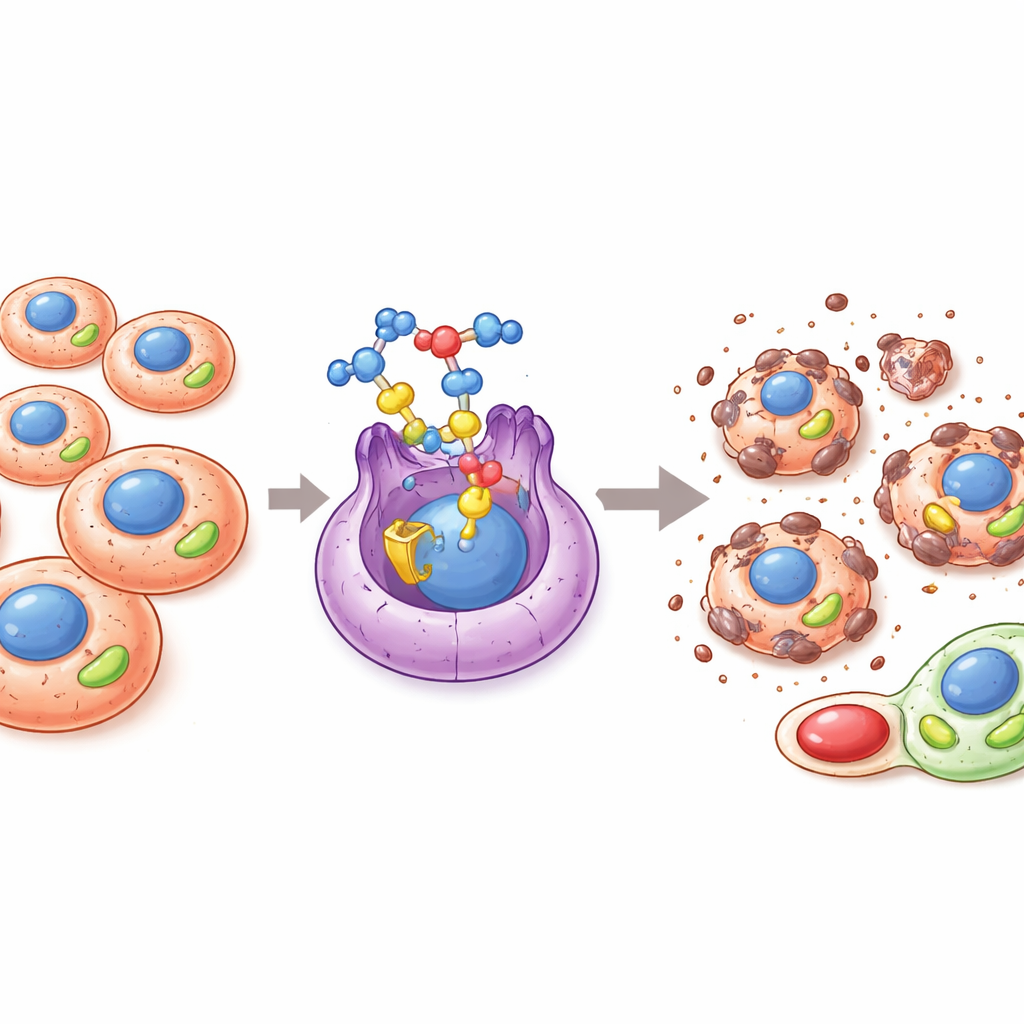
Eens binnen in leukemie‑ en solide tumorcellen verstoort PAMT‑001 sterk de mitochondriale functie. Genexpressieanalyses toonden een brede onderdrukking van genen voor oxidatieve fosforylering, en metingen van zuurstofconsumptie live lieten een duidelijke daling zien in basale en piekrespiratie en in ATP‑productie. Onder de microscoop werden mitochondriën in behandelde cellen opgezwollen en misvormd, met cristae—de binnenvouwen waar energieprocessen plaatsvinden—verwijd of verdwenen. Deze schade leidt tot overproductie van reactieve zuurstofsoorten, agressieve moleculen die zowel mitochondriën als het naburige endoplasmatisch reticulum, het vouwhub voor eiwitten, belasten. Antioxidanten herstelden de celoverleving deels, wat bevestigt dat deze oxidatieve uitbarsting een belangrijke drijvende kracht is achter de effecten van het middel.
Drie doodsroutes in plaats van één
In plaats van te vertrouwen op één schakel activeert PAMT‑001 tegelijkertijd meerdere gereguleerde doodsprogramma’s. Het triggert klassieke intrinsieke apoptose: mitochondriën geven cytochroom c af, uitvoerende enzymen genaamd caspases worden geknipt en geactiveerd, en celmembranen vertonen kenmerkende blaarvorming; pan‑caspase‑remmers dempen dit effect aanzienlijk. Tegelijkertijd induceert het middel krachtige autofagie, waarbij dubbelmembraanblaasjes vormen en beschadigde mitochondriën en ander celmateriaal insluiten. Het blokkeren van dit proces met autofagieremmers of door een sleutelgen voor autofagie uit te schakelen, vermindert celdood en verlaagt stresssignalen, wat aangeeft dat autofagie in deze context overgeactiveerd en schadelijk in plaats van beschermend wordt. Ten slotte veroorzaakt PAMT‑001 een vurig type celdood dat pyroptose heet: poriën openen in het celmembraan, inhoud lekt weg en een eiwit genaamd gasdermin E wordt gekliefd tot een porievormend fragment. Gezamenlijk vormen pyroptose, apoptose en autophagische celdood wat de auteurs “PAAoptose” noemen, een gecoördineerde multi‑route ineenstorting van de kankercel.

Belofte voor moeilijk behandelbare kankers
PAMT‑001 werkte niet alleen in petrischaaltjes. In muismodellen van dikkedarmkanker en acute myeloïde leukemie vertraagde het middel tumorgroei, verminderde het aantal leukemiecellen in het beenmerg en verlaagde het algemene kankergehalte zoals gemeten met beeldvorming, en dat alles zonder duidelijke schade aan lichaamsgewicht of normale cellen. Monsters van patiënten met acute myeloïde leukemie waren over het algemeen gevoeliger voor PAMT‑001 dan gezonde bloedcellen, en leukemieën met mutaties in een gen genaamd NPM1—vaak geassocieerd met hoge mitochondriale activiteit—waren bijzonder kwetsbaar. Het middel doodde ook leukemiecellen die resistent waren tegen cytarabine en longkankercellen resistent tegen een EGFR‑gericht medicijn, wat suggereert dat de brede aanval op mitochondriaal metabolisme en de multi‑route celdood kan helpen om behandelingsresistentie te overwinnen.
Wat dit betekent voor toekomstige kankerzorg
Dit werk introduceert PAMT‑001 als prototype van een nieuw type kankermiddel dat een energiecontrolerende schakel target en tumoren dwingt tot PAAoptose, een mengsel van drie destructieve doodsprogramma’s. Door de energietoevoer te ondermijnen en meerdere vitale systemen tegelijk te belasten, laten dergelijke middelen kankercellen minder ruimte om resistentie te ontwikkelen. Hoewel PAMT‑001 zelf meer tests nodig heeft voor veiligheid, dosering en langetermijneffecten, wijst de studie op therapieën die de unieke energievraag van kankercellen exploiteren en multi‑route celdood gebruiken om hardnekkige tumoren minder kans te geven terug te veren.
Bronvermelding: Seo, W., Heo, Y., Tran, K.V. et al. A novel PAAoptosis-inducing ERRα-targeting compound for combating hematopoietic and solid cancers. Cell Death Discov. 12, 188 (2026). https://doi.org/10.1038/s41420-026-03010-4
Trefwoorden: kankermetabolisme, mitochondriën, ERR alfa, geneesmiddelresistentie, celdoodroutes