Clear Sky Science · fr
Un nouveau composé ciblant ERRα et induisant la PAAoptose pour lutter contre les cancers hématopoïétiques et solides
Pourquoi cette nouvelle étude sur le cancer est importante
Les médicaments anticancéreux tentent généralement de bloquer un point faible isolé des cellules tumorales, mais les cancers s’adaptent souvent et deviennent résistants. Cette étude décrit un nouveau médicament expérimental, nommé PAMT‑001, qui attaque les cellules cancéreuses d’une manière très différente : en submergeant leurs centrales énergétiques et en déclenchant plusieurs types de mort cellulaire simultanément. Ce travail suggère une stratégie nouvelle pour combattre à la fois les cancers du sang et les tumeurs solides, y compris des formes qui ne répondent plus bien à la chimiothérapie standard.
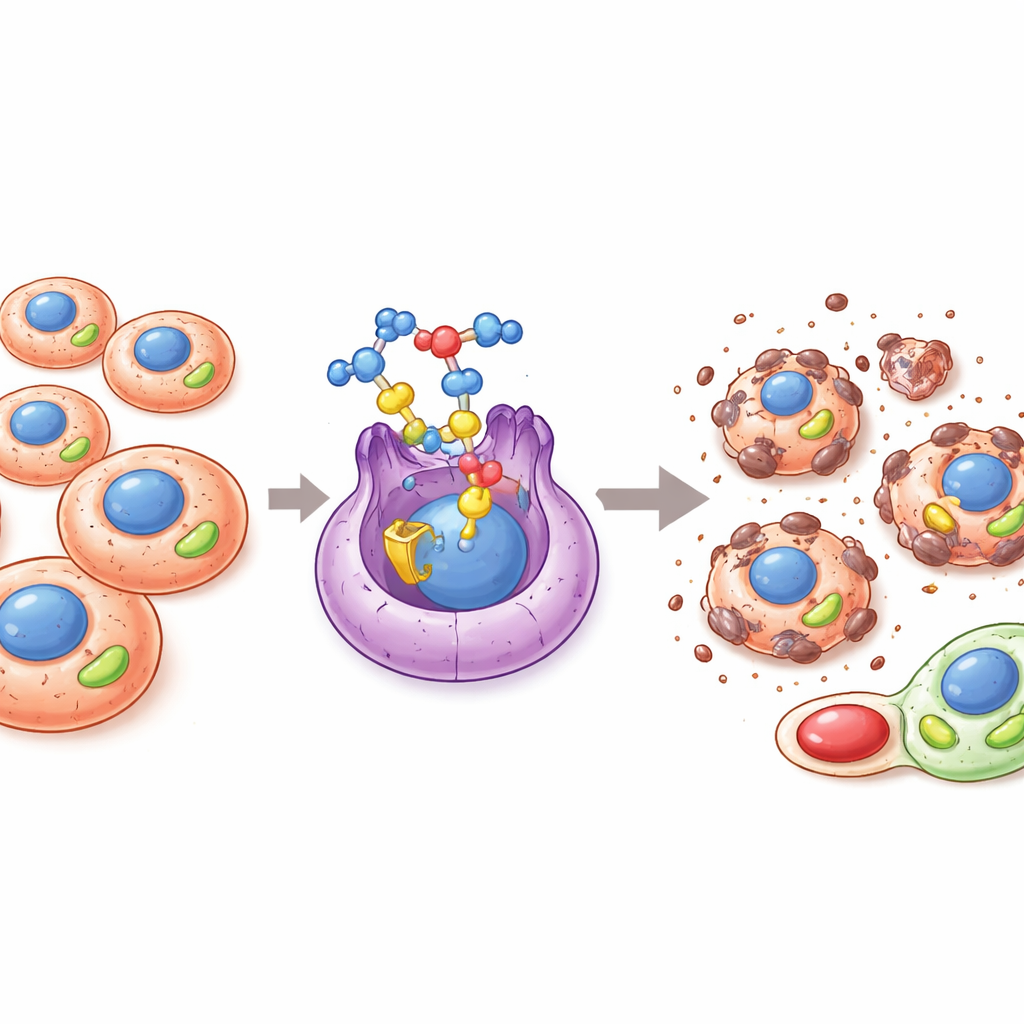
Un interrupteur caché qui alimente la croissance tumorale
Beaucoup de cancers reconfigurent la manière dont ils produisent et utilisent l’énergie pour croître, se disséminer et résister aux traitements. Un acteur clé de cette réorganisation métabolique est une protéine connue sous le nom d’ERRα, un type d’interrupteur moléculaire dans le noyau cellulaire qui contrôle des gènes impliqués dans la production d’énergie mitochondriale et l’équilibre redox. Lorsque ERRα est excessivement actif, les tumeurs peuvent augmenter leur production mitochondriale, neutraliser les sous‑produits oxydants nocifs, maintenir des cellules cancéreuses à caractéristiques souches et mieux survivre à des conditions difficiles comme l’hypoxie ou l’exposition aux médicaments. Pour ces raisons, ERRα a suscité de l’intérêt comme cible prometteuse pour de nouvelles thérapies anticancéreuses visant à couper les avantages énergétiques de la tumeur.
Concevoir un bloqueur du cancer plus malin
Les chercheurs sont partis d’une ancienne molécule inhibitrice d’ERRα, XCT‑790, et l’ont reconfigurée chimiquement pour créer une famille de composés apparentés. Parmi douze candidats, PAMT‑001 est apparu comme le plus puissant pour tuer les cellules cancéreuses, bien qu’en laboratoire il se lie en réalité à ERRα un peu moins fortement que XCT‑790. La modélisation informatique et des essais rapporteurs ont montré que PAMT‑001 peut s’insérer dans la même région d’ERRα qui interagit normalement avec une protéine co‑activateur appelée PGC1α, laquelle amplifie le contrôle d’ERRα sur les gènes mitochondriaux. En perturbant ce partenariat, PAMT‑001 bloque plus efficacement les programmes métaboliques pilotés par ERRα, en particulier dans les cellules qui dépendent fortement de cet axe pour leur survie.
Priver les centrales énergétiques de la cellule
Une fois dans les cellules de leucémie et des tumeurs solides, PAMT‑001 perturbe fortement la fonction mitochondriale. Des analyses d’expression génique ont révélé une suppression étendue des gènes de la phosphorylation oxydative, et des mesures en direct de la consommation d’oxygène ont montré une chute marquée de la respiration de base et maximale ainsi que de la production d’ATP. Au microscope, les mitochondries des cellules traitées apparaissaient gonflées et déformées, avec des crêtes — replis internes où se déroulent les réactions énergétiques — élargies ou absentes. Ces dégâts entraînent une production excessive d’espèces réactives de l’oxygène, des molécules chimiquement agressives qui fatiguent à la fois les mitochondries et le réticulum endoplasmique voisin, le centre de maturation des protéines de la cellule. Les antioxydants ont partiellement restauré la survie cellulaire, confirmant que cette poussée oxydative est un moteur clé des effets du médicament.
Trois voies de mort au lieu d’une
Plutôt que de s’appuyer sur un seul interrupteur létal, PAMT‑001 active plusieurs programmes de mort régulée en parallèle. Il déclenche l’apoptose intrinsèque classique : les mitochondries libèrent le cytochrome c, des enzymes exécutrices appelées caspases sont clivées et activées, et les membranes cellulaires présentent le blebbing caractéristique ; des inhibiteurs pan‑caspases atténuent sensiblement cet effet. Simultanément, le composé induit une autophagie marquée, dans laquelle des sacs à double membrane se forment et engloutissent les mitochondries endommagées et d’autres composants cellulaires. Bloquer ce processus avec des inhibiteurs de l’autophagie ou en désactivant un gène essentiel de l’autophagie réduit la mort cellulaire et diminue les signaux de stress, indiquant que, dans ce contexte, l’autophagie devient surexcitée et délétère plutôt que protectrice. Enfin, PAMT‑001 provoque une forme incendiaire de mort appelée pyroptose : des pores s’ouvrent dans la membrane cellulaire, le contenu fuit, et une protéine nommée gasdermine E est clivée en un fragment formant des pores. Ensemble, pyroptose, apoptose et mort autophagique se combinent en ce que les auteurs appellent la « PAAoptose », un effondrement coordonné et multi‑voies de la cellule cancéreuse.

Promesse pour les cancers difficiles à traiter
PAMT‑001 n’a pas seulement été efficace en culture cellulaire. Dans des modèles murins de cancer du côlon et de leucémie aiguë myéloblastique, le médicament a ralenti la croissance tumorale, réduit les cellules leucémiques dans la moelle osseuse et diminué la charge tumorale globale mesurée par imagerie, le tout sans effet évident sur le poids corporel ou les cellules normales. Des prélèvements de patients atteints de leucémie aiguë myéloblastique étaient en général plus sensibles à PAMT‑001 que les cellules sanguines saines, et les leucémies portant des mutations du gène NPM1 — souvent associées à une activité mitochondriale élevée — étaient particulièrement vulnérables. Le composé a aussi tué des cellules leucémiques résistantes à la cytarabine et des cellules de cancer du poumon résistantes à un médicament ciblant EGFR, suggérant que son attaque large sur le métabolisme mitochondrial et la mort cellulaire multi‑voies pourrait aider à surmonter la résistance aux traitements.
Ce que cela implique pour les soins oncologiques futurs
Ce travail présente PAMT‑001 comme un prototype d’un nouveau type de médicament anticancéreux qui cible un interrupteur contrôlant l’énergie et pousse les tumeurs vers la PAAoptose, un mélange de trois programmes destructeurs de mort cellulaire. En s’attaquant à l’alimentation énergétique et en stressant plusieurs systèmes vitaux à la fois, de tels médicaments pourraient laisser moins de marge aux cellules cancéreuses pour développer des mécanismes de résistance. Bien que PAMT‑001 lui‑même doive encore être testé pour la sécurité, le dosage et les effets à long terme, l’étude oriente vers des thérapies qui exploitent les demandes énergétiques particulières des cellules cancéreuses et utilisent une mort cellulaire multi‑voies pour empêcher les tumeurs tenaces de rebondir.
Citation: Seo, W., Heo, Y., Tran, K.V. et al. A novel PAAoptosis-inducing ERRα-targeting compound for combating hematopoietic and solid cancers. Cell Death Discov. 12, 188 (2026). https://doi.org/10.1038/s41420-026-03010-4
Mots-clés: métabolisme du cancer, mitochondries, ERR alpha, résistance aux médicaments, voies de mort cellulaire