Clear Sky Science · es
Un nuevo compuesto que induce PAAoptosis y se dirige a ERRα para combatir cánceres hematológicos y sólidos
Por qué importa este nuevo estudio sobre el cáncer
Los fármacos contra el cáncer suelen intentar bloquear un único punto débil en las células tumorales, pero los cánceres a menudo se adaptan y desarrollan resistencia. Este estudio describe un nuevo fármaco experimental, llamado PAMT‑001, que ataca a las células cancerosas de una forma muy diferente: sobrecargando sus centrales energéticas y desencadenando varios tipos de muerte celular a la vez. El trabajo sugiere una estrategia novedosa para abordar tanto los cánceres de la sangre como los tumores sólidos, incluidas formas que ya no responden bien a la quimioterapia estándar.
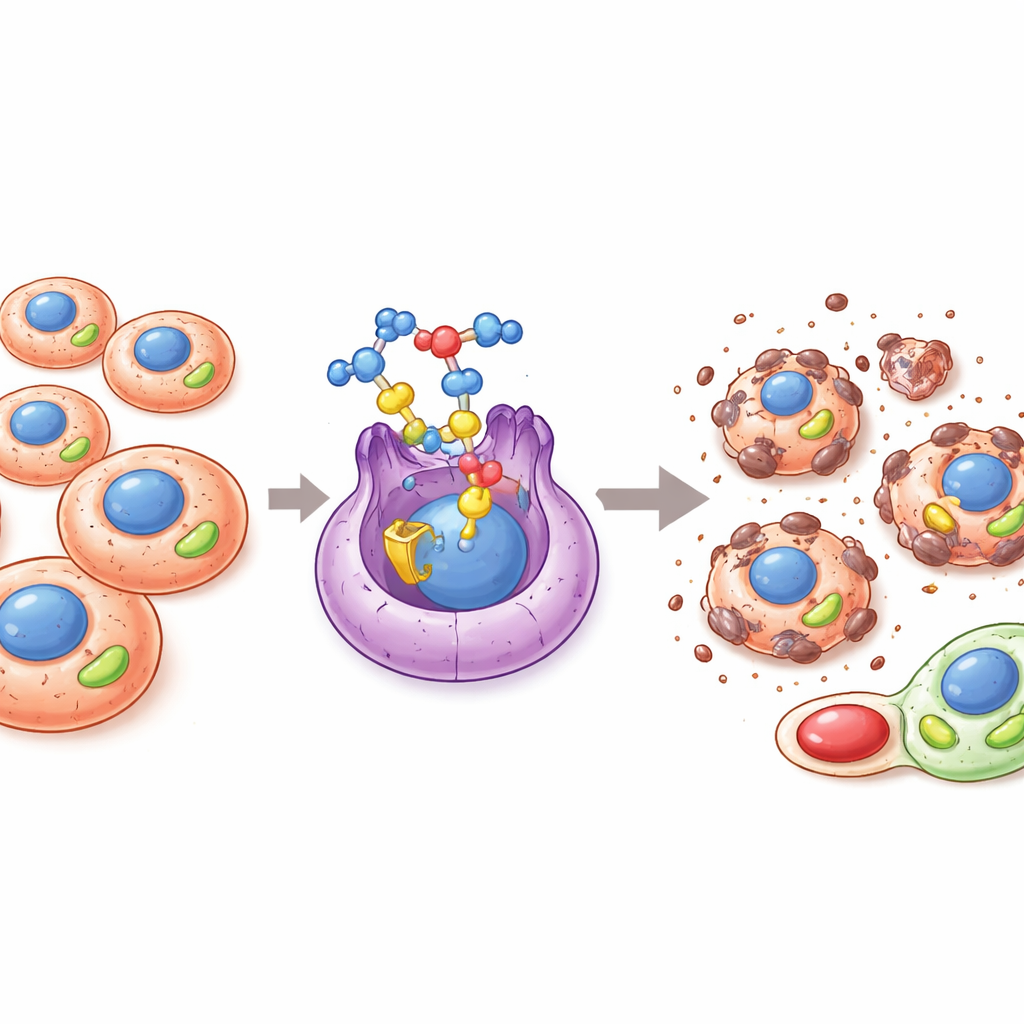
Un interruptor oculto que impulsa el crecimiento del cáncer
Muchos cánceres reconectan la forma en que generan y usan la energía para crecer, diseminarse y resistir los tratamientos. Un actor clave en esta remodelación metabólica es una proteína conocida como ERRα, un tipo de interruptor molecular en el núcleo celular que controla genes implicados en la producción de energía mitocondrial y el equilibrio redox. Cuando ERRα está sobreactivado, los tumores pueden aumentar su rendimiento mitocondrial, neutralizar subproductos oxigenados dañinos, mantener células cancerosas con rasgos de progenitor y sobrevivir mejor en condiciones adversas como la hipoxia o la exposición a fármacos. Por ello, ERRα ha atraído la atención como un objetivo prometedor para nuevas terapias contra el cáncer que buscan cortar las ventajas energéticas del tumor.
Diseñando un bloqueador del cáncer más inteligente
Los investigadores partieron de una molécula bloqueadora de ERRα anterior, XCT‑790, y la rediseñaron químicamente para crear una familia de compuestos relacionados. De doce candidatos, PAMT‑001 emergió como el más potente para matar células cancerosas, aunque en pruebas de laboratorio se une a ERRα algo menos fuerte que XCT‑790. Modelado por ordenador y ensayos con reporteros mostraron que PAMT‑001 puede alojarse en la misma región de ERRα que normalmente interactúa con una proteína coactivadora llamada PGC1α, que potencia el control de ERRα sobre genes mitocondriales. Al interferir con esta asociación, PAMT‑001 apaga de forma más eficaz los programas metabólicos impulsados por ERRα, especialmente en células que dependen en gran medida de este eje para sobrevivir.
Hambre en las centrales energéticas de la célula
Una vez dentro de las células de leucemia y tumores sólidos, PAMT‑001 perturba con fuerza la función mitocondrial. Los análisis de expresión génica revelaron una supresión extensa de genes de fosforilación oxidativa, y mediciones en vivo del consumo de oxígeno mostraron una caída notable en la respiración basal y máxima, así como en la producción de ATP. Bajo el microscopio, las mitocondrias de las células tratadas se volvieron hinchadas y deformes, con cristas —los repliegues internos donde ocurren las reacciones energéticas— ensanchadas o perdidas. Este daño provoca una producción excesiva de especies reactivas de oxígeno, moléculas químicamente agresivas que afectan tanto a las mitocondrias como al retículo endoplásmico vecino, el centro de plegamiento de proteínas de la célula. Los antioxidantes rescataron parcialmente la supervivencia celular, confirmando que este estallido oxidativo es un impulsor clave de los efectos del fármaco.
Tres rutas de muerte en lugar de una
En lugar de depender de un único interruptor letal, PAMT‑001 activa varios programas regulados de muerte en paralelo. Desencadena la apoptosis intrínseca clásica: las mitocondrias liberan citocromo c, las enzimas ejecutoras llamadas caspasas se escinden y activan, y las membranas celulares presentan el característico blebbing; los inhibidores pan‑caspasa atenúan sustancialmente este efecto. Al mismo tiempo, el fármaco induce una autofagia intensa, en la que se forman sacos de doble membrana que engullen mitocondrias dañadas y otros contenidos celulares. Bloquear este proceso con inhibidores de la autofagia o desactivando un gen clave de la autofagia reduce la muerte celular y disminuye las señales de estrés, lo que indica que, en este contexto, la autofagia se sobreactiva y resulta perjudicial en lugar de protectora. Finalmente, PAMT‑001 desencadena una forma inflamatoria de muerte llamada piroptosis: se abren poros en la membrana celular, el contenido se filtra y una proteína llamada gasdermina E se escinde en un fragmento que forma poros. Juntas, la piroptosis, la apoptosis y la muerte por autofagia se combinan en lo que los autores denominan “PAAoptosis”, un colapso coordinado y multipista de la célula cancerosa.

Promesa para cánceres difíciles de tratar
PAMT‑001 no solo funcionó en placas de laboratorio. En modelos murinos de cáncer de colon y leucemia mieloide aguda, el fármaco ralentizó el crecimiento tumoral, redujo las células leucémicas en la médula ósea y disminuyó la carga tumoral total medida por imagen, todo ello sin daño evidente en el peso corporal o en las células normales. Muestras de pacientes con leucemia mieloide aguda fueron en general más sensibles a PAMT‑001 que las células sanguíneas sanas, y las leucemias con mutaciones en un gen llamado NPM1 —a menudo asociadas con alta actividad mitocondrial— fueron especialmente vulnerables. El fármaco también mató células leucémicas resistentes a citarabina y células de cáncer de pulmón resistentes a un fármaco dirigido contra EGFR, lo que sugiere que su ataque amplio al metabolismo mitocondrial y la muerte celular por múltiples vías podría ayudar a superar la resistencia al tratamiento.
Qué significa esto para la atención futura del cáncer
Este trabajo presenta a PAMT‑001 como un prototipo de un nuevo tipo de fármaco contra el cáncer que apunta a un interruptor que controla la energía y fuerza a los tumores a entrar en PAAoptosis, una combinación de tres programas destructivos de muerte. Al socavar el suministro energético y estresar varios sistemas vitales a la vez, tales fármacos podrían dejar menos margen a las células cancerosas para evolucionar resistencia. Aunque PAMT‑001 en sí requerirá más pruebas de seguridad, dosificación y efectos a largo plazo, el estudio apunta hacia terapias que explotan las demandas energéticas únicas de las células tumorales y utilizan la muerte celular multimodal como forma de impedir que los tumores persistentes se recuperen.
Cita: Seo, W., Heo, Y., Tran, K.V. et al. A novel PAAoptosis-inducing ERRα-targeting compound for combating hematopoietic and solid cancers. Cell Death Discov. 12, 188 (2026). https://doi.org/10.1038/s41420-026-03010-4
Palabras clave: metabolismo del cáncer, mitocondrias, ERR alfa, resistencia a fármacos, vías de muerte celular