Clear Sky Science · ja
造血系および固形がんと闘うための新しいPAAoptosis誘導ERRα標的化化合物
この新しいがん研究が重要な理由
多くのがん薬は腫瘍細胞の単一の弱点を狙って機能を止めようとしますが、がんはしばしば適応して耐性を獲得します。本研究はPAMT‑001と名付けられた新しい実験的化合物を紹介します。これは従来とは異なるやり方でがん細胞を攻撃し、エネルギー供給源を圧倒して複数の種類の細胞死を同時に誘導します。この成果は、血液がんや固形腫瘍、標準的な化学療法に反応しにくくなった形態も含めて、新たな攻撃戦略を示唆します。
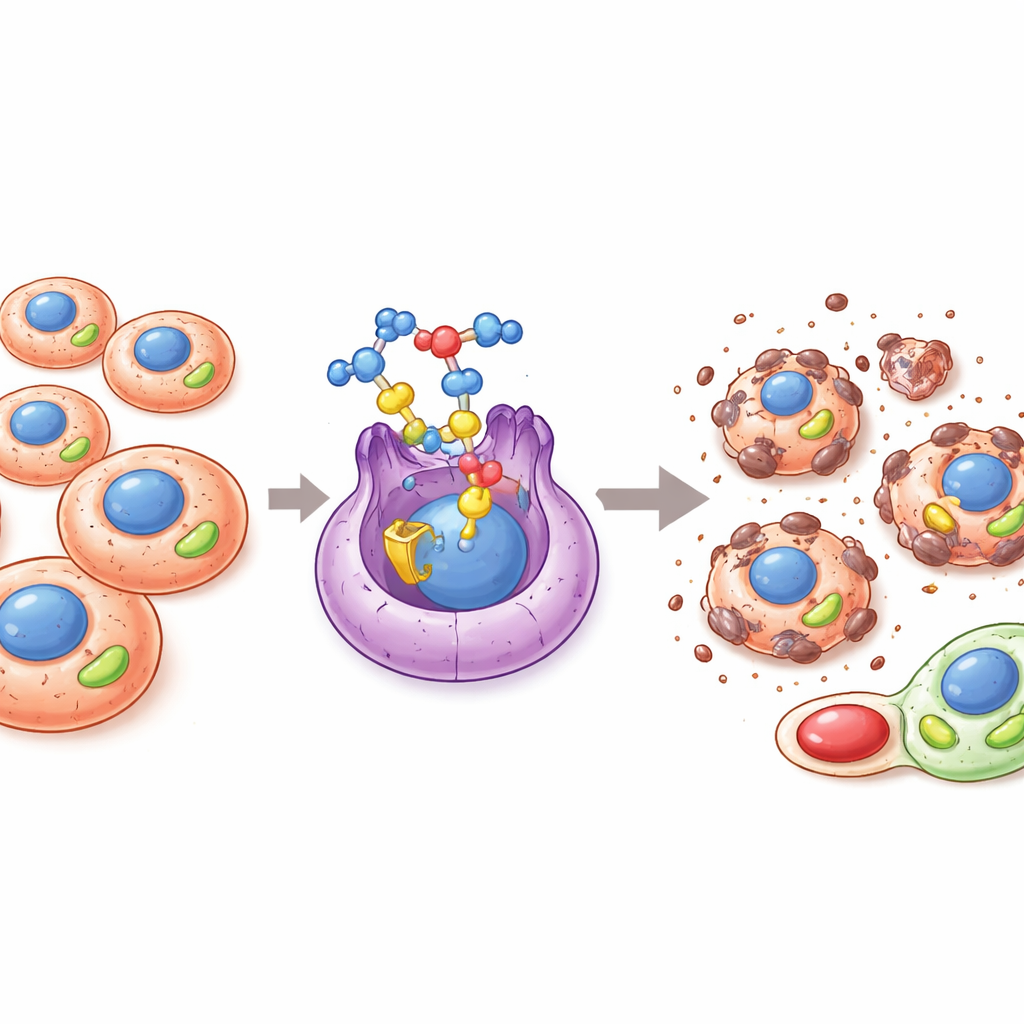
がんの成長を駆動する隠れたスイッチ
多くのがんは増殖、転移、治療抵抗性を獲得するためにエネルギーの作り方と利用方法を書き換えます。その代謝再編成の重要な担い手の一つがERRαと呼ばれるタンパク質で、核内にある分子的なスイッチの一種としてミトコンドリアのエネルギー産生やレドックス(酸化還元)バランスに関わる遺伝子を制御します。ERRαが過剰に活性化すると、腫瘍はミトコンドリアの出力を高め、有害な酸素代謝物を処理し、幹様のがん細胞を維持し、低酸素や薬剤暴露のような過酷な条件下でも生き残りやすくなります。このため、ERRαは腫瘍のエネルギー的優位を断つことを狙う新しいがん治療の有望な標的として注目されています。
より賢いがん阻害剤の設計
研究者らは古いERRα阻害分子XCT‑790を出発点に化学修飾を加え、一群の類縁化合物を設計しました。12候補のうちPAMT‑001が最も強力にがん細胞を死滅させることが示されました。興味深いことに、試験管内の結合アッセイではXCT‑790よりやや弱くERRαに結合するにもかかわらず、PAMT‑001は効果が高かったのです。コンピューターモデリングやレポーターアッセイは、PAMT‑001が通常は共活性化因子PGC1αと相互作用するERRαの同じ領域に収まり込めることを示しました。PGC1αはERRαのミトコンドリア遺伝子制御を強化するため、この相互作用を妨げることでPAMT‑001はERRα駆動の代謝プログラムをより効果的に遮断し、特にこの軸に依存して生きる細胞で強い作用を示します。
細胞の発電所を飢餓状態にする
白血病および固形腫瘍細胞に取り込まれたPAMT‑001はミトコンドリア機能を強く撹乱します。遺伝子発現解析は酸化的リン酸化遺伝子群の広範な抑制を明らかにし、酸素消費の生測定では基礎呼吸および最大呼吸、さらにATP産生の著しい低下が示されました。顕微鏡下では、処理された細胞のミトコンドリアが膨張して形が崩れ、エネルギー反応が行われる内膜のひだ(クリステ)が広がるか消失していました。この損傷は反応性酸素種(ROS)の過剰生成を招き、ミトコンドリアと隣接する小胞体(タンパク質折りたたみの中枢)に負荷をかけます。抗酸化剤は細胞生存を部分的に回復させたため、この酸化的な爆発が薬剤効果の重要な推進因子であることが確認されました。
一つではなく三つの死の経路
PAMT‑001は単一のスイッチに頼るのではなく、複数の制御された死プログラムを同時に活性化します。まず古典的な内因性アポトーシスを誘導します:ミトコンドリアからシトクロムcが放出され、エフェクター酵素であるカスパーゼが切断・活性化され、細胞膜に特徴的なブレbbingが現れます。汎カスパーゼ阻害剤はこの効果をかなり抑えます。同時に、二重膜の小胞が形成され損傷ミトコンドリアや細胞内容物を取り込む強いオートファジーが誘導されます。オートファジー阻害剤や主要なオートファジー遺伝子の機能喪失でこの過程を阻むと細胞死とストレスシグナルが減少し、この文脈ではオートファジーが保護的ではなく過剰活性化され有害になることを示しています。最後に、PAMT‑001はピロトーシスと呼ばれる炎のような形の死を引き起こします:細胞膜に孔が開き内容物が漏出し、ガスダーミンEというタンパク質が孔形成断片に切断されます。ピロトーシス、アポトーシス、オートファジー性細胞死が合わさり、著者らはこれを“PAAoptosis”と呼ぶ、協調的で多経路からのがん細胞の崩壊としてまとめています。

治療が難しいがんへの可能性
PAMT‑001は培養皿内だけで働いたわけではありません。結腸がんおよび急性骨髄性白血病のマウスモデルで、この薬は腫瘍成長を遅らせ、骨髄中の白血病細胞を減少させ、イメージングで測定した全体的ながん負荷を低下させましたが、体重や正常細胞への明らかな有害影響は見られませんでした。急性骨髄性白血病患者由来のサンプルは一般に健常な血液細胞よりPAMT‑001に対して感受性が高く、ミトコンドリア活性が高いこととしばしば関連するNPM1遺伝子変異を有する白血病は特に脆弱でした。またこの薬はシタラビンに耐性を示す白血病細胞やEGFR標的薬に耐性を示す肺がん細胞も殺し、ミトコンドリア代謝への広範な攻撃と多経路の細胞死誘導が治療耐性を克服する助けになる可能性を示唆します。
今後のがん治療にとっての意義
本研究はPAMT‑001を、エネルギー制御スイッチを標的として腫瘍をPAAoptosisへと追い込み、三つの破壊的な死のプログラムを組み合わせる新しい種類のがん薬のプロトタイプとして提示します。電源供給を弱め、複数の重要系に同時に負荷をかけることで、がん細胞が抵抗性を進化させる余地を小さくできる可能性があります。PAMT‑001自体は安全性、投与法、長期影響についてさらなる検証が必要ですが、本研究はがん細胞の特異的なエネルギー需要を突き、複数経路の細胞死を利用して手強い腫瘍の再発を防ぐ治療法の方向性を示しています。
引用: Seo, W., Heo, Y., Tran, K.V. et al. A novel PAAoptosis-inducing ERRα-targeting compound for combating hematopoietic and solid cancers. Cell Death Discov. 12, 188 (2026). https://doi.org/10.1038/s41420-026-03010-4
キーワード: がん代謝, ミトコンドリア, ERRα, 薬剤耐性, 細胞死経路