Clear Sky Science · ru
Новый индуцирующий PAAоптоз препарат, нацеленный на ERRα, для борьбы с гемопоэтическими и солидными опухолями
Почему это новое исследование рака важно
Противораковые препараты обычно пытаются блокировать одну уязвимую точку в опухолевых клетках, но опухоли часто адаптируются и становятся устойчивыми. В этом исследовании описан новый экспериментальный препарат, названный PAMT‑001, который атакует раковые клетки совсем иначе: переполняя их энергетические «фабрики» и одновременно вызывая несколько типов клеточной гибели. Работа предлагает новую стратегию борьбы как с заболеваниями крови, так и с солидными опухолями, в том числе с формами, которые уже плохо реагируют на стандартную химиотерапию.
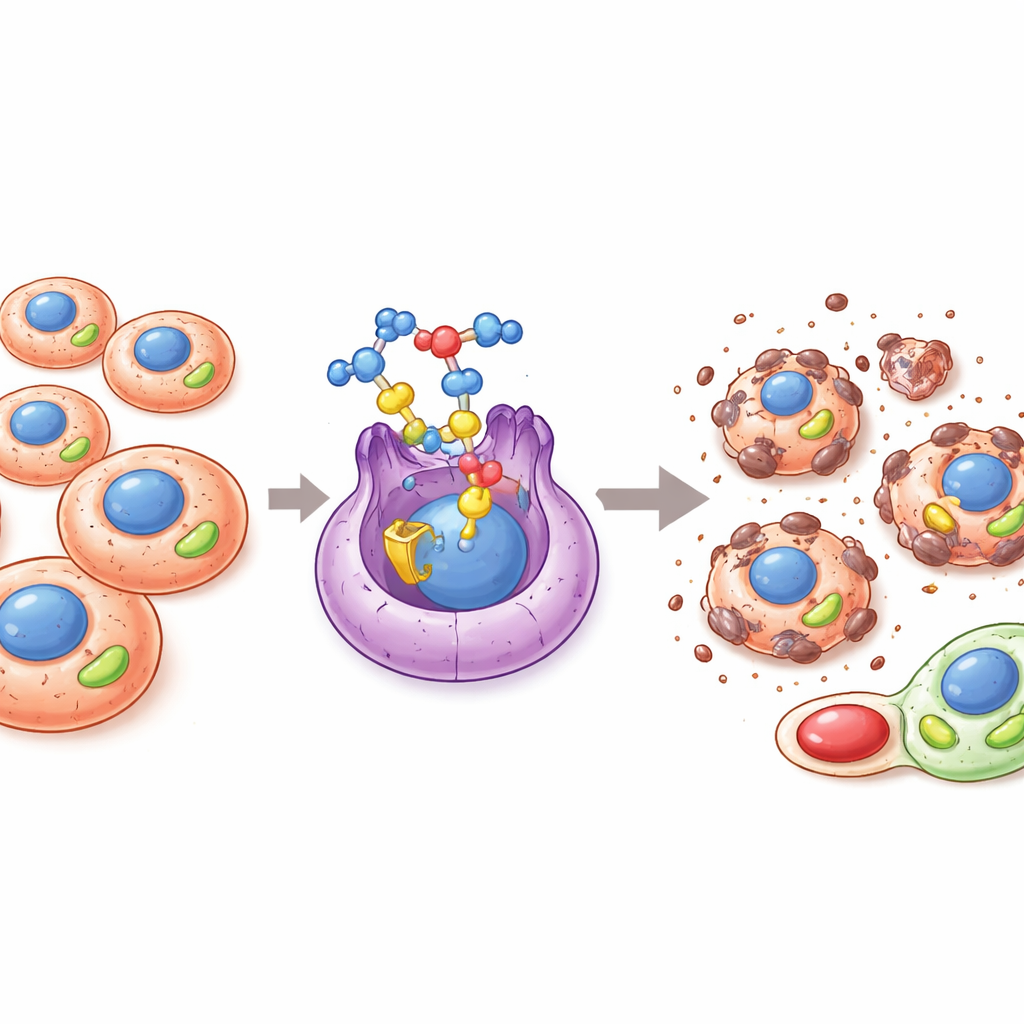
Скрытый переключатель, подпитывающий рост рака
Многие раки перенастраивают способы производства и использования энергии, чтобы расти, распространяться и сопротивляться лечению. Ключевым участником этой метаболической перестройки является белок, известный как ERRα — тип молекулярного переключателя в ядре клетки, контролирующий гены, вовлечённые в митохондриальное производство энергии и поддержание редокс‑баланса. При гиперактивации ERRα опухоли могут усиливать митохондриальную выработку энергии, устранять вредные кислородные побочные продукты, поддерживать стволоподобные раковые клетки и лучше выживать в тяжёлых условиях, таких как гипоксия или воздействие лекарств. По этой причине ERRα рассматривают как перспективную мишень для новых противораковых терапий, стремящихся лишить опухоль её энергетического преимущества.
Разработка более умного блокатора рака
Исследователи начали с предыдущей молекулы‑ингибитора ERRα, XCT‑790, и химически переработали её, создав семейство родственных соединений. Из двенадцати кандидатов PAMT‑001 оказался наиболее мощным в уничтожении раковых клеток, хотя в лабораторных тестах он фактически связывается с ERRα несколько слабее, чем XCT‑790. Компьютерное моделирование и репортерные анализы показали, что PAMT‑001 может встраиваться в тот же участок ERRα, который обычно взаимодействует с ко‑активатором PGC1α, усиливающим контроль ERRα над митохондриальными генами. Нарушая это сотрудничество, PAMT‑001 эффективнее отключает метаболические программы, управляемые ERRα, особенно в клетках, сильно зависящих от этой оси для выживания.
Истощение «электростанций» клетки
Попав в клетки лейкемии и солидных опухолей, PAMT‑001 сильно нарушает функцию митохондрий. Анализы экспрессии генов выявили широкое подавление генов окислительного фосфорилирования, а измерения потребления кислорода в реальном времени показали заметное падение как базального, так и максимального дыхания, а также производства АТФ. Под микроскопом митохондрии в обработанных клетках становились распухшими и деформированными, с расширенными или утраченными кристами — внутренними складками, где проходят энергетические реакции. Это повреждение приводит к избыточному образованию реактивных форм кислорода, агрессивных молекул, нагружающих как митохондрии, так и соседний эндоплазматический ретикулум — центр сворачивания белков в клетке. Антиоксиданты частично восстанавливали выживаемость клеток, подтверждая, что этот окислительный всплеск является ключевым драйвером эффекта препарата.
Три пути гибели вместо одного
Вместо того чтобы полагаться на один «выключатель», PAMT‑001 одновременно активирует несколько регулируемых программ гибели. Он стимулирует классическую внутреннюю апоптозу: митохондрии высвобождают цитохром c, исполнительные ферменты — каспазы — расщепляются и активируются, а мембраны клеток демонстрируют характерное образование пузырей; пан‑касказные ингибиторы существенно ослабляют этот эффект. Одновременно препарат индуцирует мощную аутофагию — формирование двойных мембранных вакуолей, которые поглощают повреждённые митохондрии и другие клеточные содержимые. Блокирование этого процесса ингибиторами аутофагии или отключение ключевого аутофагического гена уменьшает гибель клеток и снижает сигналы стресса, что указывает на то, что в данном контексте аутофагия становится чрезмерно активной и вредной, а не защитной. Наконец, PAMT‑001 вызывает огненную форму смерти — пироптоз: в мембране образуются поры, содержимое вытекает, и белок газдермин E расщепляется на фрагмент, формирующий поры. Вместе пироптоз, апоптоз и аутофагическая гибель клеток объединяются в то, что авторы называют «PAAоптозом», скоординированным много‑путевым крахом раковой клетки.

Перспективы для трудноизлечимых опухолей
PAMT‑001 оказался эффективен не только в культурах. В мышиных моделях колоректального рака и острой миелоидной лейкемии препарат замедлял рост опухолей, уменьшал количество лейкозных клеток в костном мозге и снижал общую опухолевую нагрузку по данным визуализации, при этом заметных побочных эффектов на массу тела или нормальные клетки не наблюдалось. Образцы от пациентов с острой миелоидной лейкемией в целом были более чувствительны к PAMT‑001, чем здоровые клетки крови, а лейкемии с мутациями в гене NPM1 — часто ассоциированном с высокой митохондриальной активностью — оказались особенно уязвимыми. Препарат также убивал лейкемические клетки, устойчивые к цитарабину, и клетки рака лёгкого, устойчивые к препаратам, нацеленным на EGFR, что указывает на то, что широкая атака на митохондриальный метаболизм и много‑путевые механизмы гибели могла бы помочь преодолеть лекарственную устойчивость.
Что это значит для будущего онкологической помощи
Эта работа представляет PAMT‑001 как прототип нового класса противораковых препаратов, нацеленных на энергетический переключатель и вынуждающих опухоли входить в PAAоптоз — сочетание трёх разрушительных программ гибели. Подрывая энергоснабжение и одновременно нагружая несколько жизненно важных систем, такие препараты могут уменьшить пространство для эволюции устойчивости у раковых клеток. Хотя сам PAMT‑001 потребует дальнейших испытаний на безопасность, определение доз и оценки долгосрочных эффектов, исследование указывает на подходы, использующие уникальные энергетические потребности раковых клеток и многопутевую гибель клеток как способ не дать стойким опухолям возродиться.
Цитирование: Seo, W., Heo, Y., Tran, K.V. et al. A novel PAAoptosis-inducing ERRα-targeting compound for combating hematopoietic and solid cancers. Cell Death Discov. 12, 188 (2026). https://doi.org/10.1038/s41420-026-03010-4
Ключевые слова: метаболизм рака, митохондрии, ERR альфа, лекарственная устойчивость, пути гибели клеток