Clear Sky Science · it
Un nuovo composto che induce la PAAoptosi mirando a ERRα per combattere i tumori ematopoietici e solidi
Perché questo nuovo studio sul cancro è importante
I farmaci antitumorali di solito cercano di bloccare un singolo punto debole nelle cellule tumorali, ma i tumori spesso si adattano e diventano resistenti. Questo studio descrive un nuovo farmaco sperimentale, chiamato PAMT‑001, che attacca le cellule tumorali in modo molto diverso: sovraccaricando le loro centrali energetiche e attivando contemporaneamente diversi tipi di morte cellulare. Il lavoro suggerisce una strategia nuova per affrontare sia i tumori del sangue sia i tumori solidi, comprese forme che non rispondono più efficacemente alla chemioterapia standard.
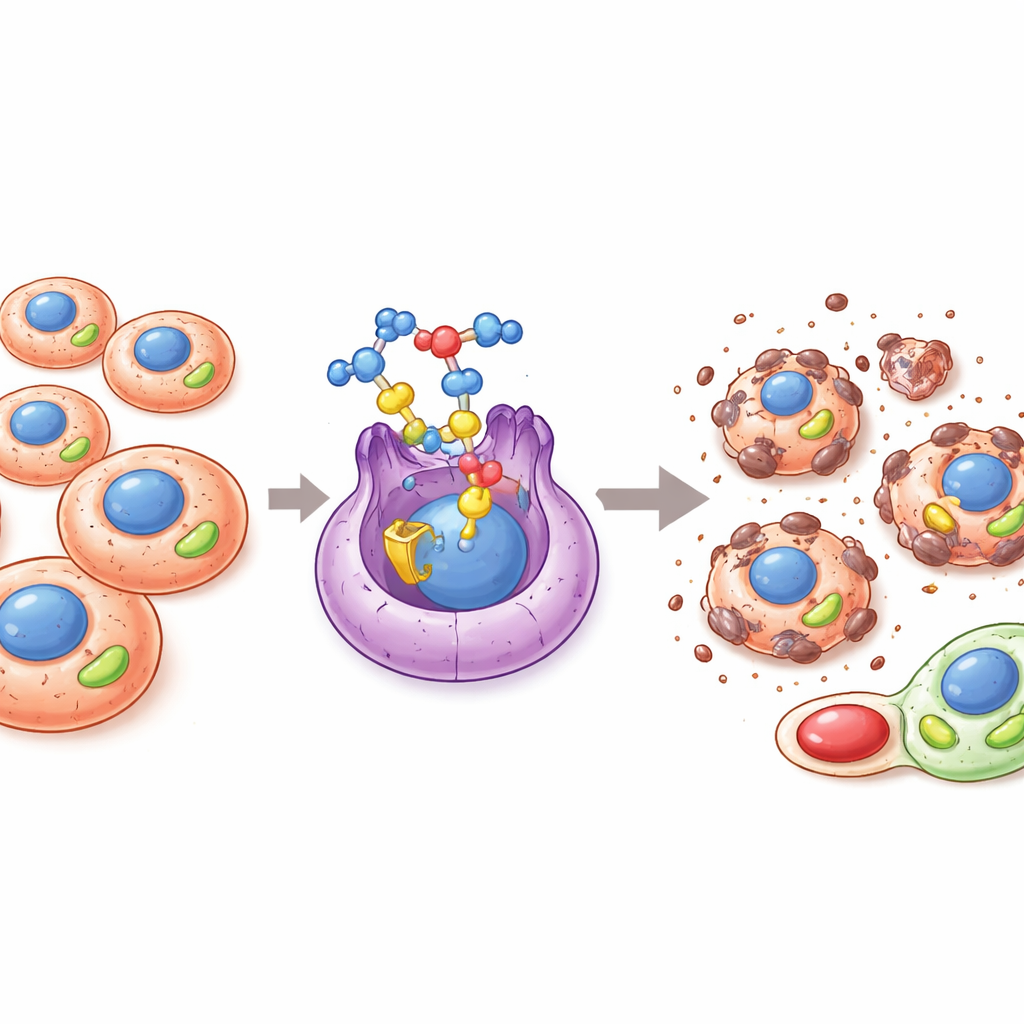
Un interruttore nascosto che alimenta la crescita tumorale
Molti tumori riorganizzano il modo in cui producono e usano energia per crescere, diffondersi e resistere ai trattamenti. Un protagonista chiave di questo rimodellamento metabolico è una proteina nota come ERRα, un tipo di interruttore molecolare nel nucleo cellulare che controlla geni coinvolti nella produzione energetica mitocondriale e nell’equilibrio redox. Quando ERRα è eccessivamente attivo, i tumori possono incrementare la produzione mitocondriale, smaltire sottoprodotti ossidativi nocivi, mantenere cellule tumorali con caratteristiche staminali e sopravvivere meglio a condizioni avverse come basso ossigeno o esposizione a farmaci. Per questo motivo, ERRα ha attirato attenzione come bersaglio promettente per nuove terapie antitumorali che puntano a tagliare i vantaggi energetici del tumore.
Progettare un blocco del cancro più intelligente
I ricercatori sono partiti da una vecchia molecola inibitrice di ERRα, XCT‑790, e l’hanno ridisegnata chimicamente per creare una famiglia di composti correlati. Su dodici candidati, PAMT‑001 è emerso come il più potente nell’uccidere le cellule tumorali, nonostante nei test di laboratorio si leghi a ERRα con forza leggermente inferiore rispetto a XCT‑790. Modellizzazione al computer e saggi con reporter hanno mostrato che PAMT‑001 può inserirsi nella stessa regione di ERRα che normalmente interagisce con una proteina co‑attivatrice chiamata PGC1α, la quale potenzia il controllo di ERRα sui geni mitocondriali. Interferendo con questa partnership, PAMT‑001 sopprime in modo più efficace i programmi metabolici guidati da ERRα, soprattutto in cellule che fanno grande affidamento su questo asse per sopravvivere.
Affamare le centrali energetiche della cellula
Una volta all’interno delle cellule leucemiche e dei tumori solidi, PAMT‑001 interrompe fortemente la funzione mitocondriale. Le analisi dell’espressione genica hanno rivelato una soppressione diffusa dei geni della fosforilazione ossidativa, e misure in vivo del consumo d’ossigeno hanno mostrato un calo marcato della respirazione basale e massima così come della produzione di ATP. Al microscopio, i mitocondri delle cellule trattate risultavano rigonfiati e deformi, con creste—le pieghe interne dove avvengono le reazioni energetiche—ampie o assenti. Questo danno porta a un’eccessiva produzione di specie reattive dell’ossigeno, molecole chimicamente aggressive che stressano sia i mitocondri sia il reticolo endoplasmatico vicino, l’hub del ripiegamento proteico cellulare. Gli antiossidanti hanno parzialmente ristabilito la sopravvivenza cellulare, confermando che questo scoppio ossidativo è un fattore chiave degli effetti del farmaco.
Tre vie di morte invece di una
Piuttosto che fare affidamento su un unico interruttore letale, PAMT‑001 attiva in parallelo diversi programmi regolati di morte. Innesca l’apoptosi intrinseca classica: i mitocondri rilasciano citocromo c, gli enzimi esecutori chiamati caspasi vengono clivati e attivati, e le membrane cellulari mostrano il caratteristico blebbing; gli inibitori pan‑caspasi attenuano sostanzialmente questo effetto. Allo stesso tempo, il farmaco induce una forte autofagia, in cui si formano sacchi a doppia membrana che inglobano mitocondri danneggiati e altri contenuti cellulari. Bloccare questo processo con inibitori dell’autofagia o disabilitando un gene chiave dell’autofagia riduce la morte cellulare e abbassa i segnali di stress, indicando che, in questo contesto, l’autofagia diventa iperattivata e dannosa piuttosto che protettiva. Infine, PAMT‑001 promuove una forma infiammatoria di morte chiamata piroptosi: si aprono pori nella membrana cellulare, i contenuti fuoriescono e una proteina chiamata gasdermin E viene clivata in un frammento che forma pori. Insieme, piroptosi, apoptosi e morte cellulare autofagica si combinano in ciò che gli autori definiscono “PAAoptosi”, un collasso coordinato e multi‑via della cellula tumorale.

Promesse per tumori difficili da trattare
PAMT‑001 non ha funzionato solo in colture cellulari. In modelli murini di cancro del colon e leucemia mieloide acuta, il farmaco ha rallentato la crescita tumorale, ridotto le cellule leucemiche nel midollo osseo e abbassato il carico tumorale complessivo misurato con imaging, il tutto senza effetti evidenti sul peso corporeo o sulle cellule normali. Campioni di pazienti con leucemia mieloide acuta sono risultati generalmente più sensibili a PAMT‑001 rispetto alle cellule del sangue sane, e le leucemie portatrici di mutazioni nel gene NPM1—spesso associate a elevata attività mitocondriale—erano particolarmente vulnerabili. Il farmaco ha inoltre ucciso cellule leucemiche resistenti alla citarabina e cellule di cancro polmonare resistenti a un farmaco mirato contro EGFR, suggerendo che il suo attacco ampio al metabolismo mitocondriale e la morte cellulare multi‑via potrebbero aiutare a superare la resistenza terapeutica.
Cosa significa per la futura cura del cancro
Questo lavoro introduce PAMT‑001 come prototipo di una nuova classe di farmaci antitumorali che prendono di mira un interruttore che controlla l’energia e costringono i tumori alla PAAoptosi, una combinazione di tre programmi distruttivi di morte. Minando la fonte di energia e stressando più sistemi vitali contemporaneamente, tali farmaci potrebbero lasciare meno spazio alle cellule tumorali per evolvere resistenza. Sebbene PAMT‑001 richieda ulteriori studi su sicurezza, dosaggio ed effetti a lungo termine, lo studio indica la strada verso terapie che sfruttano le richieste energetiche peculiari delle cellule tumorali e utilizzano la morte multi‑via come mezzo per impedire ai tumori ostinati di riprendersi.
Citazione: Seo, W., Heo, Y., Tran, K.V. et al. A novel PAAoptosis-inducing ERRα-targeting compound for combating hematopoietic and solid cancers. Cell Death Discov. 12, 188 (2026). https://doi.org/10.1038/s41420-026-03010-4
Parole chiave: metabolismo del cancro, mitocondri, ERR alfa, resistenza ai farmaci, vie di morte cellulare