Clear Sky Science · de
Eine neuartige PAAoptose‑auslösende, ERRα‑zielgerichtete Verbindung zur Bekämpfung hämatopoetischer und solider Krebserkrankungen
Warum diese neue Krebsstudie wichtig ist
Krebsmedikamente zielen meist darauf ab, eine einzelne Schwachstelle in Tumorzellen auszuschalten, doch Tumoren passen sich häufig an und entwickeln Resistenzen. Diese Studie beschreibt ein neues experimentelles Medikament namens PAMT‑001, das Krebszellen auf eine sehr andere Weise angreift: indem es ihre Energiezentralen überlastet und gleichzeitig mehrere Arten von Zelltod auslöst. Die Arbeit legt eine neue Strategie nahe, um sowohl Blutkrebserkrankungen als auch solide Tumoren anzugehen, einschließlich Formen, die auf die Standardchemotherapie nur noch schlecht ansprechen.
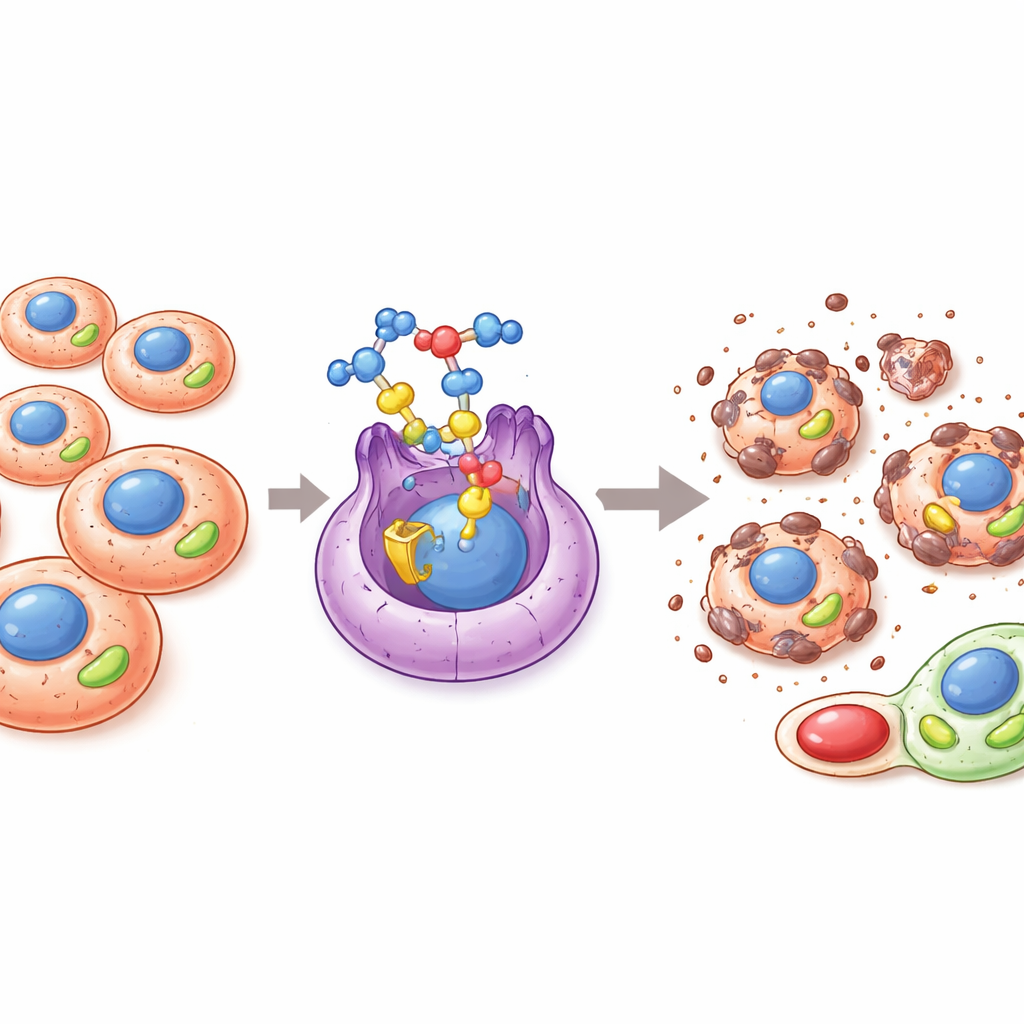
Ein verborgener Schalter, der das Krebswachstum antreibt
Viele Krebserkrankungen vernetzen die Art und Weise, wie sie Energie erzeugen und nutzen, neu, um zu wachsen, sich auszubreiten und Behandlungen zu widerstehen. Ein Schlüsselfaktor dieser metabolischen Umprogrammierung ist ein Protein namens ERRα, ein molekularer Schalter im Zellkern, der Gene steuert, die an der mitochondrialen Energieproduktion und der Redox‑Balance beteiligt sind. Ist ERRα übermäßig aktiv, können Tumoren ihre mitochondriale Leistung steigern, schädliche Sauerstoffnebenprodukte abfangen, stammzellähnliche Krebszellen erhalten und besser unter widrigen Bedingungen wie Sauerstoffmangel oder Medikamentenexposition überleben. Aus diesem Grund gilt ERRα als vielversprechendes Ziel für neue Krebstherapien, die die energetischen Vorteile des Tumors abschneiden wollen.
Entwicklung eines intelligenteren Krebsblockers
Die Forscher begannen mit einem älteren ERRα‑Blocker, XCT‑790, und überarbeiteten ihn chemisch, um eine Reihe verwandter Verbindungen zu schaffen. Von zwölf Kandidaten erwies sich PAMT‑001 als der wirksamste bei der Abtötung von Krebszellen, obwohl es in Labortests tatsächlich etwas schwächer an ERRα bindet als XCT‑790. Computermodelle und Reporter‑Assays zeigten, dass sich PAMT‑001 in denselben Bereich von ERRα einfügen kann, der normalerweise mit einem Co‑Aktivatorprotein namens PGC1α interagiert, das ERRαs Kontrolle über mitochondriale Gene verstärkt. Durch die Störung dieser Partnerschaft schaltet PAMT‑001 die von ERRα getriebenen Stoffwechselprogramme effektiver ab, insbesondere in Zellen, die stark auf diese Achse für ihr Überleben angewiesen sind.
Die Kraftwerke der Zelle aushungern
Einmal in Leukämie‑ und soliden Tumorzellen dringt PAMT‑001 stark in die mitochondriale Funktion ein. Genexpressionsanalysen zeigten eine breit angelegte Unterdrückung von Genen der oxidativen Phosphorylierung, und Messungen des Sauerstoffverbrauchs in lebenden Zellen dokumentierten einen deutlichen Rückgang von Basis‑ und Spitzenatmung sowie der ATP‑Produktion. Unter dem Mikroskop wurden die Mitochondrien in behandelten Zellen geschwollen und deformiert, mit erweiterten oder verlorenen Cristae — den inneren Falten, in denen Energieumsetzungen stattfinden. Diese Schäden führen zu einer übermäßigen Bildung reaktiver Sauerstoffspezies, aggressiven Molekülen, die sowohl die Mitochondrien als auch das angrenzende endoplasmatische Retikulum, das Proteinfaltungszentrum der Zelle, belasten. Antioxidantien stellten das Überleben der Zellen teilweise wieder her, was bestätigt, dass dieser oxidative Ausbruch ein zentraler Treiber der Wirkungen des Medikaments ist.
Drei Todespfade statt einem
Statt sich auf einen einzelnen Abtötungsmechanismus zu stützen, aktiviert PAMT‑001 mehrere regulierte Todesprogramme parallel. Es löst die klassische intrinsische Apoptose aus: Mitochondrien setzen Cytochrom c frei, Ausführungsenzyme namens Caspasen werden gespalten und aktiviert, und Zellmembranen zeigen charakteristische Blebbing‑Phänomene; Pan‑Caspase‑Inhibitoren dämpfen diesen Effekt deutlich. Gleichzeitig induziert das Medikament starke Autophagie, bei der Doppelmembranvesikel beschädigte Mitochondrien und andere Zellbestandteile einschließen. Die Blockade dieses Prozesses durch Autophagie‑Inhibitoren oder das Ausschalten eines Schlüsselgens der Autophagie reduziert den Zelltod und senkt Stresssignale, was darauf hinweist, dass Autophagie in diesem Kontext überaktiviert und schädlich statt schützend wird. Schließlich treibt PAMT‑001 eine feurige Todesform namens Pyroptose voran: Poren öffnen sich in der Zellmembran, Inhalte treten aus, und ein Protein namens Gasdermin E wird in ein porebildendes Fragment gespalten. Zusammen vereinen sich Pyroptose, Apoptose und autophagischer Zelltod zu dem, was die Autoren „PAAoptose“ nennen — ein koordiniertes, multipfadiges Versagen der Krebszelle.

Hoffnung für schwer behandelbare Krebserkrankungen
PAMT‑001 wirkte nicht nur in Zellkulturen. In Mausmodellen von Darmkrebs und akuter myeloischer Leukämie verlangsamte das Medikament das Tumorwachstum, reduzierte Leukämiezellen im Knochenmark und senkte die gesamte Tumorlast, gemessen per Bildgebung, und das alles ohne offensichtliche Beeinträchtigung von Körpergewicht oder normalen Zellen. Proben von Patienten mit akuter myeloischer Leukämie waren im Allgemeinen empfindlicher gegenüber PAMT‑001 als gesunde Blutzellen, und Leukämien mit Mutationen im Gen NPM1 — oft assoziiert mit hoher mitochondrialer Aktivität — waren besonders verwundbar. Das Medikament tötete außerdem Leukämiezellen, die gegen Cytarabin resistent waren, und Lungenkrebszellen, die gegen ein EGFR‑gerichtetes Mittel resistent waren, was darauf hindeutet, dass sein breiter Angriff auf den mitochondrialen Stoffwechsel und der multipfade Zelltod helfen könnten, Therapieresistenzen zu überwinden.
Was das für die zukünftige Krebsbehandlung bedeutet
Diese Arbeit stellt PAMT‑001 als Prototyp einer neuen Wirkstoffklasse vor, die einen energiesteuernden Schalter angreift und Tumoren in PAAoptose zwingt — eine Mischung aus drei zerstörerischen Todesprogrammen. Indem sie die Energieversorgung untergraben und gleichzeitig mehrere lebenswichtige Systeme belasten, könnten solche Wirkstoffe den Krebszellen weniger Spielraum zur Entwicklung von Resistenzen lassen. Obwohl PAMT‑001 selbst noch weitere Prüfungen zu Sicherheit, Dosierung und Langzeiteffekten benötigt, weist die Studie auf Therapien hin, die die einzigartigen Energieanforderungen von Krebszellen ausnutzen und multipfade Zelltodsmechanismen verwenden, um hartnäckige Tumoren am Wiederauftreten zu hindern.
Zitation: Seo, W., Heo, Y., Tran, K.V. et al. A novel PAAoptosis-inducing ERRα-targeting compound for combating hematopoietic and solid cancers. Cell Death Discov. 12, 188 (2026). https://doi.org/10.1038/s41420-026-03010-4
Schlüsselwörter: Krebsstoffwechsel, Mitochondrien, ERR alpha, Arzneimittelresistenz, Zelltodwege