Clear Sky Science · zh
PMEPA1 调节 YAP1 核转位以破坏 EMT 亚型并促进胆道癌转移
这项研究为何重要
胆道癌是发生在胆管和胆囊的少见但致命的癌症,现有治疗选择有限且易发生远处转移。本研究利用前沿的单细胞分析揭示了某些肿瘤细胞如何改变身份以变得更具移动性和侵袭性,并锁定了一个有助于推动这一转换的特定分子,该分子可由已有的化疗药物作为潜在靶点。
逐细胞深入观察胆管肿瘤
研究者没有对整个肿瘤取平均信号,而是检查了来自47例人类胆道癌和正常组织样本的近16万个单细胞。通过读取每个细胞的RNA,他们构建了肿瘤生态系统的详细地图,涵盖免疫细胞、支持细胞、血管细胞,尤其是产生癌变的肿瘤上皮细胞。他们发现肿瘤组织中的上皮细胞远多于正常组织,且这些上皮细胞可分为五个不同群体,每一群体各司其职,例如快速增殖、改变的能量代谢、炎症或脂质代谢等。
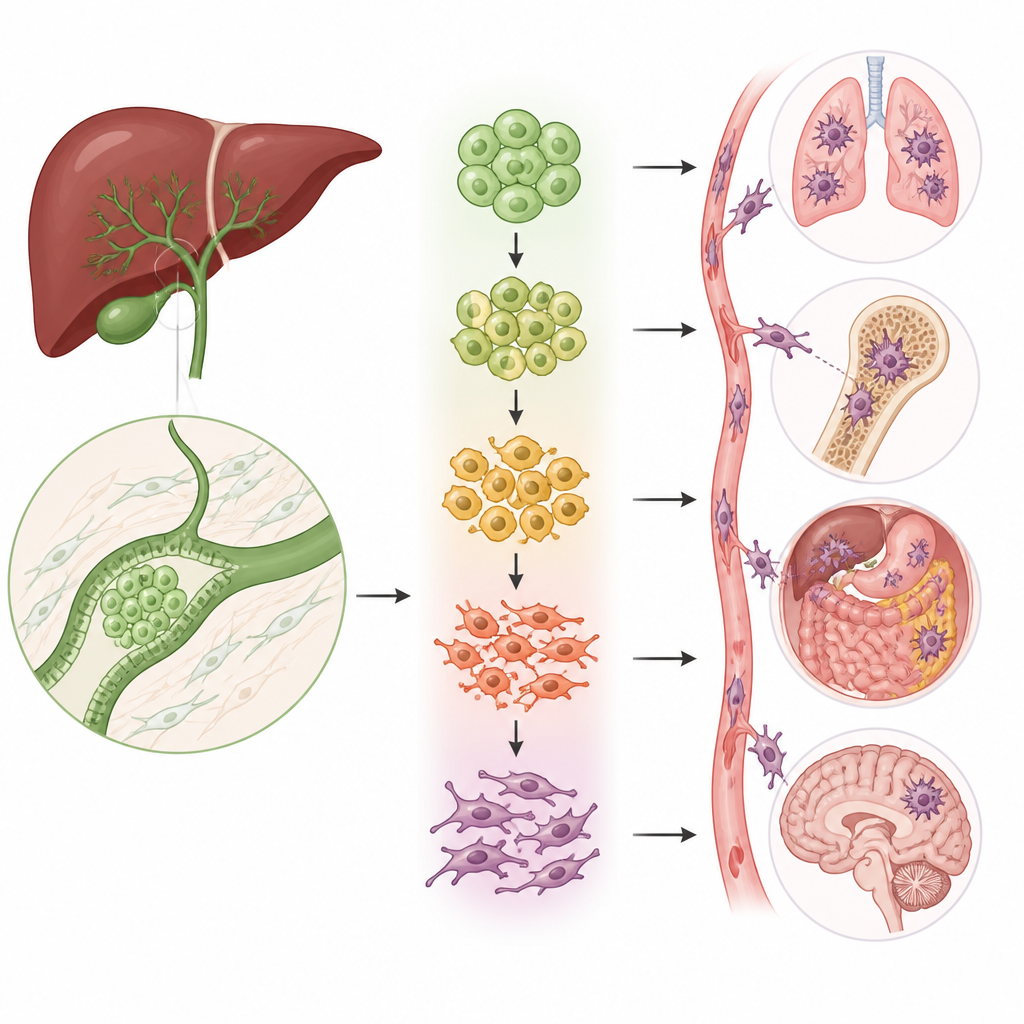
驱动转移的变形细胞
癌症扩散的一个关键过程是上皮—间质转化(EMT),在此过程中紧密、有序的细胞松散结合、改变形态并开始移动。团队发现五类上皮细胞中有两类显著富集了这一转化程序。通过多种分析方法,他们表明这些群体的细胞沿着一条从类正常、紧密连接的细胞走向高度可移动、侵袭性细胞的路径分布。随着细胞沿此路径进展,典型的静止细胞标志消失,而移动性和纤维化细胞的标志上升,将这些亚群直接与肿瘤侵袭和转移的能力联系起来。
作为侵袭性行为中心开关的 PMEPA1
为了解哪些基因真正驱动这一变化,科学家们汇编了一组针对胆道癌的51个转化相关基因,并用它们对单细胞和患者肿瘤进行评分。肿瘤评分较高的患者预后较差,将细胞层面的程序与临床结局联系起来。在富集于转化阳性细胞的基因中,名为 PMEPA1 的基因尤为突出。高 PMEPA1 水平与较差的预后相关,并且在淋巴结转移灶中高于原发胆管肿瘤。当研究者在胆管癌细胞系中降低 PMEPA1 表达时,细胞生长变慢、集落形成减少,迁移和穿膜侵袭能力显著下降,且在小鼠肺部种植肿瘤的能力降低。增强 PMEPA1 则产生相反效果。
PMEPA1 如何重编细胞内信号
进一步研究将 PMEPA1 与以蛋白 YAP1 为中心的已知生长控制通路相连接。在健康组织中,一套安全回路将 YAP1 多数保持在细胞核之外,限制其激活生长和侵袭基因的能力。研究者发现 PMEPA1 有助于削弱这套安全回路,使更多 YAP1 进入细胞核。当沉默 PMEPA1 时,上游激酶活性增强,YAP1 被更多修饰,并被困留在细胞质中而非进入细胞核。该转变伴随更静止、低侵袭性的表型。一种阻断安全回路激酶的化学抑制剂可逆转 PMEPA1 缺失引起的许多变化,证实 PMEPA1 通过引导 YAP1 进入细胞核来促进转化程序。
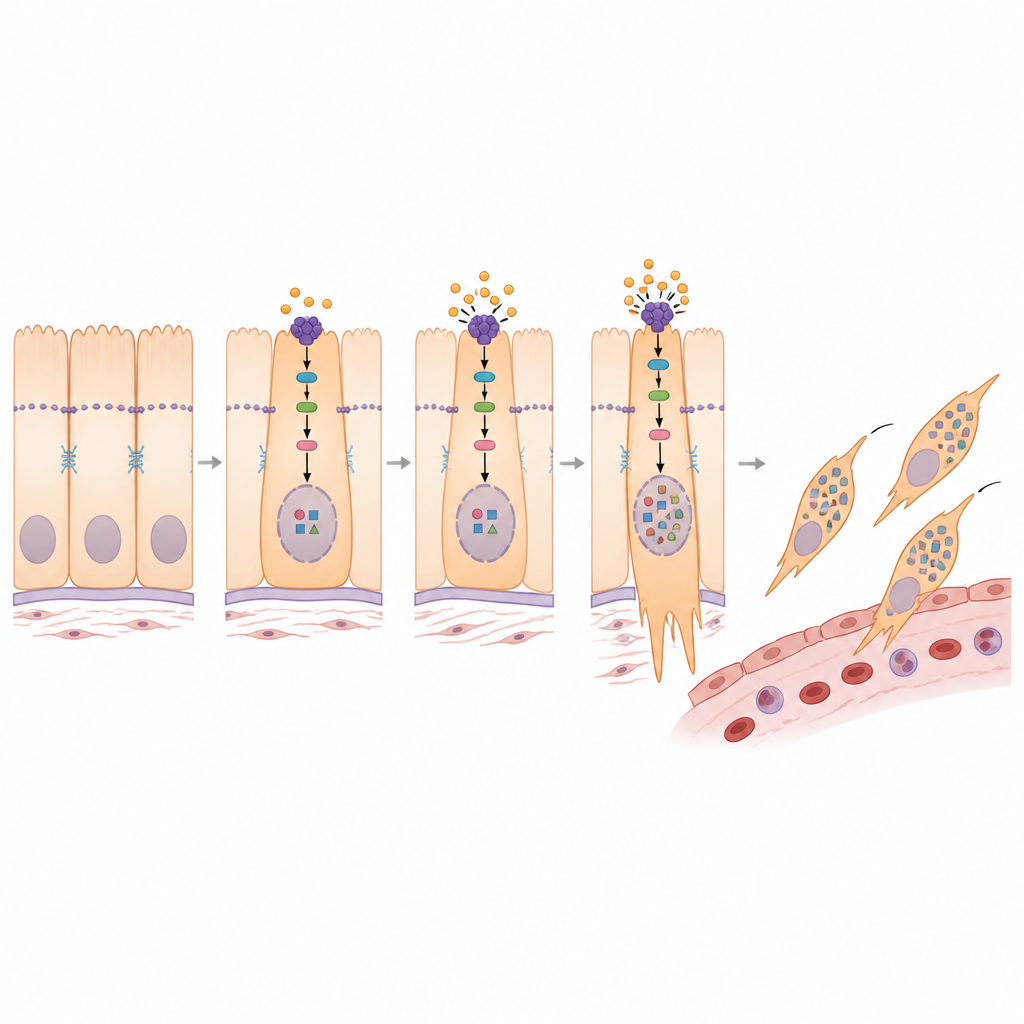
一种可能减缓扩散的药物
由于转化程序与治疗耐药密切相关,团队接着探讨是否有现成药物可选择性攻击这些侵袭性细胞。通过将药物反应数据库与他们的基因特征结合,发现包括 SN-38(伊立替康的活性形式)在内的若干化疗药物是候选者。在细胞实验中,SN-38 降低了移动性细胞状态的标志物,减少了细胞迁移和侵袭能力,并降低了 PMEPA1 和 YAP1 水平。进一步工作表明,SN-38 可能干扰一种名为 FOS 的转录因子,FOS 通常会提升 PMEPA1 的表达。在由 PMEPA1 过表达驱动的小鼠肺转移模型中,SN-38 治疗减少了转移负担并降低了肿瘤沉积中的 PMEPA1 水平。
对患者的意义
简而言之,这项研究表明特定蛋白 PMEPA1 像一个主开关一样,帮助胆管癌细胞松散结合、远迁并在新器官定植。其机制是释放另一蛋白 YAP1,使其进入细胞核并激活有利于侵袭的基因。由于携带更强该程序的肿瘤预后更差,PMEPA1 及其相关通路可作为预警性标志和治疗靶点。发现已用于其他癌症的 SN-38 能抑制该开关并在模型中减缓转移,提示通过优化或联合此类疗法,未来可能为胆道癌患者提供更精确、更有效的治疗选择。
引用: Xu, W., Ma, C., Li, P. et al. PMEPA1 modulates YAP1 nuclear translocation to disrupt EMT subtypes and promote metastasis in Biliary tract cancer. Cell Death Dis 17, 449 (2026). https://doi.org/10.1038/s41419-026-08684-3
关键词: 胆道癌, 上皮-间质转化, PMEPA1, YAP1 信号通路, SN-38