Clear Sky Science · it
PMEPA1 regola la traslocazione nucleare di YAP1 per alterare i sottotipi di EMT e favorire le metastasi nel tumore delle vie biliari
Perché questa ricerca è importante
Il tumore delle vie biliari è una neoplasia rara ma letale dei dotti biliari e della cistifellea, con poche opzioni terapeutiche efficaci e un’elevata probabilità di diffusione a organi distanti. Questo studio utilizza analisi a singola cellula all’avanguardia per scoprire come certe cellule tumorali cambino identità diventando più mobili e invasive, e individua una molecola specifica che guida questo cambiamento e potrebbe essere bersagliata da un farmaco chemioterapico già disponibile.
Esaminare i tumori delle vie biliari cellula per cellula
Invece di mediare i segnali sull’insieme del tumore, i ricercatori hanno analizzato quasi 160.000 cellule individuali provenienti da 47 campioni umani di tumore delle vie biliari e tessuto normale. Leggendo l’RNA di ciascuna cellula, hanno costruito una mappa dettagliata dell’ecosistema tumorale, includendo cellule immunitarie, cellule di supporto, cellule endoteliali e, in particolare, le cellule epiteliali tumorali da cui origina il cancro. Hanno constatato che i tessuti tumorali contenevano molte più cellule epiteliali rispetto al tessuto normale e che queste potevano essere suddivise in cinque gruppi distinti, ciascuno con un ruolo specifico, come rapida proliferazione, metabolismo energetico alterato, infiammazione o processi lipidici.
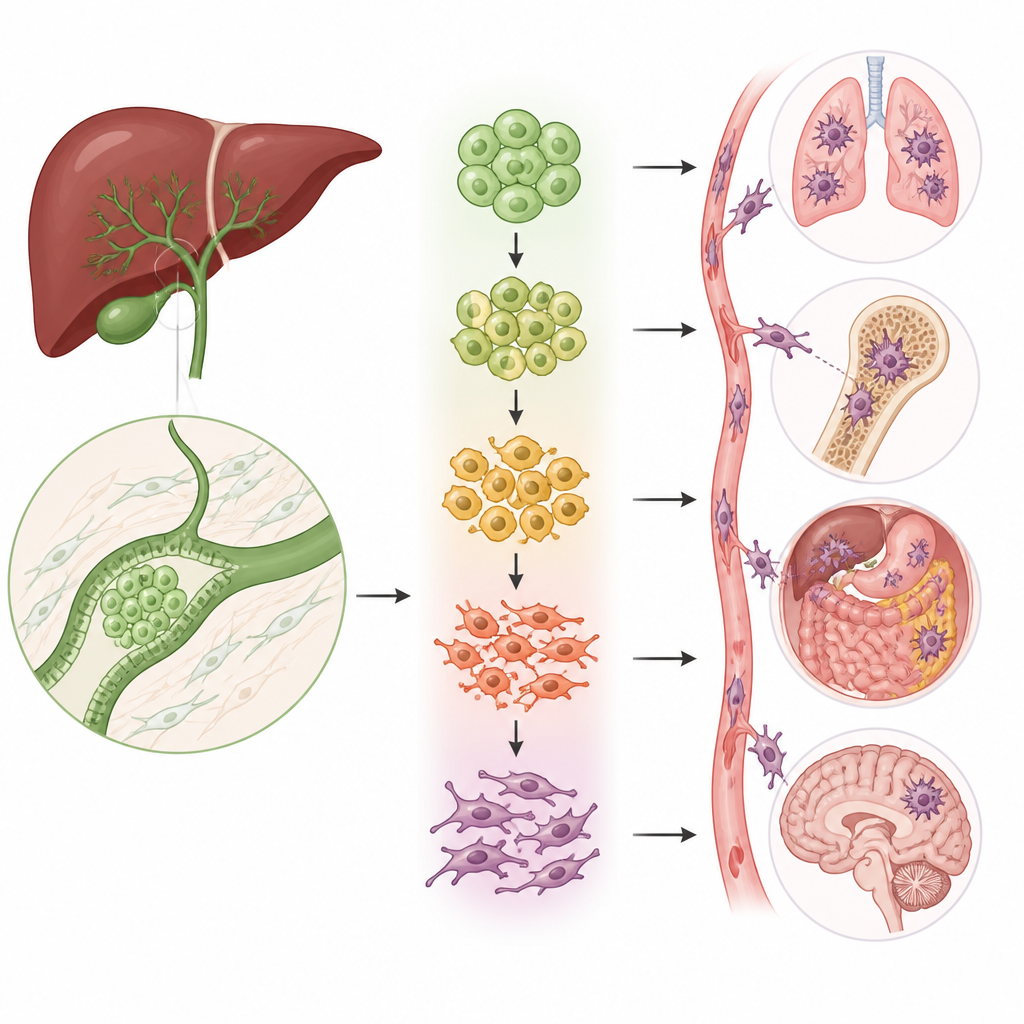
Le cellule mutaforma che guidano la diffusione
Un processo chiave nella diffusione del cancro è la transizione epitelio-mesenchimale (EMT), nella quale cellule compatte e ordinate allentano i loro legami, cambiano forma e cominciano a muoversi. Il gruppo ha scoperto che due dei cinque gruppi epiteliali erano fortemente arricchiti per questo programma di transizione. Tramite diversi tipi di analisi, hanno mostrato che le cellule in questi gruppi si collocano lungo un percorso che va da uno stato simile al normale, con cellule strettamente connesse, verso cellule altamente mobili e invasive. Man mano che le cellule progrediscono lungo questo percorso, i marcatori classici delle cellule stazionarie diminuiscono mentre aumentano i marcatori delle cellule mobili e fibrotiche, collegando questi sottogruppi direttamente alla capacità del tumore di invadere e metastatizzare.
PMEPA1 come interruttore centrale del comportamento aggressivo
Per capire quali geni guidano effettivamente questo cambiamento, gli scienziati hanno assemblato un insieme di 51 geni correlati alla transizione specifici per il tumore delle vie biliari e li hanno usati per attribuire un punteggio sia alle singole cellule sia ai tumori dei pazienti. I pazienti i cui tumori avevano punteggi più elevati mostravano una sopravvivenza peggiore, collegando il programma a livello cellulare all’esito clinico. Tra i geni arricchiti nelle cellule positive per la transizione, uno chiamato PMEPA1 è emerso come particolarmente rilevante. Livelli elevati di PMEPA1 erano associati a prognosi peggiore e risultavano più alti nelle metastasi linfonodali rispetto ai tumori primari delle vie biliari. Quando i ricercatori ridussero l’espressione di PMEPA1 in linee cellulari di carcinoma delle vie biliari, le cellule crebbero più lentamente, formarono meno colonie e persero gran parte della capacità di muoversi e invadere membrane artificiali e di impiantare tumori nei polmoni dei topi. L’aumento di PMEPA1 aveva l’effetto opposto.
Come PMEPA1 riconfigura la segnalazione intracellulare
Approfondendo, lo studio ha collegato PMEPA1 a una via di controllo della crescita nota centrata su una proteina chiamata YAP1. Nei tessuti sani, un circuito di sicurezza mantiene YAP1 in gran parte al di fuori del nucleo cellulare, limitandone la capacità di attivare geni di crescita e invasione. I ricercatori hanno scoperto che PMEPA1 contribuisce ad indebolire questo circuito di sicurezza, permettendo a più YAP1 di entrare nel nucleo. Quando PMEPA1 veniva silenziata, gli enzimi a monte diventavano più attivi, YAP1 risultava maggiormente modificato e rimaneva intrappolato nel citoplasma invece che nel nucleo. Questo cambiamento era accompagnato da un profilo più stazionario e meno invasivo. Un composto chimico che blocca gli enzimi del circuito di sicurezza invertiva molti degli effetti causati dalla perdita di PMEPA1, confermando che PMEPA1 promuove il programma di transizione indirizzando YAP1 verso il nucleo.
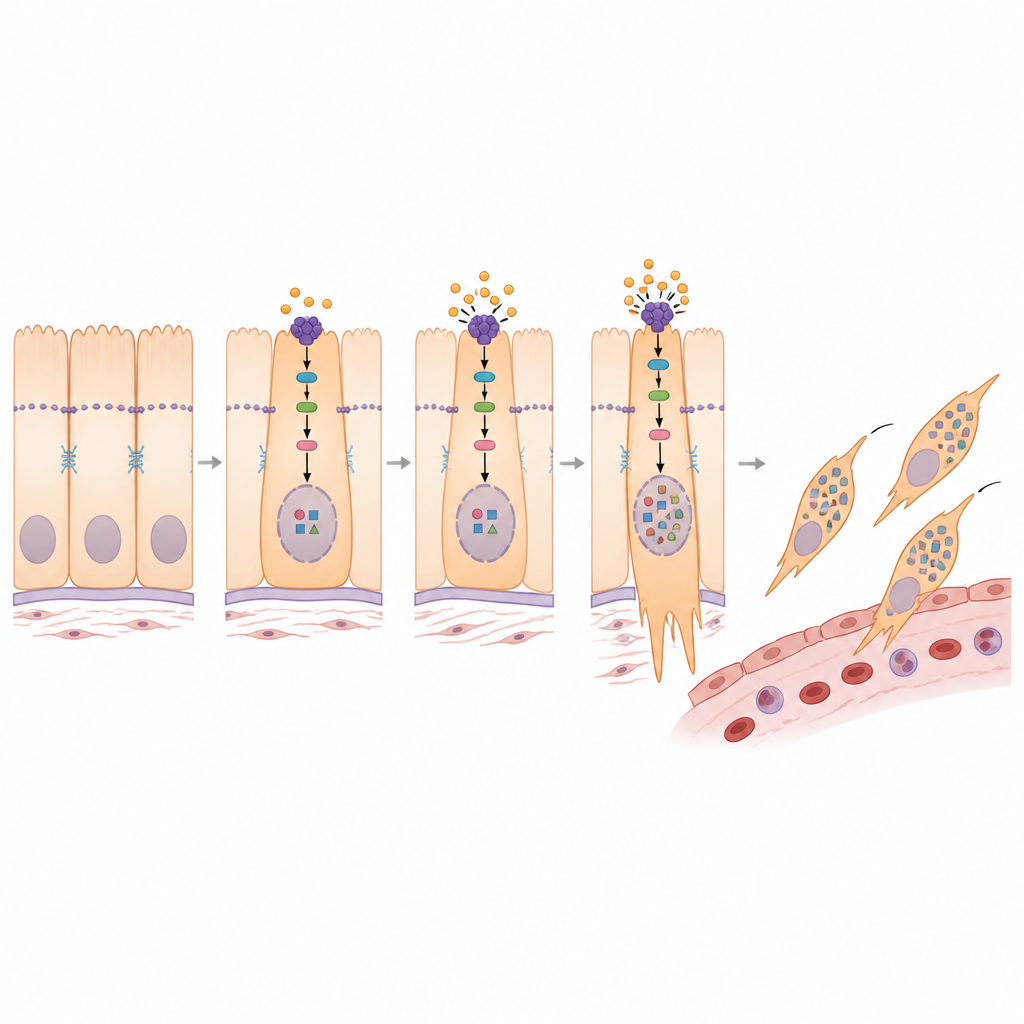
Un possibile farmaco per rallentare la diffusione
Poiché il programma di transizione è strettamente legato alla resistenza ai trattamenti, il team ha poi chiesto se farmaci esistenti potessero colpire selettivamente queste cellule aggressive. Combinando banche dati di risposta ai farmaci con le loro firme geniche, hanno segnalato diversi agenti chemioterapici, incluso SN-38, la forma attiva dell’irinotecan, come candidati. In esperimenti su cellule, SN-38 ridusse i marcatori dello stato cellulare mobile, diminuì la capacità di migrazione e invasione delle cellule e abbassò sia i livelli di PMEPA1 sia di YAP1. Ulteriori esperimenti suggerirono che SN-38 interferisce con un fattore di trascrizione chiamato FOS che normalmente aumenta la produzione di PMEPA1. In modelli murini di metastasi polmonare indotta dalla sovraespressione di PMEPA1, il trattamento con SN-38 ridusse il carico metastatico e i livelli di PMEPA1 nei depositi tumorali.
Cosa significa per i pazienti
In termini semplici, questo studio mostra che una proteina specifica, PMEPA1, funziona come un interruttore maestro che aiuta le cellule del tumore delle vie biliari ad allentarsi, spostarsi e colonizzare nuovi organi. Lo fa liberando un’altra proteina, YAP1, permettendole di entrare nel nucleo e attivare geni che favoriscono l’invasione. Poiché i tumori con una versione più attiva di questo programma hanno esiti peggiori, PMEPA1 e i suoi partner potrebbero servire da marcatori prognostici e bersagli terapeutici. Il fatto che SN-38, già impiegato in altri tumori, possa attenuare questo interruttore e rallentare le metastasi nei modelli apre la possibilità che ottimizzare o combinare tali terapie possa un giorno offrire opzioni più mirate ed efficaci per le persone con tumore delle vie biliari.
Citazione: Xu, W., Ma, C., Li, P. et al. PMEPA1 modulates YAP1 nuclear translocation to disrupt EMT subtypes and promote metastasis in Biliary tract cancer. Cell Death Dis 17, 449 (2026). https://doi.org/10.1038/s41419-026-08684-3
Parole chiave: tumore delle vie biliari, transizione epitelio-mesenchimale, PMEPA1, segnalazione YAP1, SN-38