Clear Sky Science · pl
PMEPA1 moduluje przemieszczanie się YAP1 do jądra komórkowego, zaburzając podtypy EMT i wspierając przerzuty w raku dróg żółciowych
Dlaczego te badania są istotne
Rak dróg żółciowych to rzadki, ale śmiertelny nowotwór przewodów żółciowych i pęcherzyka żółciowego, z niewieloma skutecznymi opcjami leczenia i wysokim ryzykiem rozprzestrzeniania się do odległych narządów. W tym badaniu zastosowano nowoczesne metody analizy pojedynczych komórek, aby odsłonić, jak niektóre komórki nowotworowe zmieniają swoją tożsamość, stając się bardziej ruchome i inwazyjne, oraz wskazano konkretną cząsteczkę, która napędza tę przemianę i może być celem istniejącego leku chemioterapeutycznego.
Szczegółowe badanie guzów dróg żółciowych komórka po komórce
Zamiast uśredniać sygnały po całych guzach, badacze przeanalizowali prawie 160 000 pojedynczych komórek pochodzących z 47 ludzkich próbek raka dróg żółciowych i tkanek normalnych. Odczytując RNA każdej komórki, zbudowali szczegółową mapę ekosystemu guza, obejmującą komórki odpornościowe, komórki podporowe, komórki naczyń krwionośnych i w szczególności komórki nabłonkowe nowotworu, które są źródłem raka. Stwierdzili, że tkanki guza zawierały znacznie więcej komórek nabłonkowych niż tkanki normalne oraz że te komórki nabłonkowe dały się podzielić na pięć odrębnych grup, z których każda pełniła inną funkcję, taką jak szybki wzrost, zmienione wykorzystanie energii, zapalenie czy przetwarzanie tłuszczów.
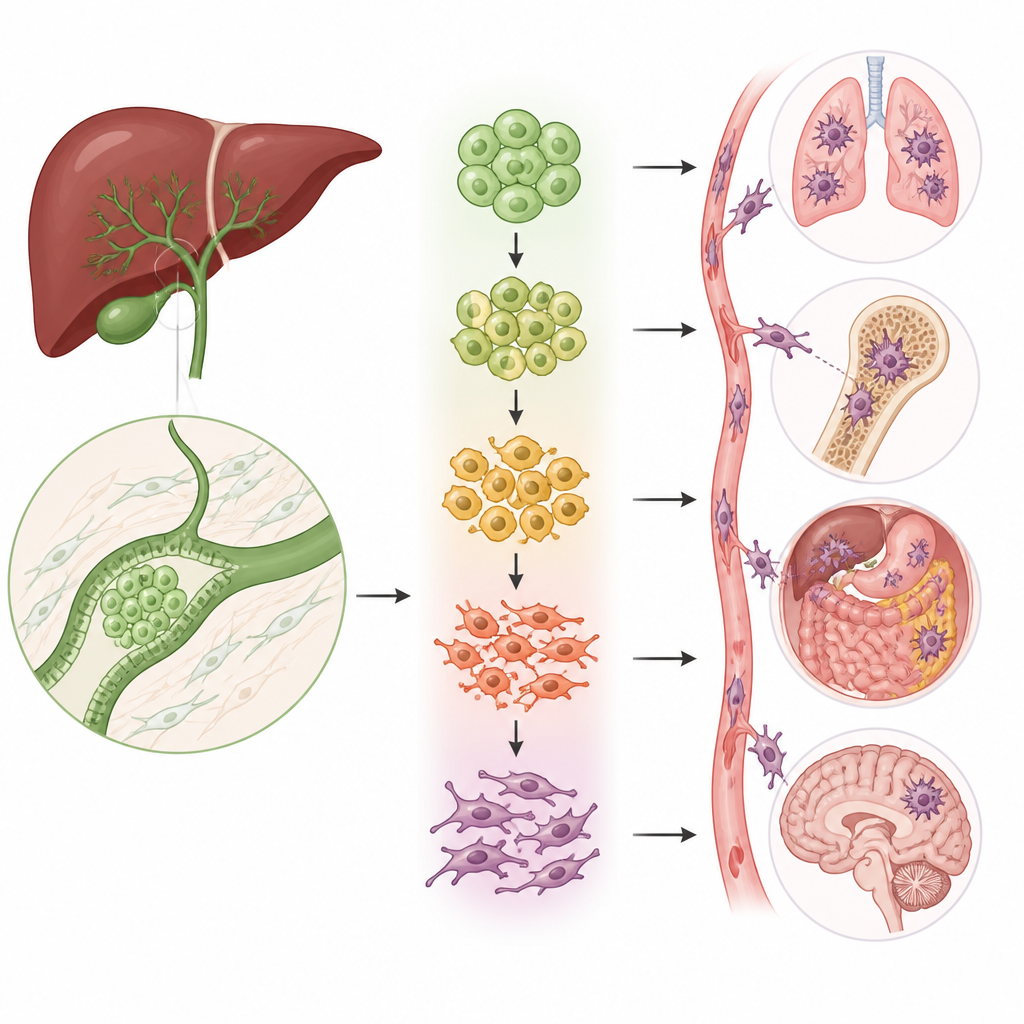
Komórki zmieniające kształt, które napędzają rozprzestrzenianie
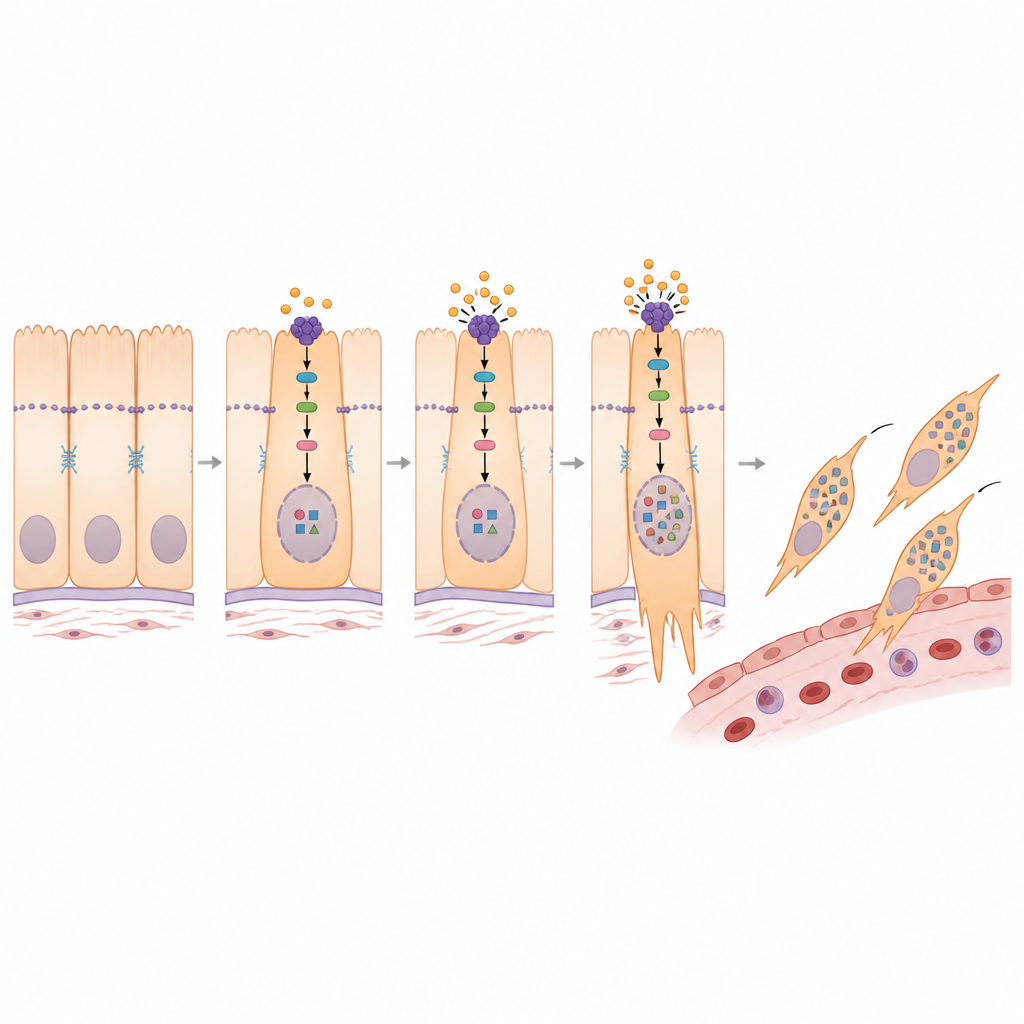
Kluczowym procesem w rozprzestrzenianiu się raka jest przejście nabłonkowo-mezenchymalne (EMT), podczas którego zwarte, uporządkowane komórki poluzowują połączenia, zmieniają kształt i zaczynają się poruszać. Zespół odkrył, że dwie z pięciu grup komórek nabłonkowych były silnie wzbogacone w program EMT. Przy użyciu kilku metod analizy wykazali, że komórki z tych grup leżą wzdłuż drogi od komórek przypominających normalne, ściśle połączone, w kierunku wysoko ruchomych, inwazyjnych komórek. W miarę jak komórki przesuwają się wzdłuż tej ścieżki, tradycyjne markery komórek osiadłych słabną, podczas gdy markery komórek ruchomych, włóknistych rosną, co łączy te podgrupy bezpośrednio ze zdolnością guza do inwazji i przerzutowania.
PMEPA1 jako centralny przełącznik agresywnego zachowania
Aby zrozumieć, które geny faktycznie napędzają tę zmianę, naukowcy stworzyli zestaw 51 genów związanych z przejściem, specyficznych dla raka dróg żółciowych, i użyli ich do oceniania pojedynczych komórek oraz guzów pacjentów. Pacjenci, których guzy miały wyższe wyniki, mieli gorsze przeżycie, co powiązało program na poziomie komórkowym z wynikiem klinicznym. Spośród genów wzbogaconych w komórkach pozytywnych w kierunku przejścia wyróżniał się gen PMEPA1. Wysokie poziomy PMEPA1 wiązały się z gorszym rokowaniem i były wyższe w przerzutach do węzłów chłonnych niż w pierwotnych guzach dróg żółciowych. Gdy badacze zmniejszyli poziom PMEPA1 w liniach komórkowych raka dróg żółciowych, komórki rosnęły wolniej, tworzyły mniej kolonii i traciły dużą część zdolności do ruchu i inwazji przez sztuczne membrany oraz do zasiedlania płuc myszy. Zwiększenie ekspresji PMEPA1 dawało efekt odwrotny.
Jak PMEPA1 przeprogramowuje sygnały wewnątrz komórki
Zagłębiając się dalej, badanie powiązało PMEPA1 ze znanym szlakiem kontroli wzrostu skupionym wokół białka YAP1. W zdrowych tkankach mechanizm zabezpieczający utrzymuje YAP1 w przeważającej mierze poza jądrem komórkowym, ograniczając jego zdolność do włączania genów wzrostu i inwazji. Badacze odkryli, że PMEPA1 pomaga osłabić ten mechanizm, pozwalając większej ilości YAP1 dostać się do jądra. Gdy PMEPA1 został wyciszony, enzymy działające powyżej stały się bardziej aktywne, YAP1 był silniej modyfikowany i pozostawał uwięziony w cytoplazmie zamiast w jądrze. Ta zmiana towarzyszyła bardziej osiadłemu, mniej inwazyjnemu profilowi. Związek chemiczny blokujący te enzymy zabezpieczające odwrócił wiele zmian spowodowanych utratą PMEPA1, potwierdzając, że PMEPA1 promuje program przejścia przez kierowanie YAP1 do jądra.
Potencjalny lek na spowolnienie rozprzestrzeniania
Ponieważ program przejścia jest ściśle związany z opornością na leczenie, zespół zapytał następnie, czy istniejące leki mogą selektywnie trafić te agresywne komórki. Łącząc bazy danych reakcji na leki z ich sygnaturami genowymi, wskazali kilka środków chemioterapeutycznych, w tym SN-38, aktywną formę irinotekanu, jako kandydatów. W eksperymentach komórkowych SN-38 zmniejszał markery stanu komórek ruchomych, ograniczał zdolność komórek do migracji i inwazji oraz obniżał poziomy zarówno PMEPA1, jak i YAP1. Dalsze badania sugerowały, że SN-38 zakłóca czynnik transkrypcyjny FOS, który zwykle zwiększa produkcję PMEPA1. W modelach mysich przerzutów do płuc napędzanych nadekspresją PMEPA1, leczenie SN-38 zmniejszyło obciążenie przerzutowe i poziomy PMEPA1 w ogniskach nowotworowych.
Co to oznacza dla pacjentów
Mówiąc wprost, to badanie pokazuje, że konkretne białko, PMEPA1, działa jak wyłącznik główny, który pomaga komórkom raka dróg żółciowych poluzować więzi, ruszyć się i skolonizować nowe narządy. Robi to, uwalniając inne białko, YAP1, aby mogło wejść do jądra i aktywować geny sprzyjające inwazji. Ponieważ guzy z silniejszą wersją tego programu mają gorsze rokowanie, PMEPA1 i jego partnerzy mogą służyć jako markery ostrzegawcze i cele terapeutyczne. Odkrycie, że SN-38, już stosowany w innych nowotworach, może stłumić ten przełącznik i spowolnić przerzutowanie w modelach, sugeruje, że udoskonalenie lub łączenie takich terapii mogłoby kiedyś zaoferować bardziej precyzyjne i skuteczne opcje dla osób z rakiem dróg żółciowych.
Cytowanie: Xu, W., Ma, C., Li, P. et al. PMEPA1 modulates YAP1 nuclear translocation to disrupt EMT subtypes and promote metastasis in Biliary tract cancer. Cell Death Dis 17, 449 (2026). https://doi.org/10.1038/s41419-026-08684-3
Słowa kluczowe: rak dróg żółciowych, przejście nabłonkowo-mezenchymalne, PMEPA1, sygnalizacja YAP1, SN-38