Clear Sky Science · fr
PMEPA1 module la translocation nucléaire de YAP1 pour perturber les sous-types d’EMT et favoriser les métastases dans le cancer des voies biliaires
Pourquoi cette recherche est importante
Le cancer des voies biliaires est un cancer rare mais mortel des canaux biliaires et de la vésicule biliaire, avec peu d’options thérapeutiques efficaces et une forte propension à se propager à des organes distants. Cette étude utilise des analyses de pointe en cellule unique pour révéler comment certains cellules tumorales changent d’identité pour devenir plus mobiles et invasives, et elle identifie une molécule spécifique qui favorise ce basculement et pourrait être ciblée par un médicament chimiothérapeutique existant.
Examiner de près les tumeurs des voies biliaires une cellule à la fois
Plutôt que de moyenniser les signaux sur l’ensemble des tumeurs, les chercheurs ont examiné près de 160 000 cellules individuelles issues de 47 échantillons humains de cancer des voies biliaires et de tissus normaux. En lisant l’ARN de chaque cellule, ils ont construit une carte détaillée de l’écosystème tumoral, incluant les cellules immunitaires, les cellules du stroma, les cellules vasculaires et, en particulier, les cellules épithéliales tumorales à l’origine du cancer. Ils ont constaté que les tissus tumoraux contenaient beaucoup plus de cellules épithéliales que les tissus normaux et que ces cellules épithéliales pouvaient être réparties en cinq groupes distincts, chacun avec une fonction propre, comme la croissance rapide, l’usage énergétique modifié, l’inflammation ou le métabolisme des lipides.
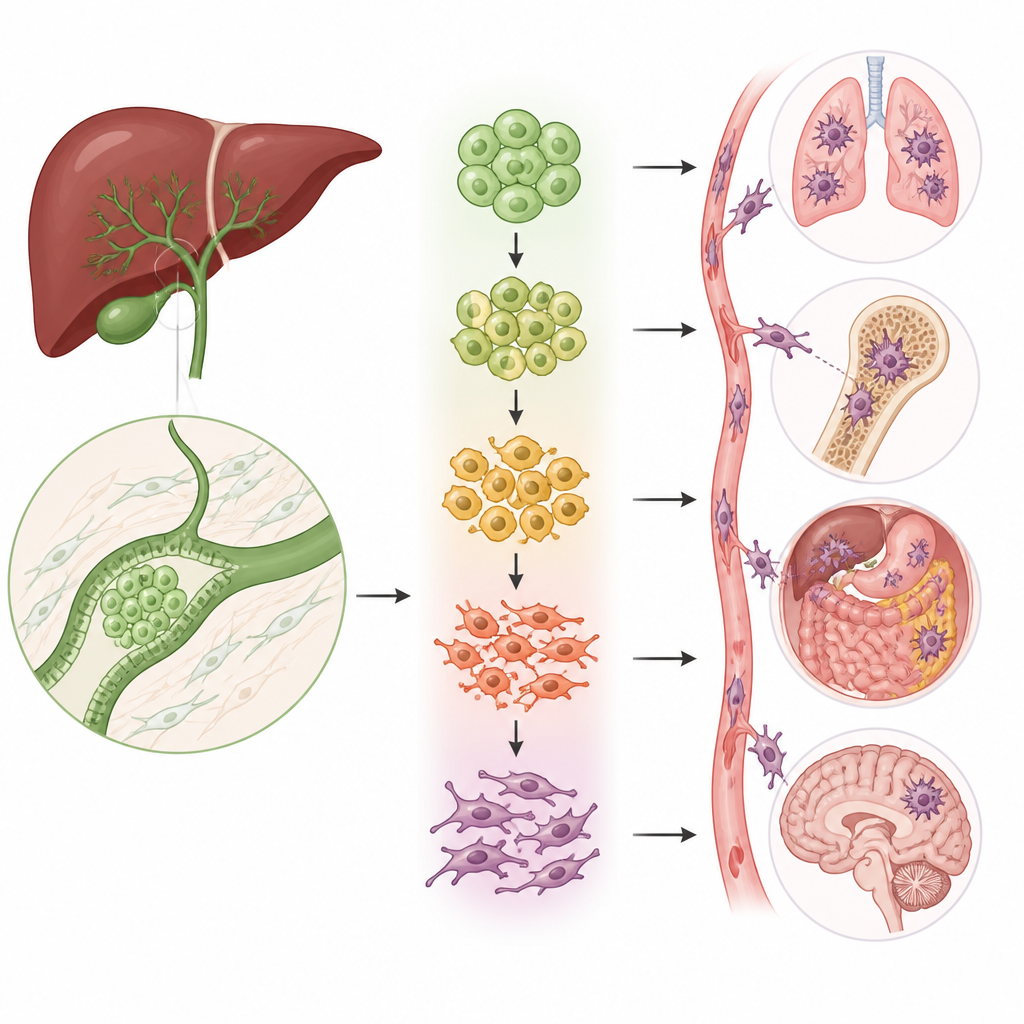
Les cellules métamorphes qui alimentent la dissémination
Un processus clé de la dissémination cancéreuse est la transition épithélio-mésenchymateuse (EMT), au cours de laquelle des cellules compactes et ordonnées relâchent leurs liaisons, changent de forme et commencent à migrer. L’équipe a découvert que deux des cinq groupes de cellules épithéliales étaient fortement enrichis en ce programme de transition. À l’aide de plusieurs types d’analyses, ils ont montré que les cellules de ces groupes se situent le long d’un parcours allant de cellules semblables au tissu normal, fortement connectées, vers des cellules hautement mobiles et invasives. Au fur et à mesure que les cellules progressent le long de ce trajet, les marqueurs classiques des cellules stationnaires diminuent tandis que les marqueurs des cellules mobiles et fibreuses augmentent, reliant directement ces sous-groupes à la capacité de la tumeur à envahir et à métastaser.
PMEPA1, un commutateur central du comportement agressif
Pour comprendre quels gènes conduisent réellement ce changement, les scientifiques ont assemblé un ensemble de 51 gènes liés à la transition spécifiques au cancer des voies biliaires et les ont utilisés pour scorer à la fois les cellules individuelles et les tumeurs de patients. Les patients dont les tumeurs présentaient des scores plus élevés avaient une survie inférieure, reliant le programme au niveau cellulaire au pronostic clinique. Parmi les gènes enrichis dans les cellules positives pour la transition, un nommé PMEPA1 s’est distingué. Des niveaux élevés de PMEPA1 étaient associés à un pire pronostic et étaient plus élevés dans les métastases ganglionnaires que dans les tumeurs primitives des voies biliaires. Lorsque les chercheurs ont réduit PMEPA1 dans des lignées cellulaires du cancer des voies biliaires, les cellules proliféraient plus lentement, formaient moins de colonies et perdaient une grande partie de leur capacité à migrer et à envahir à travers des membranes artificielles et à engendrer des tumeurs dans les poumons de la souris. L’augmentation de PMEPA1 produisait l’effet inverse.
Comment PMEPA1 reprogramme les signaux à l’intérieur de la cellule
En creusant davantage, l’étude a relié PMEPA1 à une voie de contrôle de la croissance bien connue centrée sur une protéine appelée YAP1. Dans les tissus sains, un circuit de sécurité maintient YAP1 principalement en dehors du noyau cellulaire, limitant sa capacité à activer les gènes de croissance et d’invasion. Les chercheurs ont trouvé que PMEPA1 contribue à affaiblir ce circuit de sécurité, permettant à plus de YAP1 d’entrer dans le noyau. Lorsque PMEPA1 était supprimé, les enzymes en amont devenaient plus actives, YAP1 était davantage modifié et restait confiné dans le cytoplasme au lieu du noyau. Ce basculement s’accompagnait d’un profil plus stationnaire et moins invasif. Un produit chimique qui bloque ces enzymes de sécurité a inversé bon nombre des changements causés par la perte de PMEPA1, confirmant que PMEPA1 favorise le programme de transition en orientant YAP1 vers le noyau.
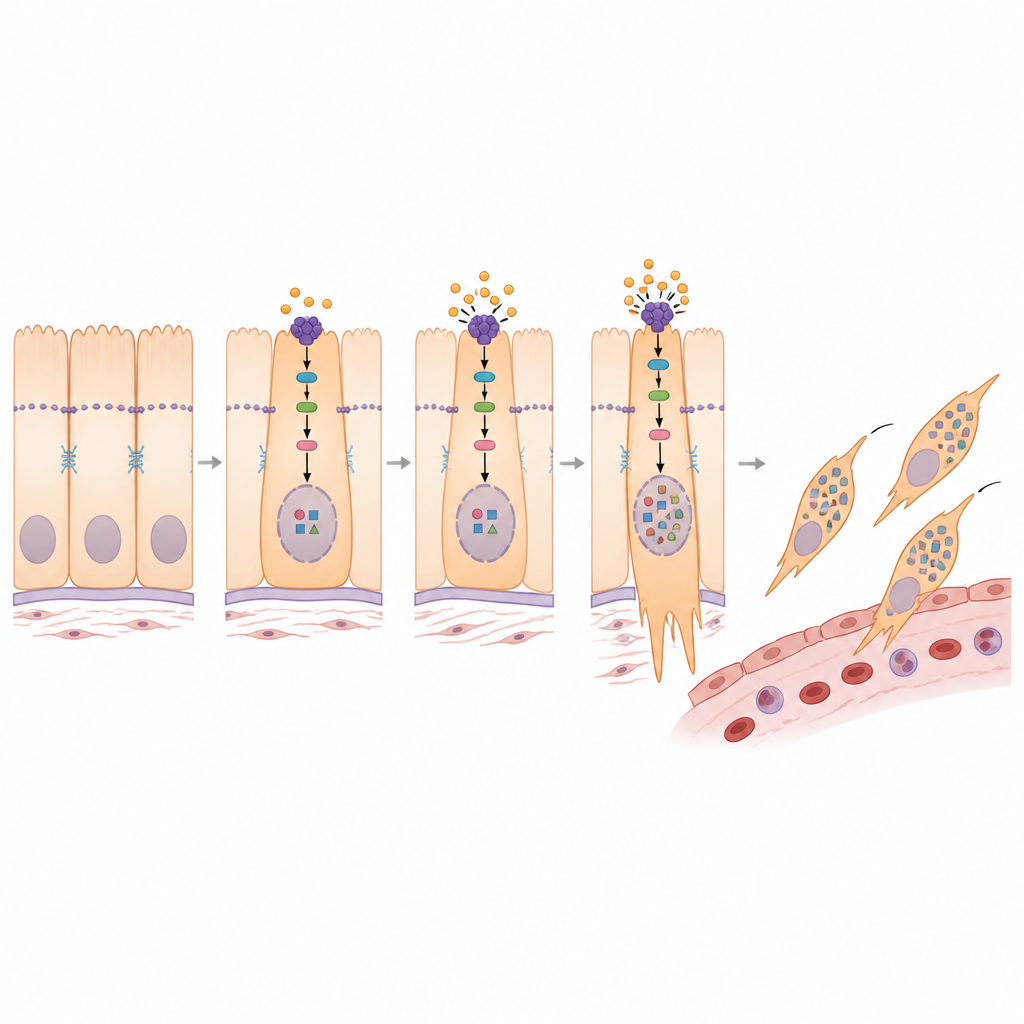
Un médicament potentiel pour ralentir la dissémination
Parce que le programme de transition est étroitement lié à la résistance au traitement, l’équipe a ensuite cherché si des médicaments existants pourraient cibler sélectivement ces cellules agressives. En combinant des bases de données de réponses médicamenteuses avec leurs signatures géniques, ils ont identifié plusieurs agents chimiothérapeutiques, dont le SN-38, la forme active de l’irinotécan, comme candidats. Dans des expériences cellulaires, le SN-38 a réduit les marqueurs de l’état cellulaire mobile, diminué la capacité des cellules à migrer et à envahir, et abaissé les niveaux de PMEPA1 et de YAP1. Des travaux supplémentaires ont suggéré que le SN-38 interfère avec un facteur de transcription nommé FOS qui stimule normalement la production de PMEPA1. Dans des modèles murins de métastases pulmonaires induites par la surexpression de PMEPA1, le traitement par SN-38 a réduit la charge métastatique et les niveaux de PMEPA1 dans les dépôts tumoraux.
Ce que cela signifie pour les patients
Concrètement, cette étude montre qu’une protéine spécifique, PMEPA1, agit comme un interrupteur maître qui aide les cellules du cancer des voies biliaires à se relâcher, à se déplacer et à coloniser de nouveaux organes. Elle le fait en libérant une autre protéine, YAP1, pour qu’elle entre dans le noyau et active des gènes favorisant l’invasion. Parce que les tumeurs présentant une version renforcée de ce programme ont un mauvais pronostic, PMEPA1 et ses partenaires pourraient servir de marqueurs d’alerte et de cibles thérapeutiques. La découverte que le SN-38, déjà utilisé dans d’autres cancers, peut atténuer cet interrupteur et ralentir les métastases dans des modèles soulève la possibilité que l’affinement ou la combinaison de telles thérapies puisse un jour offrir des options plus précises et efficaces pour les personnes atteintes d’un cancer des voies biliaires.
Citation: Xu, W., Ma, C., Li, P. et al. PMEPA1 modulates YAP1 nuclear translocation to disrupt EMT subtypes and promote metastasis in Biliary tract cancer. Cell Death Dis 17, 449 (2026). https://doi.org/10.1038/s41419-026-08684-3
Mots-clés: cancer des voies biliaires, transition épithélio-mésenchymateuse, PMEPA1, signalisation YAP1, SN-38