Clear Sky Science · ru
PMEPA1 модулирует ядерную транслокацию YAP1, нарушает подтипы EMT и способствует метастазированию при билиарном раке
Почему это исследование важно
Рак желчных протоков — редкая, но смертельно опасная опухоль желчных путей и желчного пузыря, с немногими эффективными вариантами лечения и высокой вероятностью распространения в отдалённые органы. В этом исследовании с использованием передового анализа на уровне одиночных клеток выявляют, как отдельные опухолевые клетки меняют свою идентичность, становясь более подвижными и инвазивными, и указывают на конкретную молекулу, которая управляет этим переключением и может стать мишенью для имеющегося химиотерапевтического препарата.
Изучая опухоли желчных протоков по одной клетке
Вместо усреднения сигналов по всей опухоли исследователи проанализировали почти 160 000 отдельных клеток из 47 образцов тканей человека — опухолевых и нормальных. Читая РНК каждой клетки, они построили подробную карту экосистемы опухоли, включая иммунные клетки, клетки поддержки, сосудистые клетки и особенно опухолевые эпителиальные клетки, дающие начало раку. Они обнаружили, что в опухолевых тканях было значительно больше эпителиальных клеток, чем в норме, и что эти эпителиальные клетки можно разделить на пять отдельных групп, каждая из которых выполняет свою функцию, например быстрое деление, изменённый метаболизм, воспалительные ответы или переработку липидов.
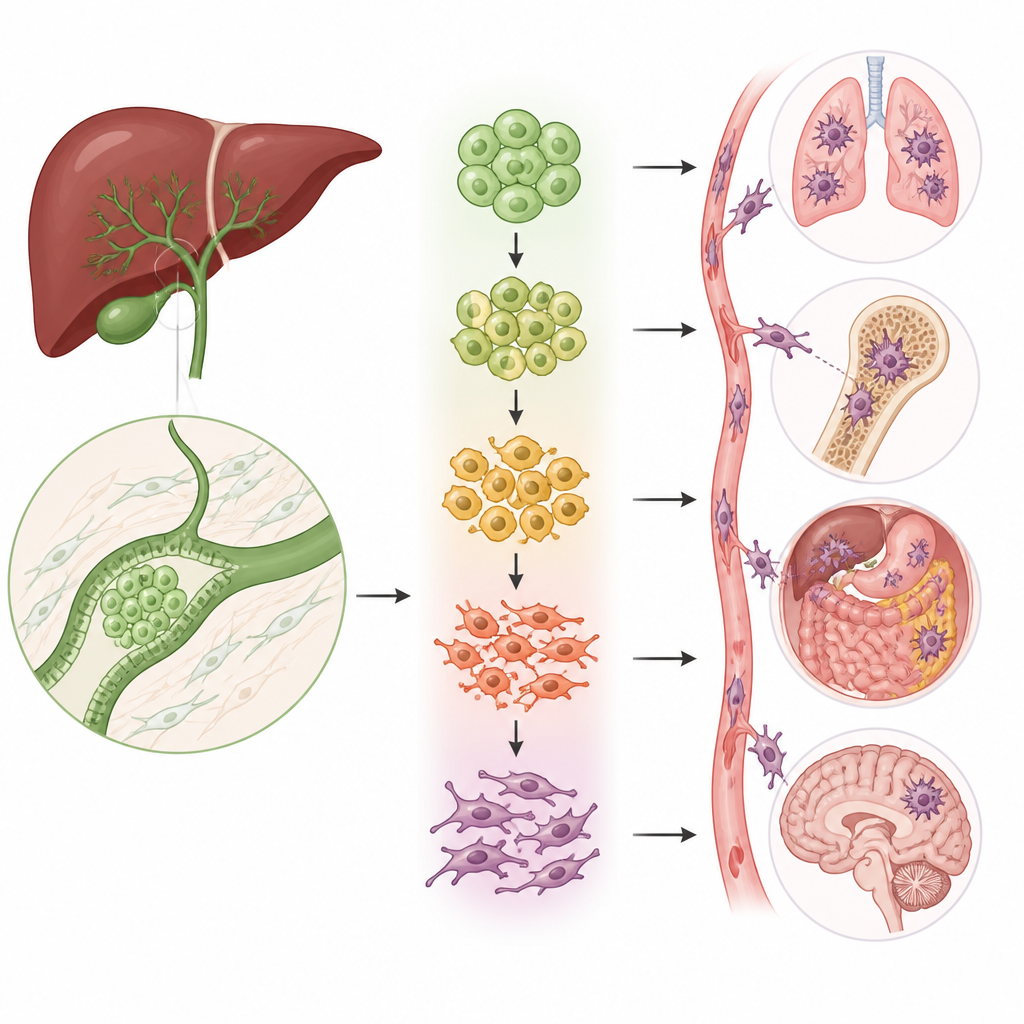
Клетки‑хамелеоны, которые приводят к распространению
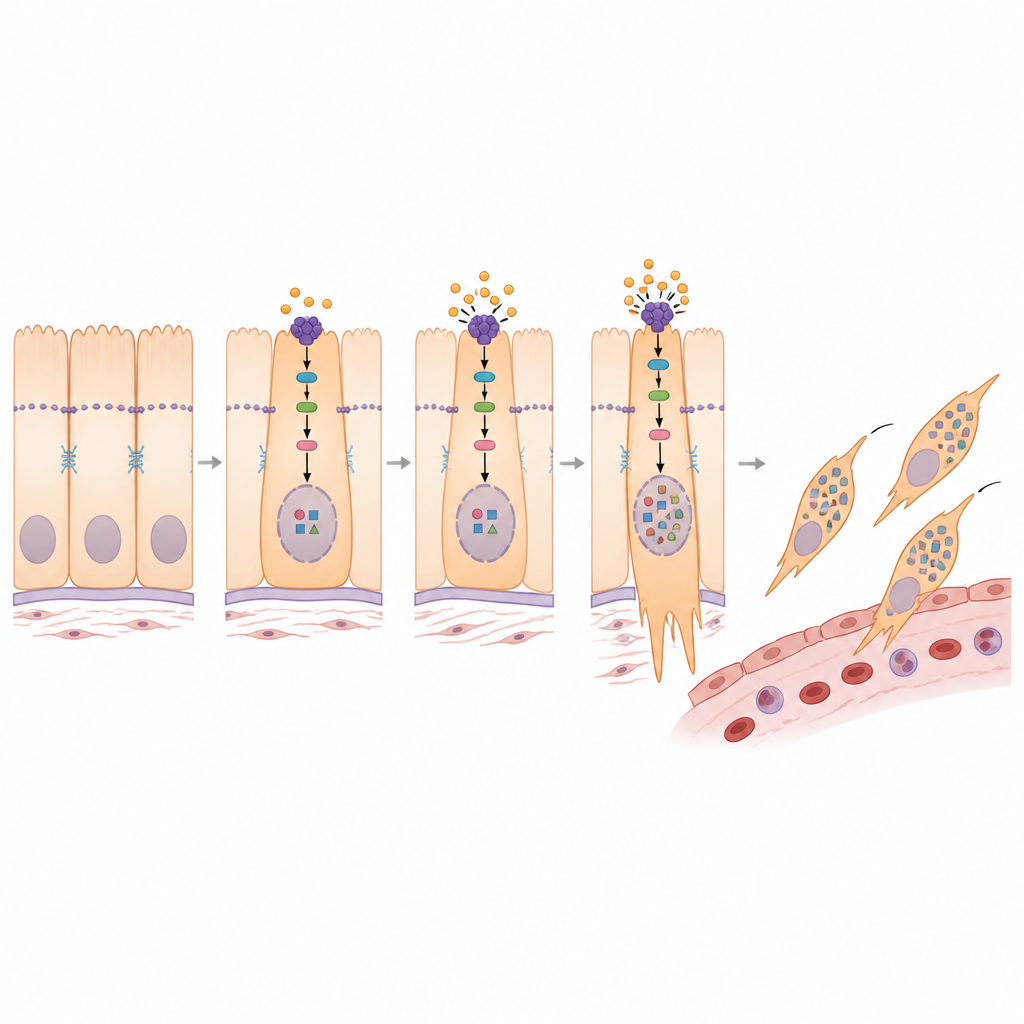
Ключевой процесс при распространении рака — эпителиально-мезенхимальный переход (EMT), при котором плотные, упорядоченные клетки ослабляют межклеточные связи, меняют форму и начинают перемещаться. Команда обнаружила, что две из пяти эпителиальных групп выражают программу перехода в значительной степени. С помощью нескольких типов анализа они показали, что клетки в этих группах располагаются вдоль траектории от нормоподобных, тесно связанных клеток к высокоподвижным, инвазивным клеткам. По мере продвижения по этой траектории классические маркёры неподвижных клеток угасают, а маркёры подвижных, фиброзных клеток усиливаются, напрямую связывая эти подгруппы с потенциалом опухоли к инвазии и метастазированию.
PMEPA1 как центральный переключатель агрессивного поведения
Чтобы понять, какие гены действительно запускают этот переход, учёные собрали набор из 51 гена, связанных с переходом и специфичных для билиарного рака, и использовали его для оценки как отдельных клеток, так и опухолей пациентов. У пациентов с более высокими баллами по этой программе выживаемость была ниже, что связывает клеточную программу с клиническим исходом. Среди генов, обогащённых в клетках с положительной программой перехода, выделялся ген PMEPA1. Высокий уровень PMEPA1 ассоциировался с худшим прогнозом и был выше в метастазах лимфатических узлов, чем в первичных опухолях желчных протоков. При подавлении PMEPA1 в клеточных линиях рака желчных протоков клетки росли медленнее, образовывали меньше колоний, теряли способность мигрировать и инвазировать через искусственные мембраны и значительно хуже посевали опухоли в лёгких у мышей. Усиление экспрессии PMEPA1 давало противоположный эффект.
Как PMEPA1 перенастраивает сигналы внутри клетки
Раскапывая механизм глубже, исследование связало PMEPA1 с известным путём контроля роста, центральным элементом которого является белок YAP1. В здоровых тканях защитный контур удерживает YAP1 преимущественно вне ядра, ограничивая его способность включать гены роста и инвазии. Исследователи показали, что PMEPA1 ослабляет этот контур, позволяя большему количеству YAP1 проникать в ядро. При подавлении PMEPA1 активность верхних ферментов возрастала, YAP1 становился более модифицированным и оставался в цитоплазме, а не в ядре. Этот сдвиг сопровождался более стационарным, менее инвазивным профилем. Химическое вещество, блокирующее эти контрольные ферменты, обратило многие изменения, вызванные утратой PMEPA1, подтверждая, что PMEPA1 продвигает программу перехода, направляя YAP1 в ядро.
Потенциальный препарат для замедления распространения
Поскольку программа перехода тесно связана с резистентностью к лечению, команда проверила, не найдутся ли существующие препараты, избирательно поражающие эти агрессивные клетки. Комбинируя базы данных отклика на лекарства с их генными сигнатурами, они выделили несколько химиотерапевтических агентов, включая SN-38, активную форму иринотекана, как кандидатов. В клеточных экспериментах SN-38 снижал маркёры подвижного состояния, уменьшал способность клеток к миграции и инвазии и снижал уровни как PMEPA1, так и YAP1. Дополнительные данные указывали на то, что SN-38 мешает фактору транскрипции FOS, который обычно повышает продукцию PMEPA1. В модельных исследованиях на мышах с метастазами в лёгких, индуцированными сверхэкспрессией PMEPA1, лечение SN-38 уменьшало метастатическую нагрузку и уровень PMEPA1 в очагах опухоли.
Что это значит для пациентов
Проще говоря, исследование показывает, что специфический белок PMEPA1 действует как главный переключатель, который помогает клеткам рака желчных протоков ослабевать, отходить и колонизировать новые органы. Он делает это, освобождая другой белок, YAP1, чтобы тот мог войти в ядро и активировать гены, способствующие инвазии. Поскольку опухоли с более выраженной этой программой имеют худший прогноз, PMEPA1 и его партнёры могут служить маркёрами риска и терапевтическими мишенями. Открытие того, что SN-38, уже применяемый при других опухолях, способен ослаблять этот переключатель и замедлять метастазирование в моделях, открывает перспективу того, что модернизация или комбинирование подобных подходов в будущем может дать более точные и эффективные варианты лечения для пациентов с билиарным раком.
Цитирование: Xu, W., Ma, C., Li, P. et al. PMEPA1 modulates YAP1 nuclear translocation to disrupt EMT subtypes and promote metastasis in Biliary tract cancer. Cell Death Dis 17, 449 (2026). https://doi.org/10.1038/s41419-026-08684-3
Ключевые слова: рак билиарного тракта, эпителиально-мезенхимальный переход, PMEPA1, сигналинг YAP1, SN-38