Clear Sky Science · he
PMEPA1 מווסתת את הטרנסלוקציה הגרעינית של YAP1 כדי להפריע לתת‑סוגי EMT ולקדם גרורתיות בסרטן דרכי המרה
מדוע מחקר זה חשוב
סרטן דרכי המרה הוא סרטן נדיר אך קטלני של דרכי המרה וכיס המרה, עם מעט אופציות טיפול יעילות וסיכון גבוה להפצה לאיברים מרוחקים. המחקר משתמש בניתוח חדיש של תא‑אחד כדי לחשוף כיצד תאי גידול מסוימים משנים את זהותם כדי להפוך לניידים ולפולשניים יותר, ומזהה מולקולה ספציפית שמניעה את המעבר הזה וניתנת אולי ליעד על‑ידי תרופת כימותרפיה קיימת.
מבט מדויק על גידולי דרכי המרה תא‑אחרת תא
במקום לאמוד אותות על פני גידולים שלמים, החוקרים בחנו כמעט 160,000 תאים בודדים מ‑47 דגימות אנושיות של סרטן דרכי המרה ורקמה תקינה. על‑ידי קריאת הרנ״א של כל תא הם בנו מפה מפורטת של אקוסיסטמת הגידול, כולל תאי חיסון, תאי תמיכה, תאי כלי דם ובפרט תאי אפיתל גידוליים שממנו מתפתח הסרטן. הם מצאו כי ברקמות הגידול היו הרבה יותר תאי אפיתל מאשר ברקמה תקינה וכי תאים אפיתליאליים אלה התחלקו לחמש קבוצות מובחנות, שלכל אחת תפקיד שונה כמו גדילה מהירה, שימוש אנרגטי משתנה, דלקת או עיבוד שומנים.
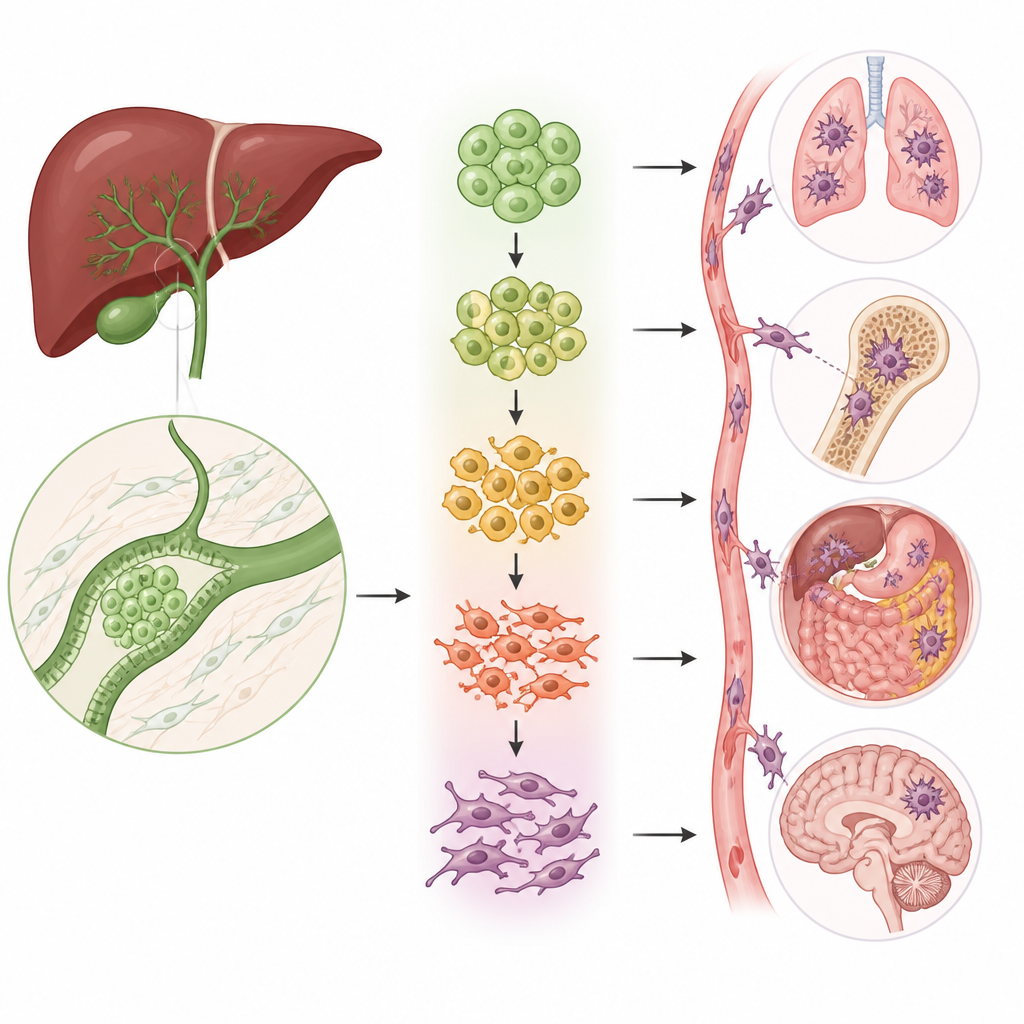
התאים המשתנים בצורה שמניעים את ההפצה
תהליך מרכזי בהפצת סרטן נקרא מעבר אפיתלי‑מזנכימלי (EMT), שבו תאים דחוסים ומסודרים משחררים את קשריהם, משנים צורה ומתחילים לנוע. הצוות גילה כי שתי מתוך חמש קבוצות האפיתל היו מועשרות משמעותית בתוכנית המעבר הזו. באמצעות מספר ניתוחים הראו החוקרים שהתאים בקבוצות אלה ממוקמים לאורך מסלול שמוביל מתאים תקינים וקשורים בצמיחה אל עבר תאים ניידים ופולשניים מאוד. ככל שהתאים מתקדמים על מסלול זה, סמנים קלאסיים של תאים סטטיים נחלשים בעוד שסמנים של תאים ניידים וסיביים עולים, וקושרים תתי‑הקבוצות האלה ישירות ליכולת הגידול לחדור ולגרור גרורות.
PMEPA1 כמתג מרכזי בהתנהגות אגרסיבית
כדי להבין אילו גנים באמת מניעים את השינוי, המדענים הרכיבו סט של 51 גנים הקשורים למעבר ספציפיים לסרטן דרכי המרה והשתמשו בו כדי לתייג הן תאים בודדים והן גידולים של מטופלים. מטופלים שלגידוליהם היו ציונים גבוהים יותר חוו הישרדות נמוכה יותר, וקישור זה מקשר את התוכנית ברמת התאים לתוצאה קלינית. בין הגנים המועשרים בתאים חיוביים למעבר בולט גן אחד בשם PMEPA1. רמות גבוהות של PMEPA1 נקשרו לפרוגנוזה גרועה יותר והיו גבוהות יותר בגרורות בבלוטות הלימפה מאשר בגידולי דרכי המרה המקוריים. כאשר החוקרים הפחיתו את PMEPA1 בקווי תאים של סרטן דרכי המרה, התאים גדלו לאט יותר, יצרו פחות קולוניות, ואיבדו חלק ניכר מיכולתם לנוע ולחדור דרך ממברנות מלאכותיות ולנטוע גידולים בריאות של עכברים. הגברת PMEPA1 נתנה את התוצאה ההפוכה.
כיצד PMEPA1 מחדש איתותים בתוך התא
בחקירה מעמיקה יותר חיבר המחקר את PMEPA1 למסלול בקרה צמיחה מוכר שמתמקד בחלבון בשם YAP1. ברקמות בריאות, מעגל בטיחות שומר על YAP1 ברובו מחוץ לגרעין התא, מה שמגביל את יכולתו להפעיל גנים הקשורים לצמיחה ולחדירה. החוקרים מצאו כי PMEPA1 עוזר להחליש את מעגל הבטיחות הזה, ומאפשר ליותר YAP1 להיכנס לגרעין. כאשר PMEPA1 הושתק, אנזימים מקדמים הפכו לפעילים יותר, YAP1 עבר שינויים בכמות גדולה יותר ונותר לכוד בציטוזול במקום בגרעין. שינוי זה לווה בפרופיל יותר סטציונרי ופחות פולשני. חומר שמחשל את האנזימים האלה היפך רבות מהשינויים שנגרמו מאובדן PMEPA1, ואישר כי PMEPA1 מקדם את תוכנית המעבר על‑ידי כיוון YAP1 לגרעין.
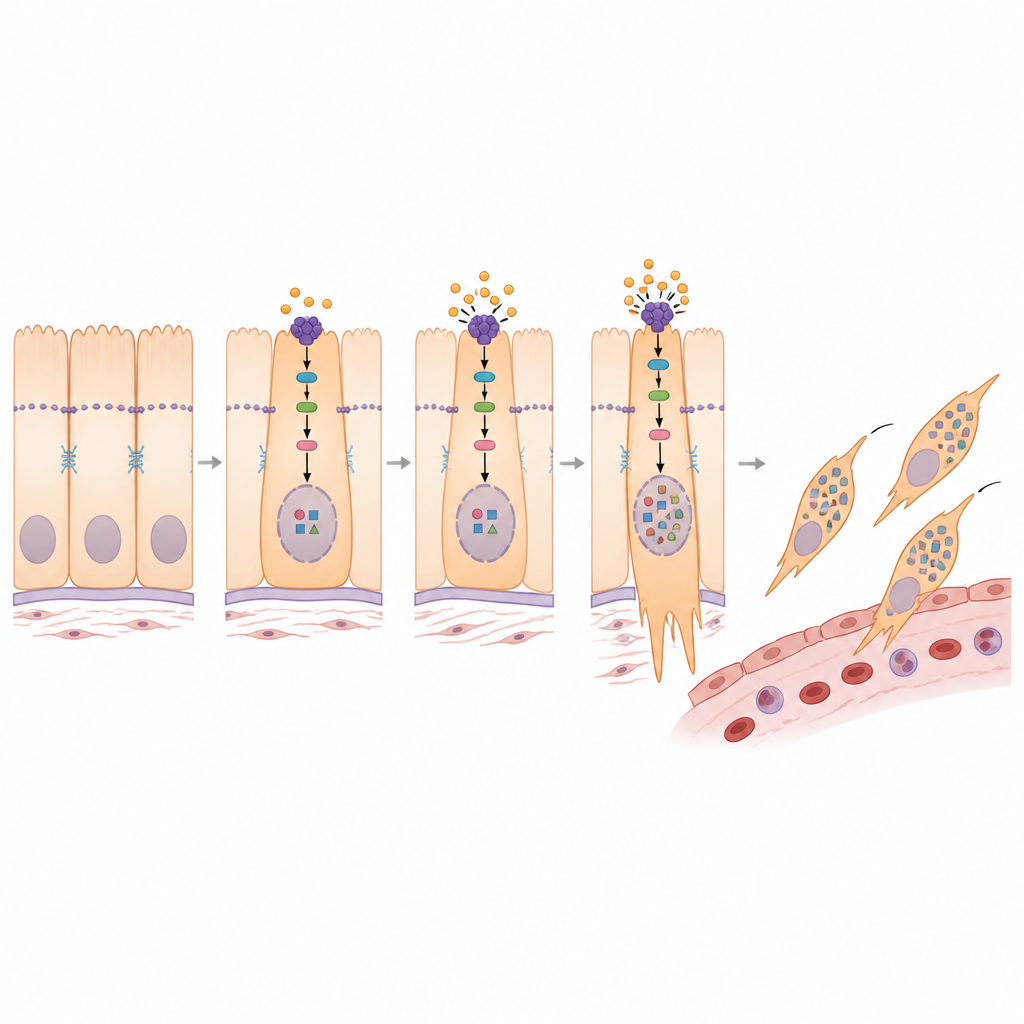
תרופה פוטנציאלית להאטת ההפצה
מכיוון שתוכנית המעבר קשורה היטב לעמידות לטיפול, הצוות בדק האם תרופות קיימות עשויות לפגוע באופן סלקטיבי בתאים אגרסיביים אלה. על‑ידי שילוב מאגרי תגובת תרופות עם חתימות הגנים שלהם, הם ציינו כמה סוכני כימותרפיה כמועמדים, כולל SN‑38, הצורה הפעילה של אירינוטקאן. בניסויים בתאים, SN‑38 הקטין סמנים של המצב הנייד, צמצם את יכולת התאים להגר ולחדור והוריד הן את רמות PMEPA1 והן את רמות YAP1. ממצאים נוספים הציעו כי SN‑38 מפריע לפקטור שעתוק בשם FOS שלרוב מגביר את ייצור PMEPA1. במודלים של עכברים לגרורת ריאות המונעת על‑ידי היפראקספרסיה של PMEPA1, טיפול ב‑SN‑38 הקטין את העומס המטסטטי ואת רמות PMEPA1 במטלאים של הגידול.
מה משמעות הדבר עבור מטופלים
במילים פשוטות, המחקר מראה כי חלבון ספציפי, PMEPA1, פועל כמתג ראשי שעוזר לתאי סרטן דרכי המרה להשתחרר, להיגרר ולהתיישב באיברים חדשים. הוא עושה זאת על‑ידי שחרורו של חלבון נוסף, YAP1, להיכנס לגרעין ולהפעיל גנים שמעדיפים חדירה. מכיוון שגידולים עם גרסה חזקה יותר של תוכנית זו נוטים לתוצאות גרועות יותר, PMEPA1 ושותפיו עשויים לשמש כסמנים מאיימים וליעדים טיפוליים. הממצא ש‑SN‑38, שכבר נמצא בשימוש בסרטן אחר, יכול להחליש את המתג הזה ולהאט גרורתיות במודלים, מעלה את האפשרות שבהמשך ניתן יהיה לחדד או לשלב טיפולים כאלה כדי להציע בעתיד אופציות מדויקות ויעילות יותר לאנשים עם סרטן דרכי המרה.
ציטוט: Xu, W., Ma, C., Li, P. et al. PMEPA1 modulates YAP1 nuclear translocation to disrupt EMT subtypes and promote metastasis in Biliary tract cancer. Cell Death Dis 17, 449 (2026). https://doi.org/10.1038/s41419-026-08684-3
מילות מפתח: סרטן דרכי המרה, מעבר אפיתלי‑מזנכימלי, PMEPA1, איתות YAP1, SN‑38