Clear Sky Science · sv
PMEPA1 reglerar YAP1:s förflyttning till kärnan för att störa EMT-subtyper och främja metastas i gallgångscancer
Varför den här forskningen är viktig
Gallgångscancer är en ovanlig men dödlig cancer i gallgångarna och gallblåsan, med få effektiva behandlingsalternativ och hög risk för spridning till avlägsna organ. I denna studie används avancerad enkelcellsanalys för att avslöja hur vissa tumörceller ändrar sin identitet för att bli mer rörliga och invasiva, och den identifierar en specifik molekyl som driver denna omställning och som kan riktas av ett redan befintligt cytostatikum.
Tittar noga på gallgångstumörer en cell i taget
I stället för att genomsnittliggöra signaler över hela tumörer undersökte forskarna nästan 160 000 individuella celler från 47 mänskliga prover av gallgångscancer och normal vävnad. Genom att läsa varje cells RNA byggde de en detaljerad karta över tumörekosystemet, inklusive immunceller, stödjeceller, blodkärlsceller och särskilt de tumörepitecliala cellerna som ger upphov till cancern. De fann att tumörvävnader innehöll betydligt fler epitelceller än normal vävnad och att dessa epitelceller kunde delas in i fem distinkta grupper, var och en med sitt eget uppdrag, såsom snabb tillväxt, förändrad energianvändning, inflammation eller fettmetabolism.
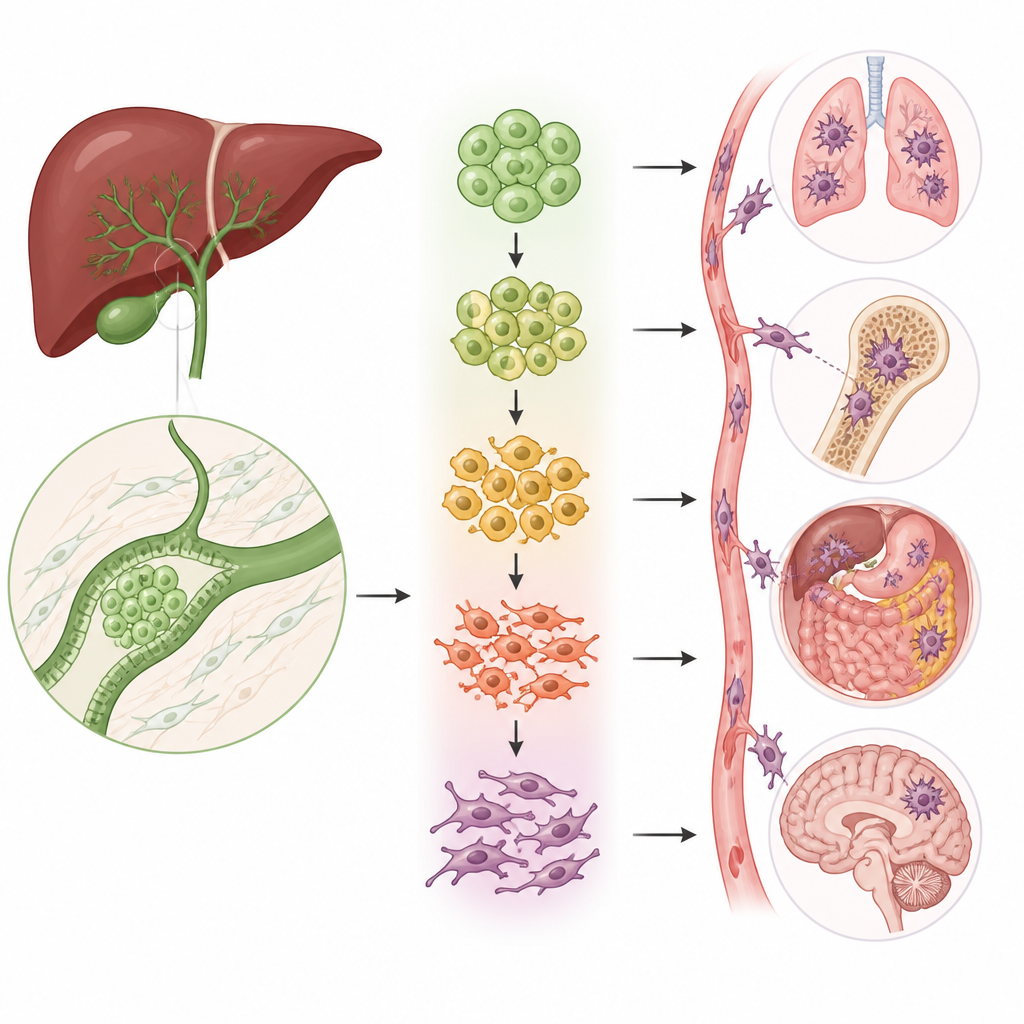
De formskiftande cellerna som driver spridning
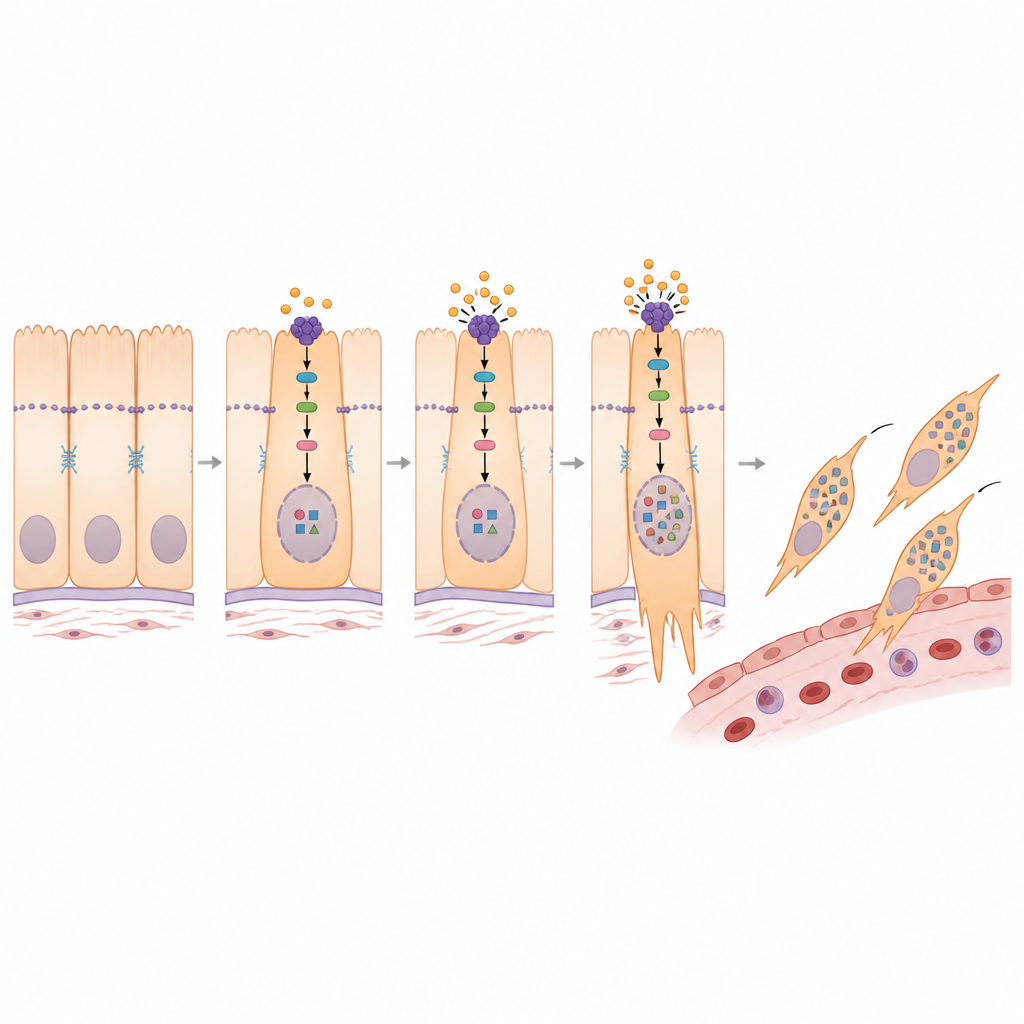
En nyckelprocess i cancerspridning kallas epitelial‑mesenkymal övergång (EMT), där tätt sammanfogade, ordnade celler luckrar upp sina kontakter, ändrar form och börjar röra sig. Teamet upptäckte att två av de fem epitelgrupperna var starkt berikade för detta övergångsprogram. Med flera analysmetoder visade de att celler i dessa grupper ligger längs en bana från mer normallika, tätt sammankopplade celler mot högst rörliga, invasiva celler. När celler förflyttas längs denna bana avtar klassiska markörer för stationära celler medan markörer för rörliga, fibrösa celler ökar, vilket länkar dessa undergrupper direkt till tumörens förmåga att invadera och metastasera.
PMEPA1 som en central knapp för aggressivt beteende
För att förstå vilka gener som faktiskt driver denna förändring samlade forskarna en uppsättning om 51 övergångsrelaterade gener specifika för gallgångscancer och använde dem för att poängsätta både enskilda celler och patienttumörer. Patienter vars tumörer hade högre poäng hade sämre överlevnad, vilket kopplade cellnivåprogrammets betydelse till kliniskt utfall. Bland de gener som var berikade i övergångspositiva celler framträdde en som kallades PMEPA1. Höga PMEPA1‑nivåer var kopplade till sämre prognos och var högre i lymfkörtelmetastaser än i de ursprungliga gallgångstumörerna. När forskarna minskade PMEPA1 i gallgångscancercellinjer växte cellerna långsammare, bildade färre kolonier och förlorade mycket av sin förmåga att röra sig och invadera genom artificiella membran samt att anlägga tumörer i mösens lungor. Att öka PMEPA1 gav motsatt effekt.
Hur PMEPA1 omkopplar signaler inne i cellen
Vid djupare analys kopplade studien PMEPA1 till en känd tillväxtkontrollväg centrerad kring ett protein kallat YAP1. I frisk vävnad håller en säkerhetskrets YAP1 mestadels utanför cellkärnan och begränsar dess förmåga att slå på gener för tillväxt och invasion. Forskarna fann att PMEPA1 bidrar till att försvaga denna säkerhetskrets, vilket tillåter mer YAP1 att komma in i kärnan. När PMEPA1 tystades blev de upstream‑enzymerna mer aktiva, YAP1 modifierades i högre grad och hölls kvar i cytoplasman istället för i kärnan. Denna förskjutning åtföljdes av ett mer stillsamt, mindre invasivt profil. En kemisk hämmare av säkerhetsenzymerna återställde många av förändringarna som orsakats av förlust av PMEPA1, vilket bekräftar att PMEPA1 främjar övergångsprogrammet genom att styra YAP1 in i kärnan.
En möjlig medicin för att bromsa spridning
Eftersom övergångsprogrammet är nära kopplat till behandlingsresistens undersökte teamet om några befintliga läkemedel selektivt kunde slå mot dessa aggressiva celler. Genom att kombinera databaser för läkemedelsrespons med deras gensignaturer flaggade de flera cytostatika, inklusive SN‑38, den aktiva formen av irinotekan, som kandidater. I cellexperiment minskade SN‑38 markörer för den rörliga cellstaten, reducerade cellernas förmåga att migrera och invadera, och sänkte både PMEPA1‑ och YAP1‑nivåerna. Ytterligare arbete antydde att SN‑38 stör en transkriptionsfaktor kallad FOS som normalt ökar PMEPA1‑produktionen. I musmodeller för lungmetastasering drivna av PMEPA1‑överuttryck minskade behandling med SN‑38 både metastasbörda och PMEPA1‑nivåer i tumöravsättningarna.
Vad detta betyder för patienter
I klartext visar denna studie att ett specifikt protein, PMEPA1, fungerar som en huvudströmbrytare som hjälper gallgångscancerceller att lossna, förflytta sig och kolonisera nya organ. Det gör det genom att frigöra ett annat protein, YAP1, så att det kan gå in i kärnan och aktivera gener som gynnar invasion. Eftersom tumörer med starkare versioner av detta program har sämre utfall kan PMEPA1 och dess partners fungera som varningsmarkörer och behandlingsmål. Upptäckten att SN‑38, som redan används i andra cancerformer, kan dämpa denna omkoppling och bromsa metastas i modeller öppnar för möjligheten att förfina eller kombinera sådana behandlingar för att en dag erbjuda mer precisa och effektiva alternativ för personer med gallgångscancer.
Citering: Xu, W., Ma, C., Li, P. et al. PMEPA1 modulates YAP1 nuclear translocation to disrupt EMT subtypes and promote metastasis in Biliary tract cancer. Cell Death Dis 17, 449 (2026). https://doi.org/10.1038/s41419-026-08684-3
Nyckelord: gallgångscancer, epitelial-mesenkymal övergång, PMEPA1, YAP1‑signalering, SN‑38