Clear Sky Science · pt
PMEPA1 modula a translocação nuclear de YAP1 para perturbar subtipos de EMT e promover metástase no câncer do trato biliar
Por que esta pesquisa importa
O câncer do trato biliar é uma doença rara, porém letal, dos ductos biliares e da vesícula biliar, com poucas opções terapêuticas eficazes e alta probabilidade de disseminação para órgãos distantes. Este estudo utiliza análise em célula única de ponta para revelar como certas células tumorais mudam sua identidade para se tornarem mais móveis e invasivas, e identifica uma molécula específica que impulsiona essa mudança e que pode ser alvo de um quimioterápico já existente.
Observando de perto tumores dos ductos biliares, célula por célula
Em vez de fazer médias sobre tumores inteiros, os pesquisadores examinaram quase 160.000 células individuais de 47 amostras humanas de câncer do trato biliar e tecidos normais. Ao ler o RNA de cada célula, eles construíram um mapa detalhado do ecossistema tumoral, incluindo células imunes, células de suporte, células vasculares e, especialmente, as células epiteliais tumorais que dão origem ao câncer. Constataram que os tecidos tumorais continham muito mais células epiteliais do que o tecido normal e que essas células epiteliais podiam ser divididas em cinco grupos distintos, cada um com sua função, como crescimento rápido, uso de energia alterado, inflamação ou processamento de lipídios.
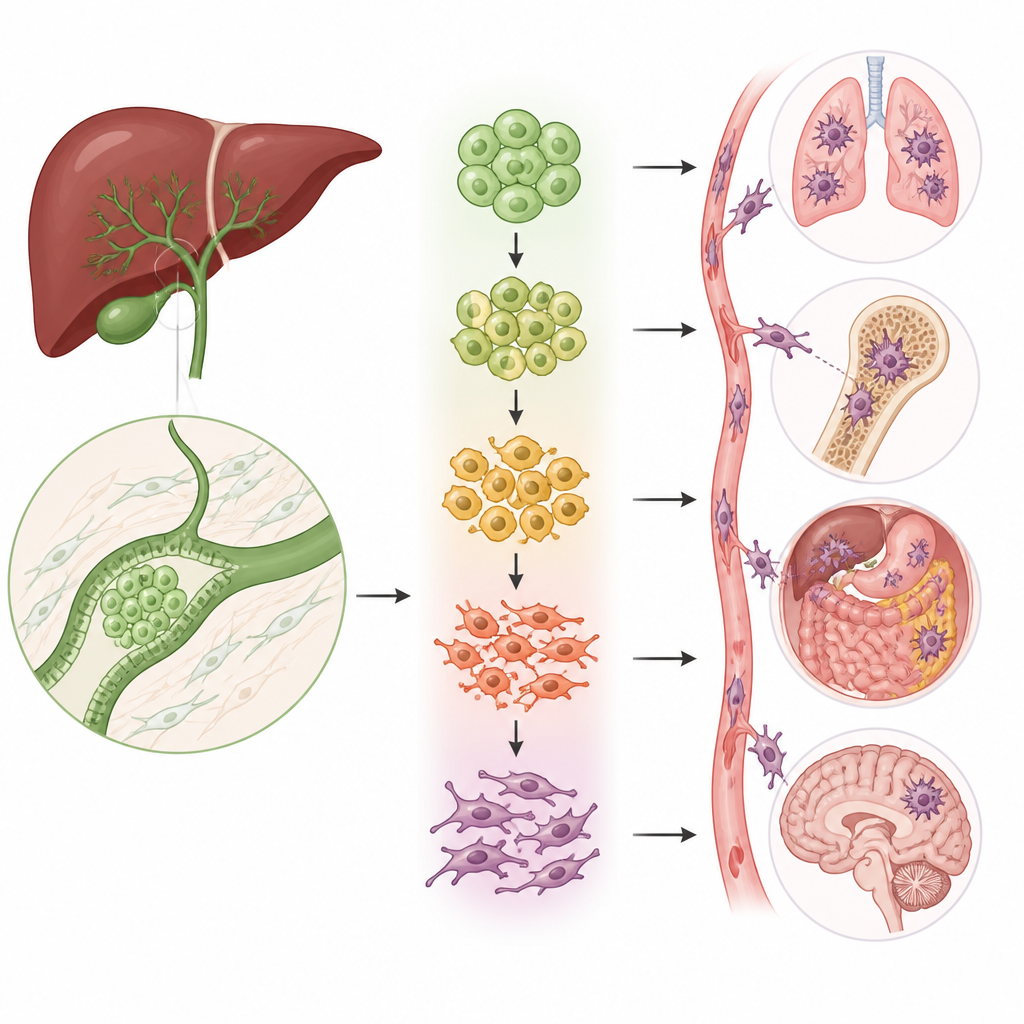
As células mutantes de forma que impulsionam a disseminação
Um processo-chave na disseminação do câncer é a transição epitélio-mesenquimal (EMT), na qual células compactas e organizadas afrouxam suas conexões, mudam de forma e começam a se mover. A equipe descobriu que dois dos cinco grupos epiteliais estavam fortemente enriquecidos por esse programa de transição. Usando vários tipos de análise, mostraram que as células nesses grupos se dispõem ao longo de um trajeto do tipo mais semelhante ao normal, com forte conectividade, até células altamente móveis e invasivas. Conforme as células progridem ao longo desse trajeto, marcadores clássicos de células estacionárias desaparecem enquanto marcadores de células móveis e fibróticas aumentam, ligando esses subgrupos diretamente à capacidade do tumor de invadir e metastatizar.
PMEPA1 como um interruptor central do comportamento agressivo
Para entender quais genes realmente impulsionam essa mudança, os cientistas montaram um conjunto de 51 genes relacionados à transição específicos do câncer do trato biliar e os usaram para pontuar tanto células individuais quanto tumores de pacientes. Pacientes cujos tumores tinham pontuações mais altas apresentaram pior sobrevida, conectando o programa ao nível celular ao desfecho clínico. Entre os genes enriquecidos em células positivas para a transição, um chamado PMEPA1 destacou-se. Níveis elevados de PMEPA1 foram associados a pior prognóstico e estavam mais altos em metástases de linfonodo do que nos tumores primários do ducto biliar. Quando os pesquisadores reduziram PMEPA1 em linhagens celulares de câncer do ducto biliar, as células cresceram mais devagar, formaram menos colônias e perderam grande parte da capacidade de migrar e invadir através de membranas artificiais e de semear tumores nos pulmões de camundongos. Aumentar PMEPA1 teve o efeito oposto.
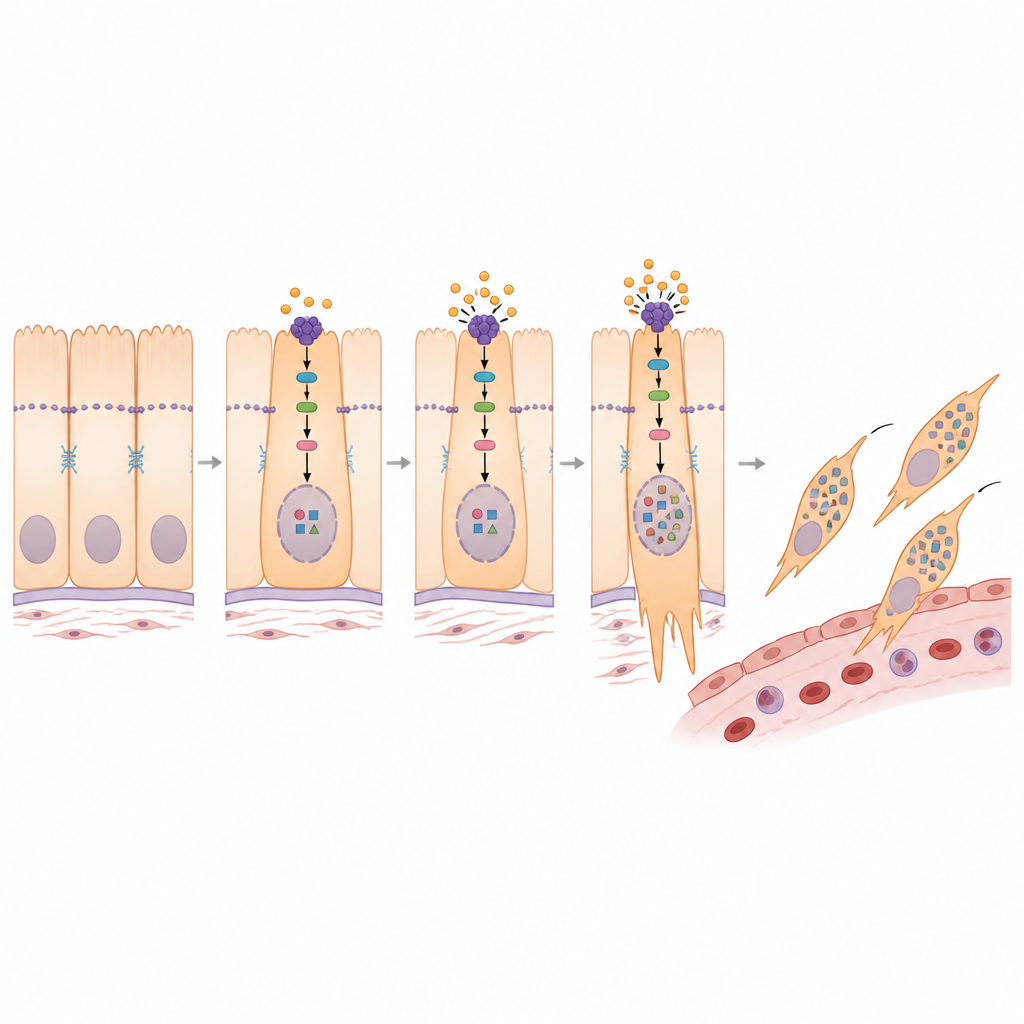
Como PMEPA1 reprograma sinais dentro da célula
Aprofundando-se, o estudo conectou PMEPA1 a uma via conhecida de controle de crescimento centrada em uma proteína chamada YAP1. Em tecidos saudáveis, um circuito de segurança mantém YAP1 majoritariamente fora do núcleo celular, limitando sua capacidade de ativar genes de crescimento e invasão. Os pesquisadores descobriram que PMEPA1 contribui para enfraquecer esse circuito de segurança, permitindo que mais YAP1 entre no núcleo. Quando PMEPA1 foi silenciado, enzimas a montante tornaram-se mais ativas, YAP1 foi mais intensamente modificado e permaneceu retido no citoplasma em vez do núcleo. Essa mudança veio acompanhada de um perfil mais estacionário e menos invasivo. Um composto químico que bloqueia as enzimas de segurança reverteu muitas das alterações causadas pela perda de PMEPA1, confirmando que PMEPA1 promove o programa de transição ao direcionar YAP1 para o núcleo.
Um possível fármaco para frear a disseminação
Como o programa de transição está intimamente ligado à resistência ao tratamento, a equipe perguntou em seguida se algum fármaco existente poderia atingir seletivamente essas células agressivas. Ao combinar bancos de dados de resposta a drogas com suas assinaturas gênicas, eles apontaram vários agentes quimioterápicos, incluindo SN-38, a forma ativa da irinotecana, como candidatos. Em experimentos celulares, SN-38 reduziu marcadores do estado celular móvel, diminuiu a capacidade das células de migrar e invadir, e reduziu tanto os níveis de PMEPA1 quanto de YAP1. Trabalhos adicionais sugeriram que SN-38 interfere com um fator de transcrição chamado FOS, que normalmente aumenta a produção de PMEPA1. Em modelos de camundongo de metástase pulmonar impulsionada pela superexpressão de PMEPA1, o tratamento com SN-38 reduziu a carga metastática e os níveis de PMEPA1 nos depósitos tumorais.
O que isso significa para os pacientes
Em termos práticos, este estudo mostra que uma proteína específica, PMEPA1, age como um interruptor mestre que ajuda as células do câncer do ducto biliar a se afrouxarem, se deslocarem e colonizarem novos órgãos. Ela faz isso liberando outra proteína, YAP1, para entrar no núcleo e ativar genes que favorecem a invasão. Como tumores com versões mais pronunciadas desse programa têm pior prognóstico, PMEPA1 e seus parceiros podem servir como marcadores de alerta e alvos terapêuticos. A constatação de que SN-38, já usado em outros cânceres, pode atenuar esse interruptor e desacelerar a metástase em modelos levanta a possibilidade de que refinar ou combinar essas terapias possa um dia oferecer opções mais precisas e eficazes para pessoas com câncer do trato biliar.
Citação: Xu, W., Ma, C., Li, P. et al. PMEPA1 modulates YAP1 nuclear translocation to disrupt EMT subtypes and promote metastasis in Biliary tract cancer. Cell Death Dis 17, 449 (2026). https://doi.org/10.1038/s41419-026-08684-3
Palavras-chave: câncer do trato biliar, transição epitélio-mesenquimal, PMEPA1, sinalização YAP1, SN-38