Clear Sky Science · es
PMEPA1 modula la translocación nuclear de YAP1 para alterar subtipos de EMT y promover la metástasis en el cáncer de vías biliares
Por qué importa esta investigación
El cáncer de vías biliares es un cáncer raro pero letal de los conductos biliares y la vesícula biliar, con pocas opciones terapéuticas efectivas y una alta probabilidad de diseminarse a órganos distantes. Este estudio utiliza análisis unicelular de vanguardia para descubrir cómo ciertas células tumorales cambian su identidad para volverse más móviles e invasivas, y señala una molécula concreta que impulsa este cambio y que podría ser objetivo de un fármaco quimioterápico ya existente.
Analizando los tumores biliares celda a celda
En lugar de promediar señales de tumores completos, los investigadores examinaron casi 160.000 células individuales de 47 muestras humanas de cáncer de vías biliares y tejido normal. Al leer el ARN de cada célula, construyeron un mapa detallado del ecosistema tumoral, que incluye células inmunitarias, células de soporte, endoteliales y, especialmente, las células epiteliales tumorales que dan lugar al cáncer. Encontraron que los tejidos tumorales contenían muchas más células epiteliales que el tejido normal y que estas células epiteliales podían dividirse en cinco grupos distintos, cada uno con su función, como crecimiento rápido, uso energético alterado, inflamación o procesamiento de lípidos.
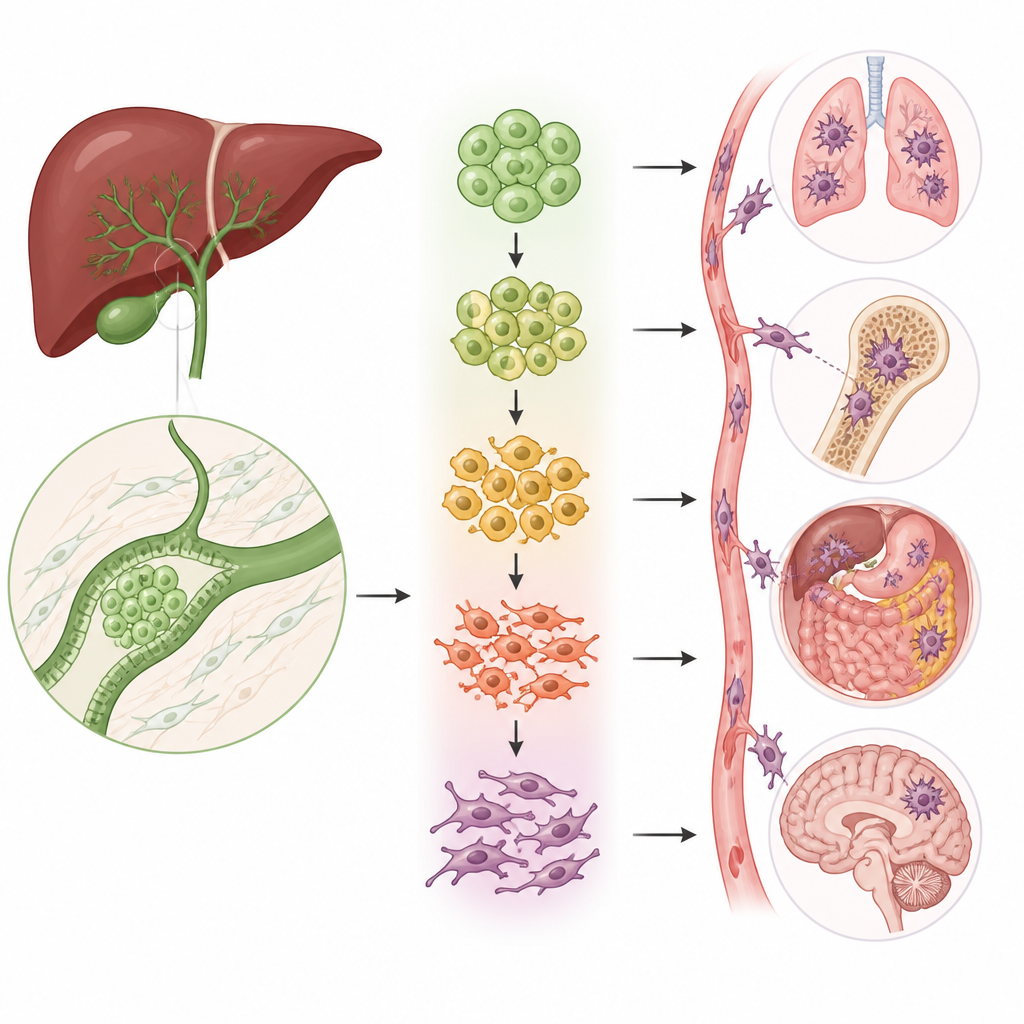
Las células cambiante de forma que impulsan la diseminación
Un proceso clave en la diseminación del cáncer se llama transición epitelio–mesénquima (EMT), en la que las células compactas y ordenadas aflojan sus uniones, cambian de forma y empiezan a moverse. El equipo descubrió que dos de los cinco grupos epiteliales estaban fuertemente enriquecidos en este programa de transición. Mediante varios tipos de análisis, mostraron que las células en estos grupos se sitúan a lo largo de un trayecto desde células parecidas a las normales y fuertemente conectadas hacia células altamente móviles e invasivas. A medida que las células progresan por este trayecto, los marcadores clásicos de células estacionarias disminuyen mientras que aumentan los marcadores de células móviles y fibróticas, vinculando estos subgrupos directamente con la capacidad del tumor para invadir y hacer metástasis.
PMEPA1 como interruptor central del comportamiento agresivo
Para entender qué genes impulsan realmente este cambio, los científicos reunieron un conjunto de 51 genes relacionados con la transición específicos del cáncer de vías biliares y los usaron para puntuar tanto las células individuales como los tumores de pacientes. Los pacientes cuyos tumores tenían puntuaciones más altas presentaron peor supervivencia, conectando el programa a nivel celular con el resultado clínico. Entre los genes enriquecidos en células positivas para la transición, uno llamado PMEPA1 destacó. Niveles altos de PMEPA1 se asociaron con un peor pronóstico y eran superiores en metástasis de ganglios linfáticos que en los tumores primarios de vía biliar. Cuando los investigadores redujeron PMEPA1 en líneas celulares de cáncer de vías biliares, las células crecieron más despacio, formaron menos colonias y perdieron gran parte de su capacidad de moverse e invadir a través de membranas artificiales y de sembrar tumores en los pulmones de ratones. Incrementar PMEPA1 produjo el efecto contrario.
Cómo PMEPA1 reconfigura las señales dentro de la célula
Profundizando, el estudio conectó PMEPA1 con una vía de control del crecimiento conocida centrada en una proteína llamada YAP1. En tejidos sanos, un circuito de seguridad mantiene a YAP1 mayormente fuera del núcleo celular, limitando su capacidad para activar genes de crecimiento e invasión. Los investigadores hallaron que PMEPA1 contribuye a debilitar ese circuito de seguridad, permitiendo que más YAP1 entre en el núcleo. Cuando se silenció PMEPA1, las enzimas aguas arriba se volvieron más activas, YAP1 presentó más modificaciones y quedó retenida en el citoplasma en lugar del núcleo. Este cambio se acompañó de un perfil más estacionario y menos invasivo. Un compuesto químico que bloquea las enzimas de ese circuito revirtió muchos de los cambios causados por la pérdida de PMEPA1, confirmando que PMEPA1 promueve el programa de transición al dirigir a YAP1 hacia el núcleo.
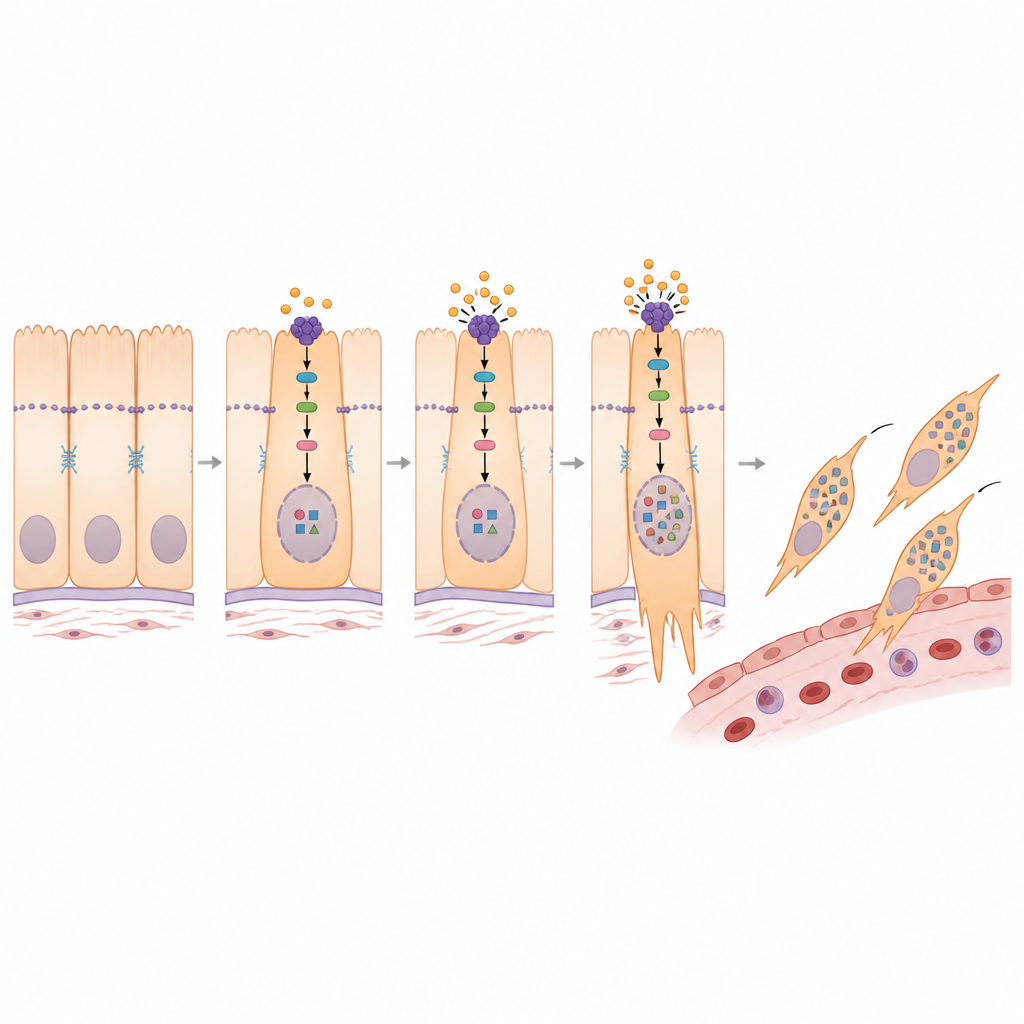
Un fármaco potencial para frenar la diseminación
Dado que el programa de transición está estrechamente ligado a la resistencia al tratamiento, el equipo preguntó si fármacos ya existentes podrían alcanzar selectivamente a estas células agresivas. Al combinar bases de datos de respuesta a fármacos con sus firmas génicas, identificaron varios agentes quimioterápicos, incluido SN-38, la forma activa de irinotecán, como candidatos. En experimentos celulares, SN-38 redujo marcadores del estado celular móvil, disminuyó la capacidad de migración e invasión de las células y rebajó tanto los niveles de PMEPA1 como de YAP1. Trabajos adicionales sugirieron que SN-38 interfiere con un factor de transcripción llamado FOS que normalmente potencia la producción de PMEPA1. En modelos de ratón de metástasis pulmonar impulsados por la sobreexpresión de PMEPA1, el tratamiento con SN-38 redujo la carga metastásica y los niveles de PMEPA1 en los depósitos tumorales.
Qué significa esto para los pacientes
En términos sencillos, este estudio muestra que una proteína específica, PMEPA1, actúa como un interruptor maestro que ayuda a las células del cáncer de vías biliares a soltarse, desplazarse y colonizar nuevos órganos. Lo hace al liberar a otra proteína, YAP1, para que entre en el núcleo y active programas génicos que favorecen la invasión. Debido a que los tumores con una versión más fuerte de este programa presentan peores resultados, PMEPA1 y sus asociados podrían servir como marcadores de alerta y como dianas terapéuticas. El hallazgo de que SN-38, ya usado en otros cánceres, puede atenuar este interruptor y frenar la metástasis en modelos plantea la posibilidad de que refinar o combinar estas terapias pueda ofrecer algún día opciones más precisas y efectivas para las personas con cáncer de vías biliares.
Cita: Xu, W., Ma, C., Li, P. et al. PMEPA1 modulates YAP1 nuclear translocation to disrupt EMT subtypes and promote metastasis in Biliary tract cancer. Cell Death Dis 17, 449 (2026). https://doi.org/10.1038/s41419-026-08684-3
Palabras clave: cáncer de vías biliares, transición epitelio–mesénquima, PMEPA1, señalización YAP1, SN-38