Clear Sky Science · de
PMEPA1 moduliert die nukleäre Translokation von YAP1, stört EMT-Subtypen und fördert Metastasen beim Gallengangskarzinom
Warum diese Forschung wichtig ist
Gallengangskarzinom ist eine seltene, aber tödliche Krebsform der Gallenwege und der Gallenblase, mit wenigen wirksamen Behandlungsoptionen und hoher Wahrscheinlichkeit der Fernmetastasierung. Diese Studie nutzt modernste Einzelzellanalysen, um zu zeigen, wie bestimmte Tumorzellen ihre Identität ändern, um mobiler und invasiver zu werden, und identifiziert ein spezifisches Molekül, das diesen Wechsel antreibt und durch ein bereits verfügbares Chemotherapeutikum gezielt werden könnte.
Die Gallenwegstumoren Zelle für Zelle genau betrachten
Anstatt Signale über ganze Tumoren zu mitteln, untersuchten die Forscher nahezu 160.000 einzelne Zellen aus 47 menschlichen Proben von Gallengangskarzinomen und Normalgewebe. Durch das Auslesen der RNA jeder Zelle erstellten sie eine detaillierte Karte des Tumorökosystems, einschließlich Immunzellen, Stützgewebe, Blutgefäßzellen und besonders der Tumor-epithelialen Zellen, aus denen der Krebs entsteht. Sie stellten fest, dass Tumorgewebe deutlich mehr epitheliale Zellen enthielt als normales Gewebe und dass sich diese epithelialen Zellen in fünf verschiedene Gruppen unterteilen ließen, jede mit einer eigenen Funktion, etwa schnelles Wachstum, veränderter Energiestoffwechsel, Entzündungsantwort oder Fettstoffwechsel.
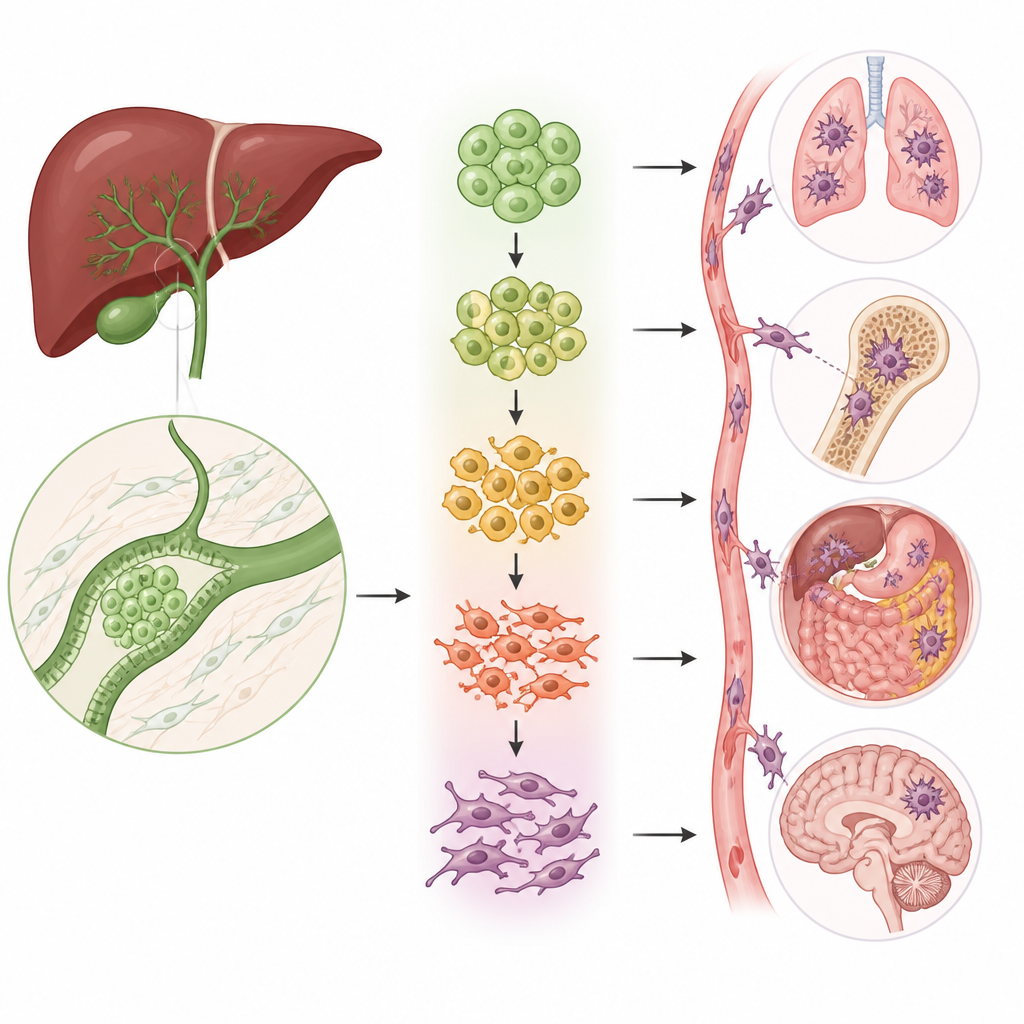
Die gestaltwandelnden Zellen, die die Ausbreitung antreiben
Ein zentraler Prozess bei der Krebsstreuung ist die epithelial-mesenchymale Transition (EMT), bei der kompakte, geordnete Zellen ihre Bindungen lockern, ihre Form ändern und zu wandern beginnen. Das Team entdeckte, dass zwei der fünf epithelialen Zellgruppen stark mit diesem Übergangsprogramm angereichert waren. Mit mehreren Analyseansätzen zeigten sie, dass sich Zellen dieser Gruppen auf einem Pfad von normalähnlichen, eng verbundenen Zellen zu hochmobilen, invasiven Zellen befinden. Im Verlauf dieses Pfades schwinden klassische Marker stationärer Zellen, während Marker mobiler, fibröser Zellen zunehmen — ein direkter Zusammenhang dieser Subgruppen mit der Fähigkeit des Tumors zu invasivem Wachstum und Metastasierung.
PMEPA1 als zentraler Schalter für aggressives Verhalten
Um zu verstehen, welche Gene diesen Wandel tatsächlich antreiben, stellten die Wissenschaftler einen Satz von 51 Übergangsgenen zusammen, die für das Gallengangskarzinom spezifisch sind, und nutzten diese, um sowohl einzelne Zellen als auch Tumoren von Patienten zu bewerten. Patienten mit höheren Scores hatten eine schlechtere Überlebensprognose, sodass das zelluläre Programm mit dem klinischen Verlauf verknüpft ist. Unter den in Übergangs-positiven Zellen angereicherten Genen stach eines namens PMEPA1 hervor. Hohe PMEPA1-Spiegel standen mit schlechterer Prognose in Verbindung und waren in Lymphknotenmetastasen höher als in den Primärtumoren der Gallenwege. Wenn die Forscher PMEPA1 in Zelllinien des Gallengangskarzinoms reduzierten, wuchsen die Zellen langsamer, bildeten weniger Kolonien und verloren einen Großteil ihrer Fähigkeit, sich zu bewegen, durch künstliche Membranen einzudringen und in den Lungen von Mäusen Tumoren zu bilden. Eine Erhöhung von PMEPA1 zeigte den umgekehrten Effekt.
Wie PMEPA1 Signale innerhalb der Zelle umschaltet
Bei tiefergehender Untersuchung verband die Studie PMEPA1 mit einem bekannten Wachstumsregulationsweg, der um das Protein YAP1 zentriert ist. In gesunden Geweben hält eine Sicherheits-Schaltung YAP1 überwiegend außerhalb des Zellkerns, wodurch seine Fähigkeit, Wachstums- und Invasionsgene einzuschalten, begrenzt wird. Die Forscher fanden heraus, dass PMEPA1 dazu beiträgt, diese Sicherheits-Schaltung zu schwächen, sodass mehr YAP1 in den Zellkern gelangen kann. Bei Stilllegung von PMEPA1 wurden die upstream-Enzyme aktiver, YAP1 stärker modifiziert und blieb im Zytoplasma statt im Zellkern gefangen. Dieser Wechsel ging mit einem stationäreren, weniger invasiven Profil einher. Ein Wirkstoff, der diese Sicherheits-Enzyme blockiert, kehrte viele der durch PMEPA1-Verlust verursachten Veränderungen um und bestätigte, dass PMEPA1 das Übergangsprogramm fördert, indem es YAP1 in den Kern steuert.
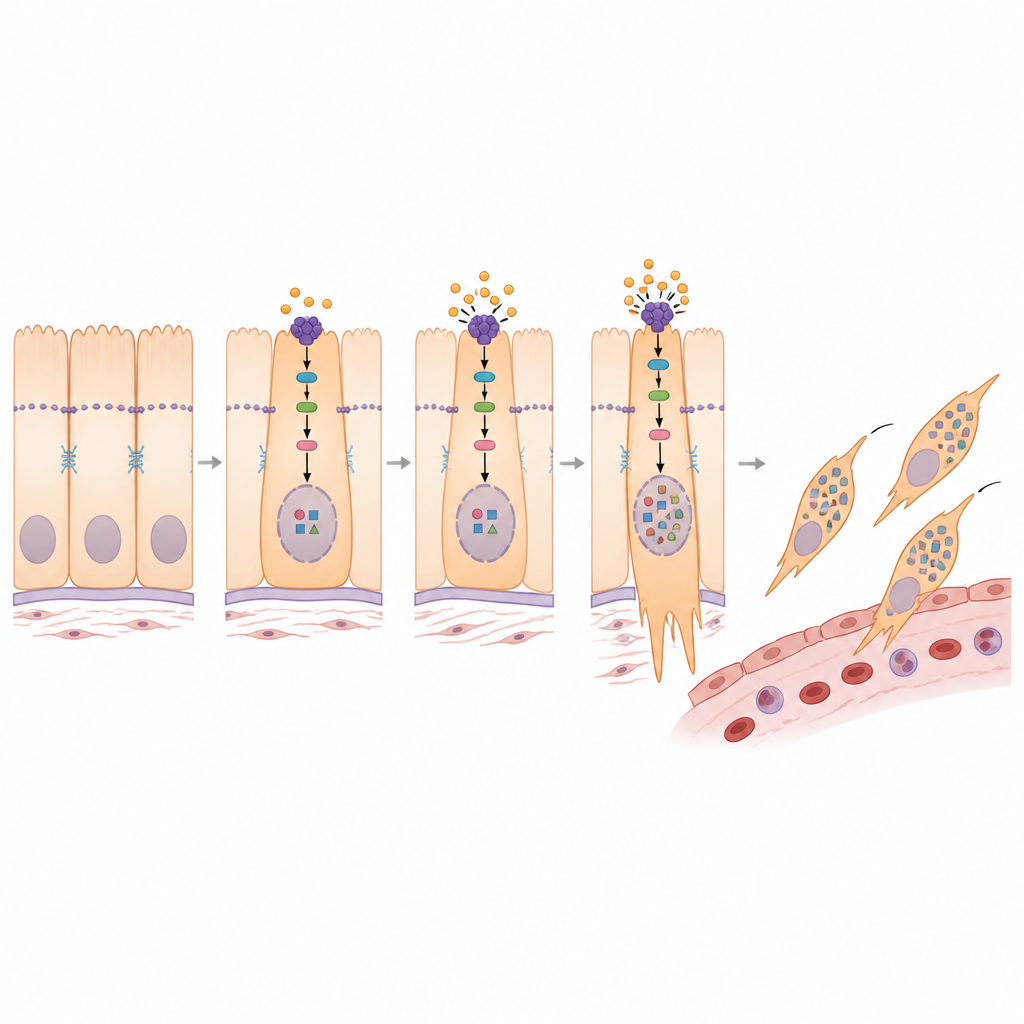
Ein potenzielles Medikament, um die Ausbreitung zu verlangsamen
Da das Übergangsprogramm eng mit Therapieresistenz verbunden ist, fragten die Forscher als Nächstes, ob bestehende Medikamente diese aggressiven Zellen selektiv treffen könnten. Durch die Kombination von Wirkstoffantwort-Datenbanken mit ihren Gen-Signaturen identifizierten sie mehrere Chemotherapeutika, darunter SN-38, die aktive Form von Irinotecan, als Kandidaten. In Zellexperimenten verringerte SN-38 Marker des mobilen Zellzustands, reduzierte die Wander- und Invasionsfähigkeit der Zellen und senkte sowohl PMEPA1- als auch YAP1-Level. Weitere Arbeiten zeigten, dass SN-38 in einen Transkriptionsfaktor namens FOS eingreift, der normalerweise die PMEPA1-Produktion fördert. In Mausmodellen für Lungenmetastasen, die durch PMEPA1-Überexpression getrieben wurden, reduzierte die SN-38-Behandlung die Metastasenlast und die PMEPA1-Spiegel in Tumorabsiedlungen.
Was das für Patientinnen und Patienten bedeutet
Kurz gesagt zeigt diese Studie, dass ein spezifisches Protein, PMEPA1, wie ein Hauptschalter wirkt, der Gallengangkrebszellen hilft, sich zu lösen, wegzuwandern und neue Organe zu besiedeln. Es tut dies, indem es einem anderen Protein, YAP1, ermöglicht, in den Zellkern zu gelangen und Gene zu aktivieren, die Invasion begünstigen. Da Tumoren mit stärker ausgeprägtem diesem Programm schlechtere Verläufe zeigen, könnten PMEPA1 und seine Partner als Warnmarker und therapeutische Ziele dienen. Die Beobachtung, dass SN-38, das bereits in anderen Krebsarten eingesetzt wird, diesen Schalter dämpfen und in Modellen die Metastasierung verlangsamen kann, eröffnet die Möglichkeit, dass die Verfeinerung oder Kombination solcher Therapien eines Tages präzisere und wirksamere Optionen für Menschen mit Gallengangskarzinom bieten könnte.
Zitation: Xu, W., Ma, C., Li, P. et al. PMEPA1 modulates YAP1 nuclear translocation to disrupt EMT subtypes and promote metastasis in Biliary tract cancer. Cell Death Dis 17, 449 (2026). https://doi.org/10.1038/s41419-026-08684-3
Schlüsselwörter: Gallengangskarzinom, epithelial-mesenchymale Transition, PMEPA1, YAP1-Signalgebung, SN-38