Clear Sky Science · nl
PMEPA1 moduleert YAP1-nucleaire translocatie om EMT-subtypen te verstoren en metastase te bevorderen bij galwegkanker
Waarom dit onderzoek ertoe doet
Galwegkanker is een zeldzame maar dodelijke vorm van kanker van de galgangen en de galblaas, met weinig effectieve behandelingsopties en een grote kans op uitzaaiing naar verre organen. Deze studie gebruikt geavanceerde single-cellanalyse om te achterhalen hoe bepaalde tumorcellen van identiteit veranderen om mobieler en invasiever te worden, en identificeert een specifiek molecuul dat deze omschakeling aandrijft en mogelijk gericht kan worden met een bestaand chemotherapiemiddel.
Galwegtumoren één cel tegelijk nader bekeken
In plaats van signalen te middelen over hele tumoren, onderzochten de onderzoekers bijna 160.000 individuele cellen uit 47 humane monsters van galwegkanker en normaal weefsel. Door het RNA van elke cel te lezen, bouwden ze een gedetailleerde kaart van het tumorecosysteem, inclusief immuuncellen, ondersteunende cellen, bloedvatcellen en vooral de tumor epitheelcellen waaruit de kanker ontstaat. Ze vonden dat tumorweefsels veel meer epitheelcellen bevatten dan normaal weefsel en dat deze epitheelcellen konden worden onderverdeeld in vijf verschillende groepen, elk met een eigen functie, zoals snelle groei, veranderd energiegebruik, ontsteking of vetverwerking.
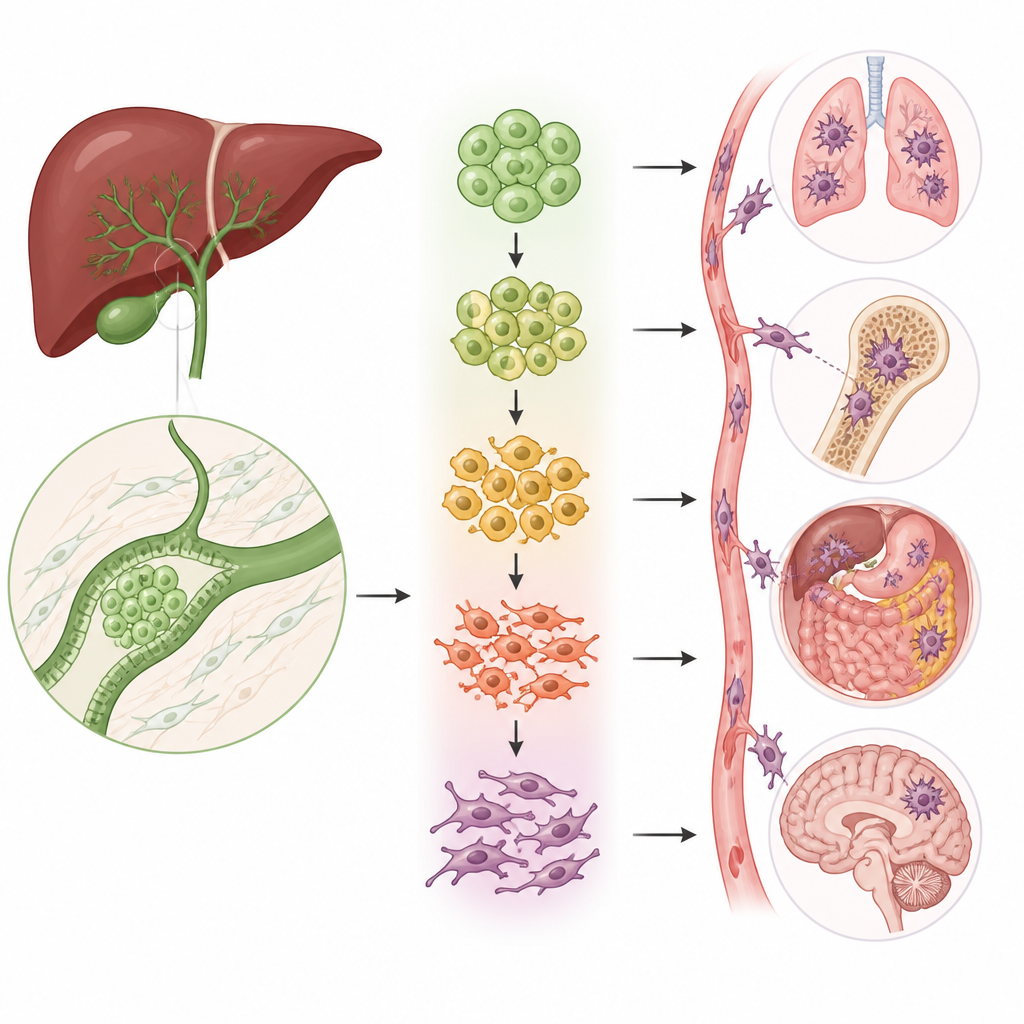
De vormveranderende cellen die verspreiding aandrijven
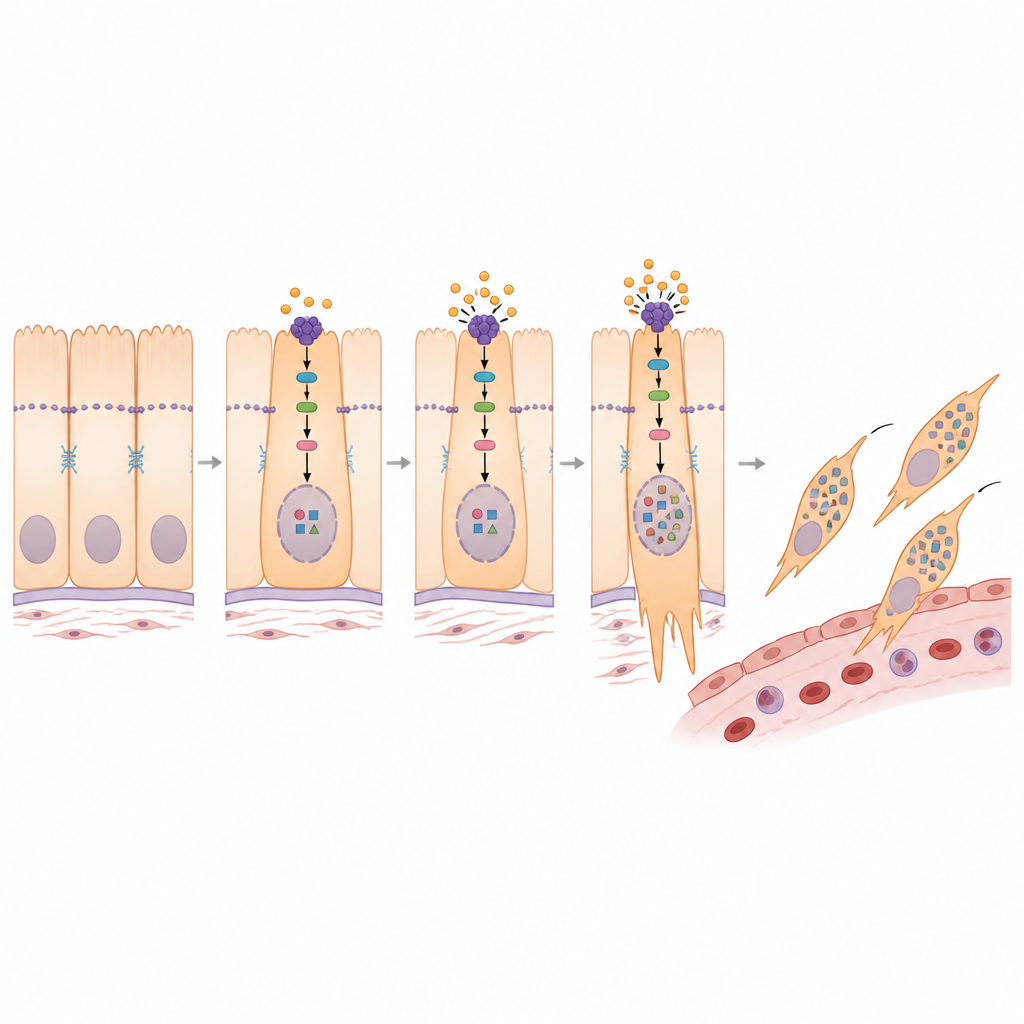
Een belangrijk proces bij kankerspreiding is de epitheliaal-mesenchymale transitie (EMT), waarbij compacte, geordende cellen hun verbindingen verzwakken, van vorm veranderen en gaan bewegen. Het team ontdekte dat twee van de vijf epitheelcelgroepen sterk verrijkt waren voor dit transitieprogramma. Met verschillende analysemethoden toonden ze aan dat cellen in deze groepen langs een traject liggen van normaal-achtige, strak verbonden cellen naar sterk mobiele, invasieve cellen. Naarmate cellen dit pad volgen, nemen de klassieke merkers van stationaire cellen af terwijl merkers van mobiele, vezelachtige cellen toenemen, waarmee deze subgroepen rechtstreeks worden gekoppeld aan het vermogen van de tumor om in te dringen en te metastaseren.
PMEPA1 als centraal schakelpunt in agressief gedrag
Om te begrijpen welke genen deze verandering daadwerkelijk aandrijven, stelden de wetenschappers een set samen van 51 transitiegerelateerde genen specifiek voor galwegkanker en gebruikten deze om zowel individuele cellen als patiëntentumoren te scoren. Patiënten waarvan de tumoren hogere scores hadden, hadden slechtere overleving, waarmee het celprogramma werd verbonden met klinische uitkomst. Onder de genen die verrijkt waren in transitie-positieve cellen stak één genaamd PMEPA1 eruit. Hoge PMEPA1-niveaus waren geassocieerd met slechtere prognose en waren hoger in lymfeknoopmetastasen dan in de oorspronkelijke galwegtumoren. Wanneer de onderzoekers PMEPA1 verminderden in galwegkankercellijnen, groeiden de cellen trager, vormden ze minder kolonies en verloren ze grotendeels hun vermogen om te migreren en in kunstmatige membranen te invaseren en om tumoren in de longen van muizen te zaaien. Het verhogen van PMEPA1 had het tegenovergestelde effect.
Hoe PMEPA1 signalen binnen de cel herschakelt
Dieper gravend koppelde de studie PMEPA1 aan een bekend groeiregulerend pad dat draait om een eiwit genaamd YAP1. In gezonde weefsels houdt een veiligheidscircuit YAP1 grotendeels buiten de celkern, waardoor zijn vermogen om groeiovergangs- en invasiegenen aan te zetten beperkt blijft. De onderzoekers vonden dat PMEPA1 helpt dit veiligheidscircuit te verzwakken, waardoor meer YAP1 de kern kan binnendringen. Wanneer PMEPA1 werd uitgeschakeld, werden upstream-enzymen actiever, werd YAP1 zwaarder gemodificeerd en bleef het gevangen in het celplasma in plaats van in de kern. Deze verschuiving ging gepaard met een meer stationair, minder invasief profiel. Een chemische remmer van de veiligheidsenzymen keerde veel van de veranderingen veroorzaakt door PMEPA1-verlies om, wat bevestigt dat PMEPA1 het transitieprogramma bevordert door YAP1 naar de kern te sturen.
Een potentieel geneesmiddel om verspreiding te vertragen
Aangezien het transitieprogramma sterk samenhangt met therapieresistentie, vroeg het team vervolgens of bestaande middelen deze agressieve cellen selectief zouden kunnen treffen. Door geneesmiddelresponsdatabases te combineren met hun genhandtekeningen, identificeerden ze verschillende chemotherapiemiddelen, waaronder SN-38, de actieve vorm van irinotecan, als kandidaten. In celexperimenten verlaagde SN-38 merkers van de mobiele celtoestand, verminderde het de migratie- en invasiecapaciteit van de cellen en verlaagde het zowel PMEPA1- als YAP1-niveaus. Verdere gegevens suggereerden dat SN-38 interfereert met een transcriptiefactor genaamd FOS die normaal gesproken de productie van PMEPA1 verhoogt. In muismodellen van longmetastase aangedreven door PMEPA1-overexpressie verminderde behandeling met SN-38 de metastatische last en de PMEPA1-niveaus in tumordeposities.
Wat dit betekent voor patiënten
Eenvoudig gezegd toont deze studie aan dat een specifiek eiwit, PMEPA1, fungeert als een hoofdschakelaar die galwegkankercellen helpt losser te worden, weg te bewegen en nieuwe organen te koloniseren. Het doet dit door een ander eiwit, YAP1, vrijer de kern binnen te laten gaan en genen te activeren die invasie bevorderen. Omdat tumoren met sterkere versies van dit programma slechtere uitkomsten hebben, zouden PMEPA1 en zijn partners kunnen dienen als waarschuwingsmarkers en behandelingsdoelen. De bevinding dat SN-38, al gebruikt bij andere kankers, deze schakel kan dempen en metastase in modellen kan vertragen, wekt de mogelijkheid dat het verfijnen of combineren van dergelijke therapieën op termijn nauwkeuriger en effectievere opties kan bieden voor mensen met galwegkanker.
Bronvermelding: Xu, W., Ma, C., Li, P. et al. PMEPA1 modulates YAP1 nuclear translocation to disrupt EMT subtypes and promote metastasis in Biliary tract cancer. Cell Death Dis 17, 449 (2026). https://doi.org/10.1038/s41419-026-08684-3
Trefwoorden: galwegkanker, epitheliaal-mesenchymale transitie, PMEPA1, YAP1-signaaltransductie, SN-38