Clear Sky Science · zh
在表达 TrkA 的感觉神经元中,Ndfip2 通过控制 TrkA 信号和蛋白水平调节有害机械感觉
为何疼痛需要精细调节
疼痛看似令人讨厌,但它是身体最重要的警报系统之一。当这一警报出错——在慢性疼痛中声音过大,或在几乎感觉不到伤害的人身上过于安静——后果可能是毁灭性的。本研究发现了一种此前未知的分子,名为 Ndfip2,它有助于设定某些痛觉神经元的敏感度。了解这一内部调节旋钮的工作方式,研究者希望为开发在不关闭重要防御功能的前提下缓解疼痛的新疗法指明方向。
疼痛警报的关键角色
探测疼痛的神经元称为伤害感受器,位于脊髓旁的簇状结构中,当它们遇到针刺或极端高温等有害刺激时向大脑发送信息。许多此类细胞依赖一种称为神经生长因子(NGF)的生长信号及其细胞表面受体 TrkA。NGF 与 TrkA 结合会启动一连串信号,既帮助这些神经元发育,也决定它们对疼痛刺激的反应强度。TrkA 活性过强会放大疼痛,而过弱则会削弱疼痛感。由于直接阻断 NGF 在临床试验中引发了副作用,科学家们正寻求在细胞内部更安全地调节这一通路的方法。
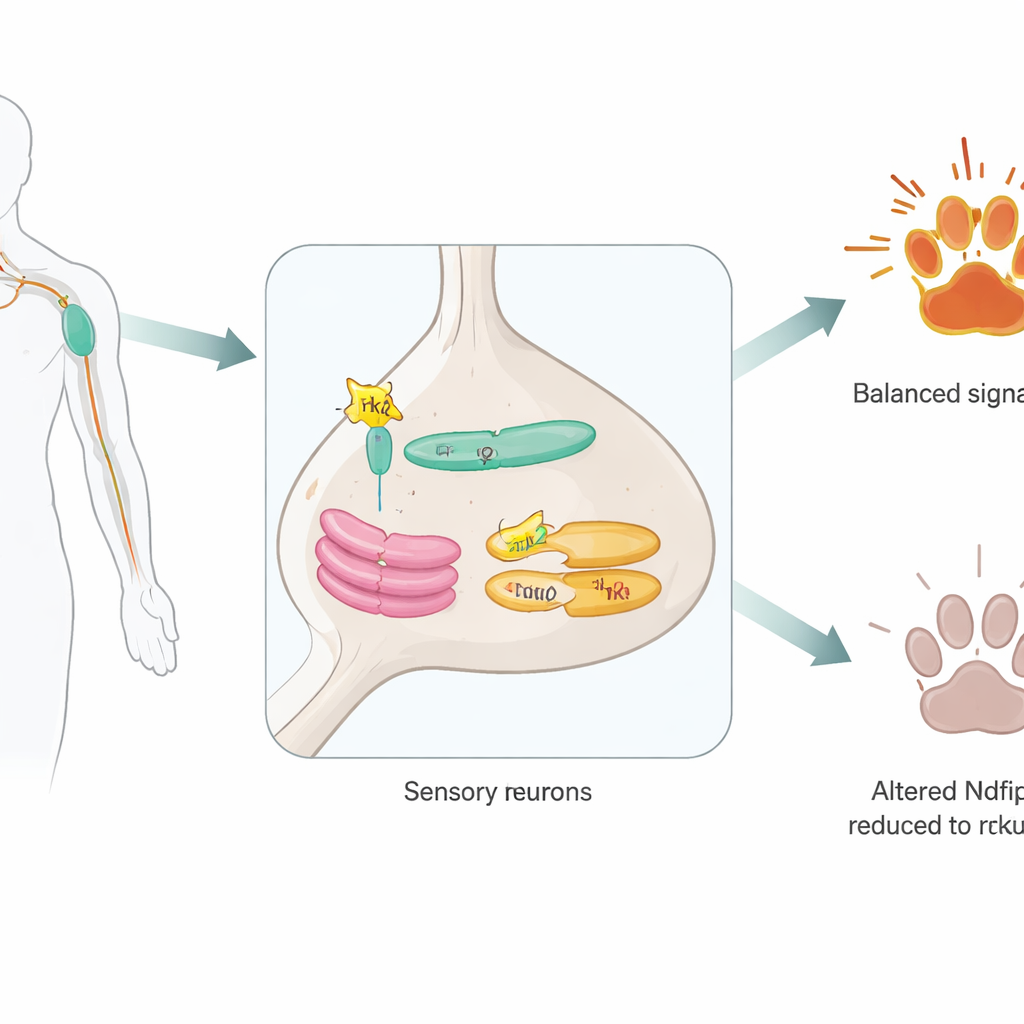
感觉神经元内的隐秘助力
研究人员将注意力集中在 Ndfip2——一种先前已知帮助酶将其他蛋白标记以便降解的蛋白质。他们首先确认 Ndfip2 存在于成年脊神经节的痛觉神经元中,并在携带 TrkA 的细胞中尤为富集。在这些神经元内,Ndfip2 聚集在细胞的内部运输中心——内质网和高尔基体——而不是细胞表面,并在那里与 TrkA 本身发生物理相互作用。有趣的是,雄性小鼠在这些神经元中表现出比雌性更高的 Ndfip2 基线水平,暗示该分子可能有助于已知的性别疼痛感差异。
在不麻痹所有感知的前提下削弱机械性疼痛
为了探究 Ndfip2 在活体中的作用,团队构建了仅在表达 TrkA 的细胞中去除 Ndfip2 的小鼠。这些动物生长正常,与同窝对照在运动或类焦虑行为上无显著差异。但当用校准的机械压力测试它们的足垫时,雄雌两性突变小鼠都需要更大的力才会撤回,显示对有害机械刺激的敏感性选择性降低。相比之下,对热刺激和大多数冷刺激的反应无明显变化,且在福尔马林注射的最初几分钟内,雌鼠的炎症性疼痛行为仅轻度增强。这一模式表明 Ndfip2 微调的是一条特定的疼痛通路——有害压力——而非广泛地钝化所有感觉形式。
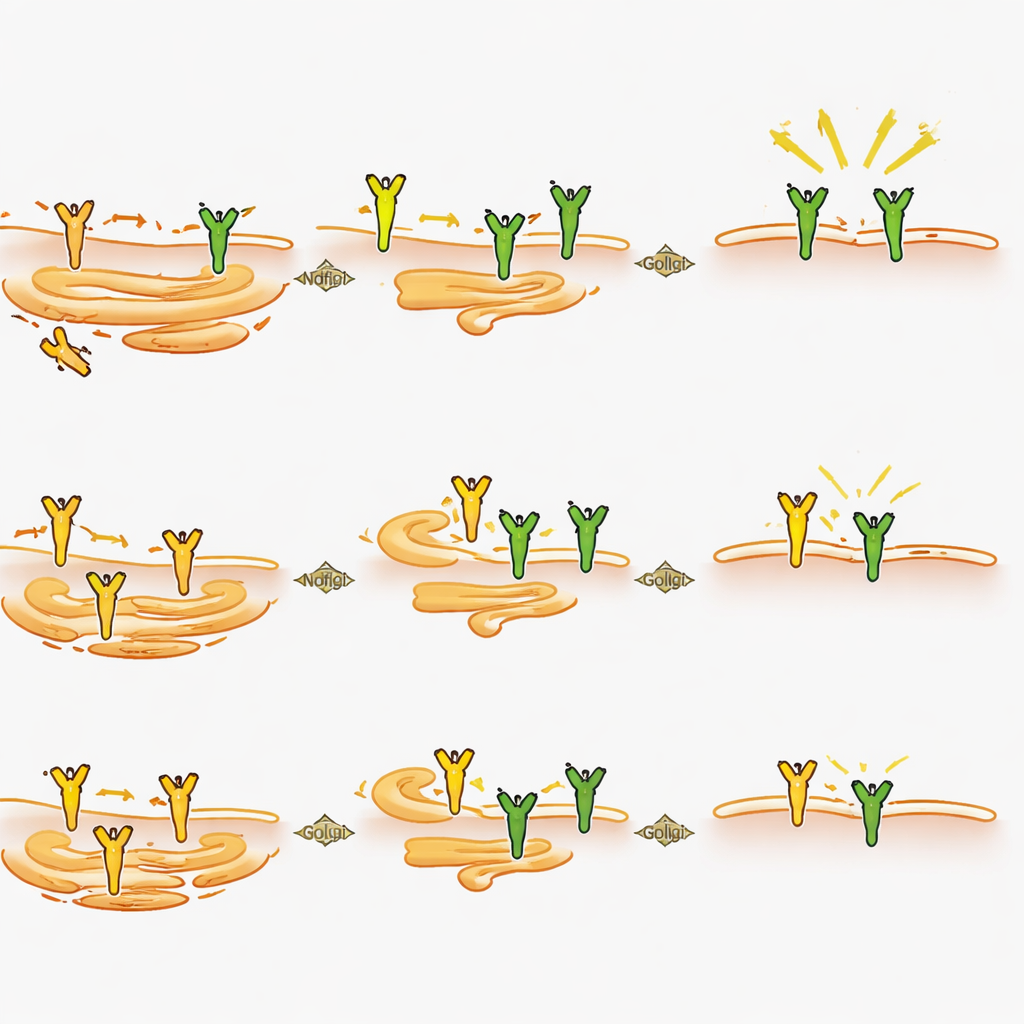
Ndfip2 如何从细胞内部塑造疼痛信号
细察这些神经元后,科学家发现删除 Ndfip2 会降低成年脊神经节中整体 TrkA 蛋白的含量,尤其在雄性中更为明显,尽管 TrkA 的基因表达仍保持正常水平。在培养神经元中,缺失 Ndfip2 会同时降低 TrkA 水平和 NGF 触发信号的强度,且同样在雄性中更为显著。出人意料的是,这一效应并非源于 TrkA 常见的降解标记变化。相反,细胞实验显示,额外的 Ndfip2 会使 TrkA 在未成熟、未糖基化的形式中累积,同时耗竭通常到达细胞表面的成熟加工形式。与此一致的是,在神经元中敲低 Ndfip2 会增加雄性膜上 TrkA 的比例。综上,这些发现表明 Ndfip2 调控 TrkA 在细胞内的化学成熟和运输,从而控制可用于感知 NGF 的功能性受体数量。
对未来疼痛治疗的意义
通过发现 Ndfip2 作为 NGF–TrkA 系统的内部调控因子,这项工作为理解身体如何校准疼痛敏感性,尤其是对有害机械刺激的敏感性,增加了新的层面。与其完全阻断 NGF,不如影响 Ndfip2 或 TrkA 成熟相关的环节,可能让临床医生能够在特定疼痛通路中微妙地减少过度信号传导,同时保留疼痛的保护功能。观察到的 Ndfip2 水平和效应的性别差异也强调了在未来疼痛治疗中根据生物学背景而非一刀切的重要性。
引用: Cañada-García, D., Hernández-García, A., Vicente-García, C. et al. Ndfip2 in TrkA-expressing sensory neurons regulates noxious mechanosensation through control of TrkA signaling and protein levels. Cell Death Dis 17, 437 (2026). https://doi.org/10.1038/s41419-026-08670-9
关键词: 机械性疼痛, 感觉神经元, 神经生长因子, TrkA 受体, 翻译后调控