Clear Sky Science · de
Ndfip2 in TrkA-exprimierenden sensorischen Neuronen reguliert schmerzhafte Mechanosensation durch Kontrolle von TrkA-Signalgebung und Proteinmengen
Warum Schmerz sorgfältig feinabgestimmt werden muss
Schmerz mag wie ein Ärgernis wirken, ist aber eines der wichtigsten Warnsysteme des Körpers. Wenn dieser Alarm falsch auslöst – entweder zu laut bei chronischen Schmerzen oder zu leise bei Menschen, die Verletzungen kaum spüren – können die Folgen verheerend sein. Diese Studie enthüllt ein bislang unbekanntes Molekül namens Ndfip2, das hilft, die Empfindlichkeit bestimmter schmerzaufnehmender Nervenzellen einzustellen. Indem Forschende verstehen, wie dieses innere Stellrad funktioniert, hoffen sie, Wege zu neuen Behandlungen aufzuzeigen, die Schmerzen lindern, ohne lebenswichtige Schutzfunktionen abzuschalten.
Wichtige Akteure im Schmerzalarm
Schmerz wahrnehmende Nervenzellen, sogenannte Nozizeptoren, liegen in Ganglien neben dem Rückenmark und senden Signale ans Gehirn, wenn sie schädliche Reize wie einen Nadelstich oder extreme Hitze wahrnehmen. Viele dieser Zellen sind abhängig von einem Wachstumsignal, dem Nervenwachstumsfaktor (NGF), und seinem Partner an der Zelloberfläche, dem Rezeptor TrkA. Wenn NGF an TrkA bindet, startet eine Signalkaskade, die diesen Neuronen bei der Entwicklung hilft und später bestimmt, wie stark sie auf schmerzhafte Reize reagieren. Zu viel TrkA-Aktivität kann Schmerz verstärken, zu wenig ihn abschwächen. Da eine direkte Blockade von NGF in klinischen Studien Nebenwirkungen verursachte, suchen Wissenschaftler nun nach sichereren Wegen, diesen Signalweg von innen heraus zu modulieren.
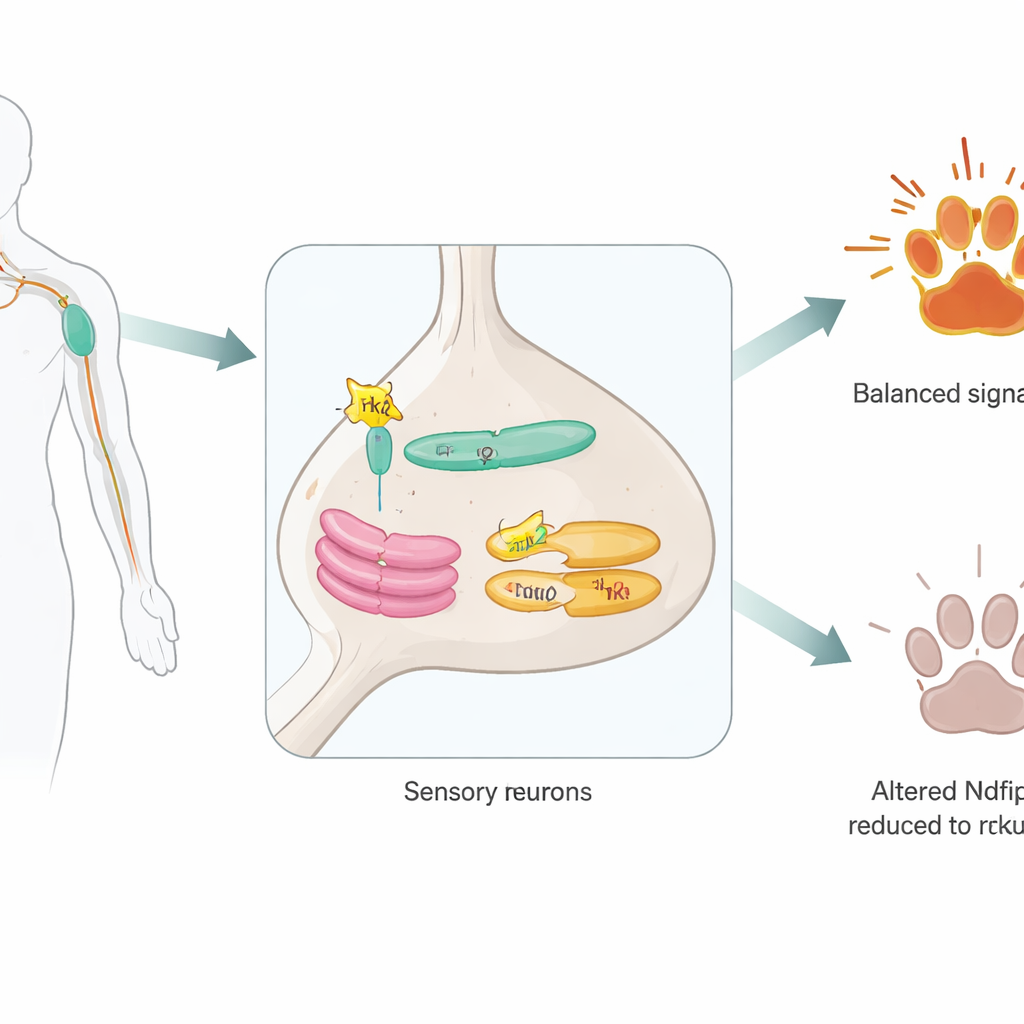
Ein verborgener Helfer in sensorischen Neuronen
Die Forschenden konzentrierten sich auf Ndfip2, ein Protein, das zuvor dafür bekannt war, Enzyme zu unterstützen, die andere Proteine für den Abbau markieren. Zunächst bestätigten sie, dass Ndfip2 in erwachsenen schmerzaufnehmenden Neuronen der dorsalen Wurzelganglien vorhanden ist und besonders in Zellen angereichert ist, die TrkA tragen. Innerhalb dieser Neuronen sammelt sich Ndfip2 in den inneren Versandzentren der Zelle – dem endoplasmatischen Retikulum und dem Golgi-Apparat – statt an der Zelloberfläche. Dort geht es eine physische Verbindung mit TrkA selbst ein. Interessanterweise zeigten männliche Mäuse höhere Ausgangslevel von Ndfip2 in diesen Neuronen als Weibchen, was darauf hindeutet, dass dieses Molekül zu bekannten Geschlechtsunterschieden in der Schmerzwahrnehmung beitragen könnte.
Mechanischen Schmerz dämpfen, ohne alles zu betäuben
Um Ndfip2s Rolle in lebenden Tieren zu untersuchen, erzeugte das Team Mäuse, bei denen Ndfip2 nur in Zellen entfernt wurde, die TrkA exprimieren. Diese Tiere entwickelten sich normal und zeigten keine Unterschiede in Bewegung oder angstähnlichem Verhalten im Vergleich zu ihren Wurfgeschwistern. Wurden jedoch die Pfoten mit kalibriertem mechanischem Druck getestet, benötigten sowohl männliche als auch weibliche Mutanten stärkere Kraft, bevor sie zurückzogen, was auf eine selektive Verringerung der Empfindlichkeit gegenüber schmerzhaften mechanischen Reizen hinweist. Im Gegensatz dazu blieben Reaktionen auf Hitze und die meisten Kältereize unverändert, und das Verhalten bei entzündlichem Schmerz war bei Weibchen nur in den ersten Minuten nach einer Formalininjektion leicht erhöht. Dieses Muster legt nahe, dass Ndfip2 einen spezifischen Schmerzkanal – schädlichen Druck – feinabstimmt, statt alle Formen der Empfindung pauschal zu dämpfen.
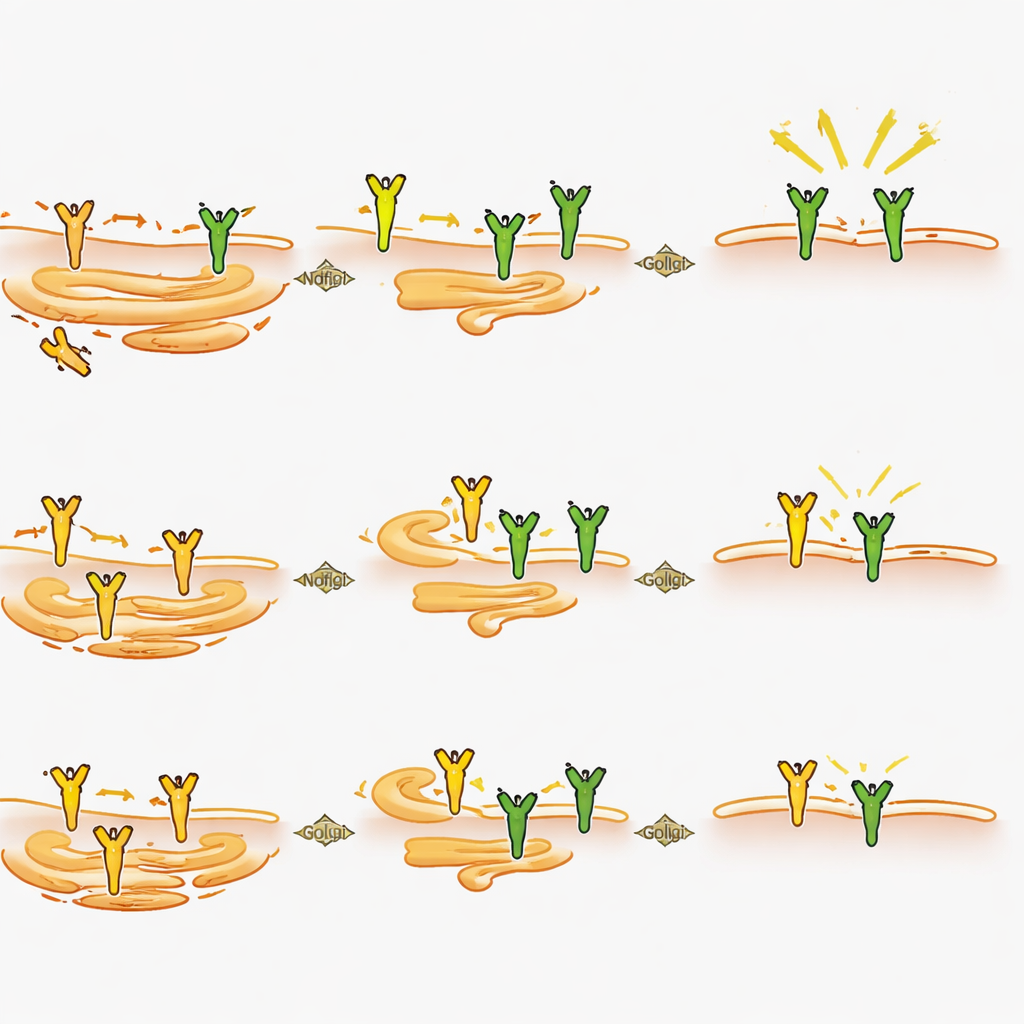
Wie Ndfip2 das Schmerzsignal aus dem Zellinneren formt
Bei genauerer Betrachtung der Neuronen fanden die Wissenschaftler heraus, dass das Löschen von Ndfip2 die Gesamtmenge an TrkA-Protein in den dorsalen Wurzelganglien erwachsener Mäuse verringerte, insbesondere bei Männchen, obwohl das TrkA-Gen weiterhin in normalem Maße exprimiert wurde. In kultivierten Neuronen reduzierte der Verlust von Ndfip2 sowohl die TrkA-Level als auch die Stärke des NGF- ausgelösten Signals, wiederum stärker bei Männchen. Überraschenderweise beruhte dieser Effekt nicht auf Veränderungen der üblichen Markierung von TrkA für den Abbau. Stattdessen zeigten Zellexperimente, dass zusätzliches Ndfip2 dazu führt, dass TrkA in einer unreifen, nicht-glykolysierten Form anhäuft, während die vollständig verarbeiteten Formen, die normalerweise die Zelloberfläche erreichen, reduziert werden. Entsprechend erhöhte das Herunterregulieren von Ndfip2 in Neuronen bei Männchen den Anteil von TrkA, der an der Membran vorhanden ist. Zusammen deuten diese Befunde darauf hin, dass Ndfip2 die chemische Reifung und das intrazelluläre Routing von TrkA reguliert und damit steuert, wie viel funktionsfähiger Rezeptor zur Wahrnehmung von NGF verfügbar ist.
Was das für zukünftige Schmerztherapien bedeutet
Indem diese Arbeit Ndfip2 als internen Regler des NGF–TrkA-Systems identifiziert, ergänzt sie das Verständnis darüber, wie der Körper die Schmerzempfindlichkeit kalibriert, insbesondere bei schädlichen mechanischen Reizen. Anstatt NGF vollständig zu blockieren, könnte das Beeinflussen von Ndfip2 oder verwandter Schritte in der TrkA-Reifung es ermöglichen, übermäßige Signalgebung in spezifischen Schmerzwegen dezent zu verringern und gleichzeitig die schützende Funktion von Schmerz insgesamt zu erhalten. Die beobachteten Geschlechtsunterschiede in Ndfip2-Leveln und -Effekten unterstreichen zudem, wie wichtig es ist, zukünftige Schmerzbehandlungen an den biologischen Kontext anzupassen, statt von Einheitslösungen auszugehen.
Zitation: Cañada-García, D., Hernández-García, A., Vicente-García, C. et al. Ndfip2 in TrkA-expressing sensory neurons regulates noxious mechanosensation through control of TrkA signaling and protein levels. Cell Death Dis 17, 437 (2026). https://doi.org/10.1038/s41419-026-08670-9
Schlüsselwörter: mechanischer Schmerz, sensorische Neuronen, Nervenwachstumsfaktor, TrkA-Rezeptor, posttranslationale Regulation