Clear Sky Science · sv
Ndfip2 i TrkA-uttryckande sensoriska neuroner reglerar smärtsam mekanosensation via kontroll av TrkA-signalering och proteinnivåer
Varför smärta behöver noggrann finjustering
Smärta kan kännas som ett besvär, men det är ett av kroppens viktigaste varningssystem. När detta larm går fel — antingen för starkt vid kronisk smärta eller för svagt hos personer som knappt känner skador — kan konsekvenserna bli förödande. Denna studie avslöjar en tidigare okänd molekyl, kallad Ndfip2, som hjälper till att ställa in känsligheten hos vissa smärtupptagande nervceller. Genom att förstå hur denna interna ratt fungerar hoppas forskarna kunna peka ut nya behandlingsvägar som lindrar smärta utan att stänga av viktiga försvarsfunktioner.
Nyckelspelare i smärtlarmet
Smärtdetekterande nervceller, kända som nociceptorer, sitter i kluster intill ryggmärgen och skickar meddelanden till hjärnan när de stöter på skadliga stimuli som ett stick eller extrem värme. Många av dessa celler är beroende av en tillväxtsignal som kallas nervtillväxtfaktor (NGF) och dess partner på cellytan, en receptor kallad TrkA. När NGF binder till TrkA startar en kaskad av signaler som hjälper dessa neuroner att utvecklas och senare bestämmer hur starkt de svarar på smärtsamma stimuli. För mycket TrkA-aktivitet kan förstärka smärta, medan för lite kan dämpa den. Eftersom direkt blockering av NGF har orsakat biverkningar i kliniska studier söker forskare nu säkrare sätt att justera denna bana inifrån cellen.
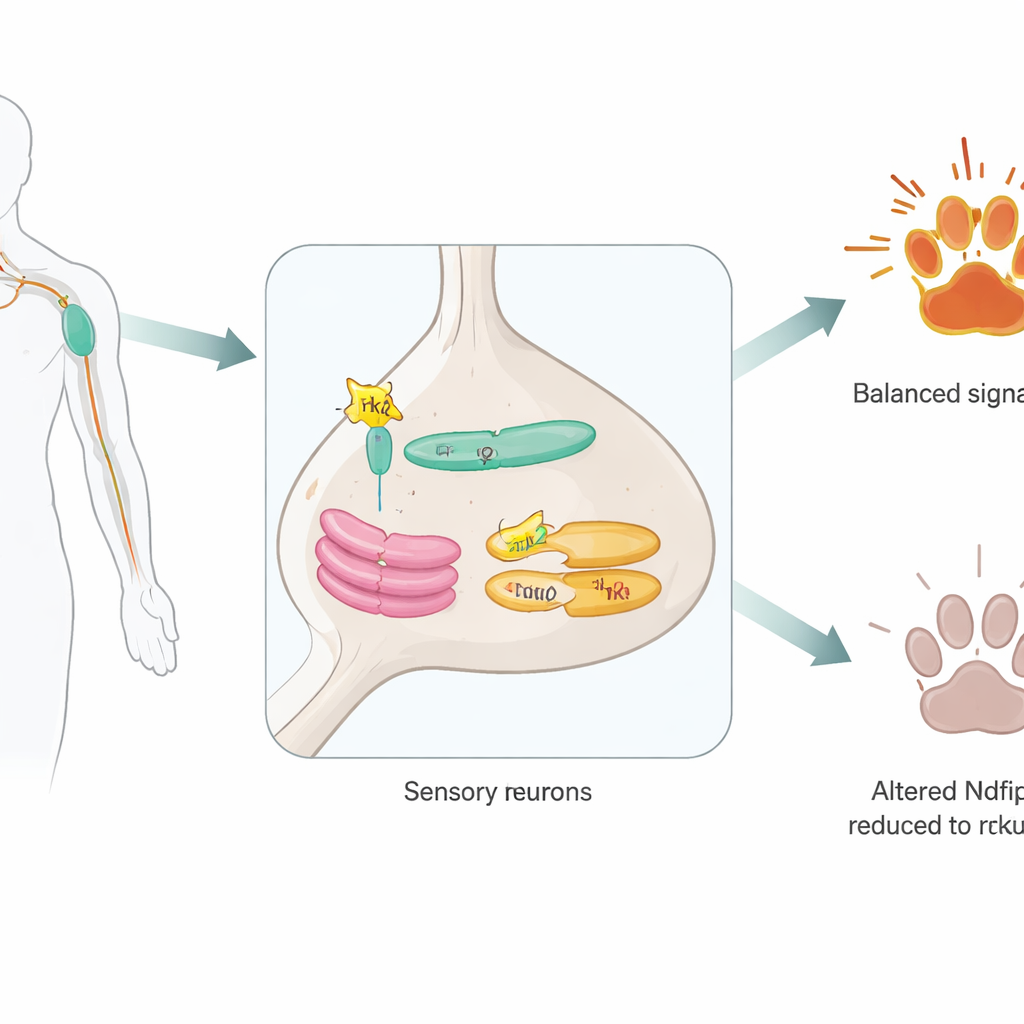
En dold hjälpare inne i sensoriska neuroner
Forskarna fokuserade på Ndfip2, ett protein tidigare känt för att hjälpa enzymer som märker andra proteiner för nedbrytning. De bekräftade först att Ndfip2 finns i vuxna smärtupptagande neuroner i dorsalrotsganglierna och är särskilt rikligt i celler som har TrkA. Inne i dessa neuroner klustrar Ndfip2 i cellens interna transportcenter — det endoplasmatiska retiklet och Golgiapparaten — snarare än vid cellytan. Där associerar det fysiskt med TrkA själv. Intressant nog visade hanliga möss högre basalt nivå av Ndfip2 i dessa neuroner än honor, vilket tyder på att denna molekyl kan bidra till kända könsskillnader i smärtuppfattning.
Sänka mekanisk smärta utan att bedöva allt
För att undersöka Ndfip2:s roll i levande djur konstruerade teamet möss där Ndfip2 togs bort endast från celler som uttrycker TrkA. Dessa djur växte normalt och visade inga skillnader i rörelse eller ångestliknande beteende jämfört med sina kullsyskon. Men när deras tassar testades med kalibrerat mekaniskt tryck krävde både hanar och honor med mutationen starkare kraft innan de drog tillbaka sig, vilket avslöjade en selektiv minskning i känslighet för smärtsamma mekaniska stimuli. Däremot var svaren på värme och de flesta kyla-tester oförändrade, och inflammatorisk smärtreaktion var endast måttligt förhöjd hos honor under de första minuterna efter en formalininjektion. Detta mönster tyder på att Ndfip2 finjusterar en specifik smärtkanal — skadligt tryck — snarare än att generellt dämpa alla former av sensation.
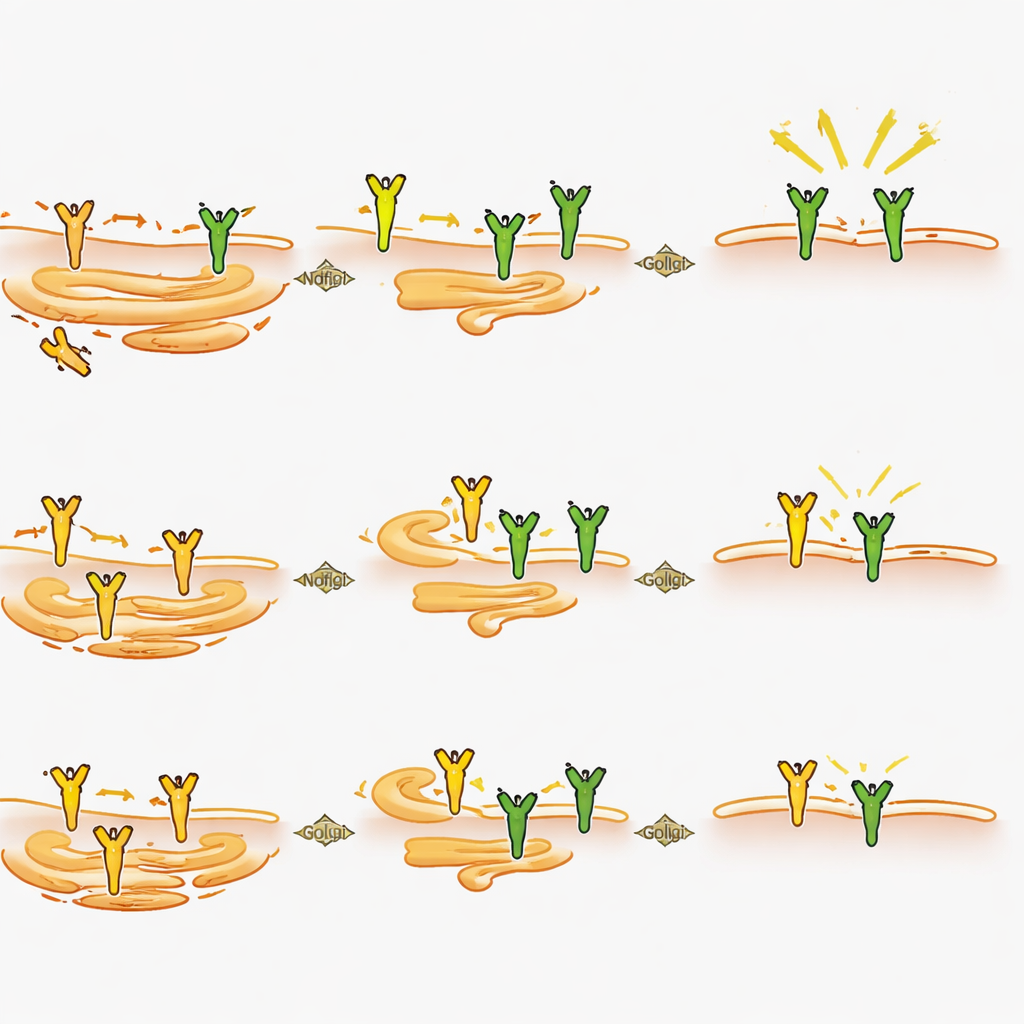
Hur Ndfip2 formar smärtsignalen inifrån cellen
När forskarna granskade neuronerna närmare fann de att borttagning av Ndfip2 sänkte den totala mängden TrkA-protein i vuxna dorsalrotsganglier, särskilt hos hanar, trots att genen för TrkA fortfarande uttrycktes på normala nivåer. I odlade neuroner minskade förlust av Ndfip2 både TrkA-nivåerna och styrkan i NGF-utlösta signaler, återigen mer uttalat hos hanar. Överraskande nog berodde denna effekt inte på förändringar i den vanliga märkningen av TrkA för nedbrytning. Istället visade experiment i celler att extra Ndfip2 får TrkA att ackumuleras i en omogen, icke-glykolyserad form samtidigt som de fullständigt processade versionerna som normalt når cellytan minskar. I överensstämmelse med detta ökade nedreglering av Ndfip2 i neuroner andelen TrkA som finns vid membranet hos hanar. Tillsammans pekar dessa fynd på Ndfip2 som en regulator av hur TrkA kemiskt mogna och dirigeras inne i cellen, och därigenom kontrollerar hur mycket funktionell receptor som finns tillgänglig för att känna av NGF.
Vad detta innebär för framtida smärtterapier
Genom att avslöja Ndfip2 som en intern kontrollant av NGF–TrkA-systemet tillför detta arbete ett nytt skikt i förståelsen av hur kroppen kalibrerar smärtkänslighet, särskilt för skadliga mekaniska stimuli. Istället för att helt blockera NGF kan påverkan på Ndfip2 eller relaterade steg i TrkA-mognad göra det möjligt för kliniker att subtilt minska överdriven signalering i specifika smärtvägar samtidigt som smärtans skyddande funktioner bevaras. De observerade könsskillnaderna i Ndfip2-nivåer och effekter betonar också vikten av att anpassa framtida smärtbehandlingar efter biologisk kontext snarare än att anta universella lösningar.
Citering: Cañada-García, D., Hernández-García, A., Vicente-García, C. et al. Ndfip2 in TrkA-expressing sensory neurons regulates noxious mechanosensation through control of TrkA signaling and protein levels. Cell Death Dis 17, 437 (2026). https://doi.org/10.1038/s41419-026-08670-9
Nyckelord: mekanisk smärta, sensoriska neuroner, nervtillväxtfaktor, TrkA-receptor, post-translationell reglering