Clear Sky Science · pt
Ndfip2 em neurônios sensoriais que expressam TrkA regula a mecanossensação nociva por meio do controle do sinal de TrkA e dos níveis proteicos
Por que a dor precisa de ajuste fino
A dor pode parecer um incômodo, mas é um dos sistemas de alerta mais importantes do corpo. Quando esse alarme falha — seja alto demais na dor crônica, seja apagado em pessoas que quase não sentem lesões — as consequências podem ser devastadoras. Este estudo revela uma molécula até então desconhecida, chamada Ndfip2, que ajuda a determinar a sensibilidade de certos neurônios que detectam a dor. Ao entender como esse ajuste interno funciona, os pesquisadores esperam apontar caminhos para novos tratamentos que aliviem a dor sem desligar defesas vitais.
Principais atores no alarme da dor
Neurônios detectores de dor, conhecidos como nociceptores, ficam agrupados ao lado da medula espinhal e enviam mensagens ao cérebro quando encontram estímulos nocivos como um alfinete ou calor extremo. Muitos desses neurônios dependem de um sinal de crescimento chamado fator de crescimento nervoso (NGF) e de seu parceiro na superfície celular, um receptor chamado TrkA. Quando o NGF se liga ao TrkA, é desencadeada uma cascata de sinais que ajuda esses neurônios a se desenvolverem e, posteriormente, a determinar com que intensidade respondem a estímulos dolorosos. Atividade excessiva de TrkA pode amplificar a dor, enquanto atividade insuficiente pode atenuá-la. Como bloquear o NGF diretamente provocou efeitos adversos em ensaios clínicos, os cientistas buscam agora maneiras mais seguras de ajustar essa via a partir do interior da célula.
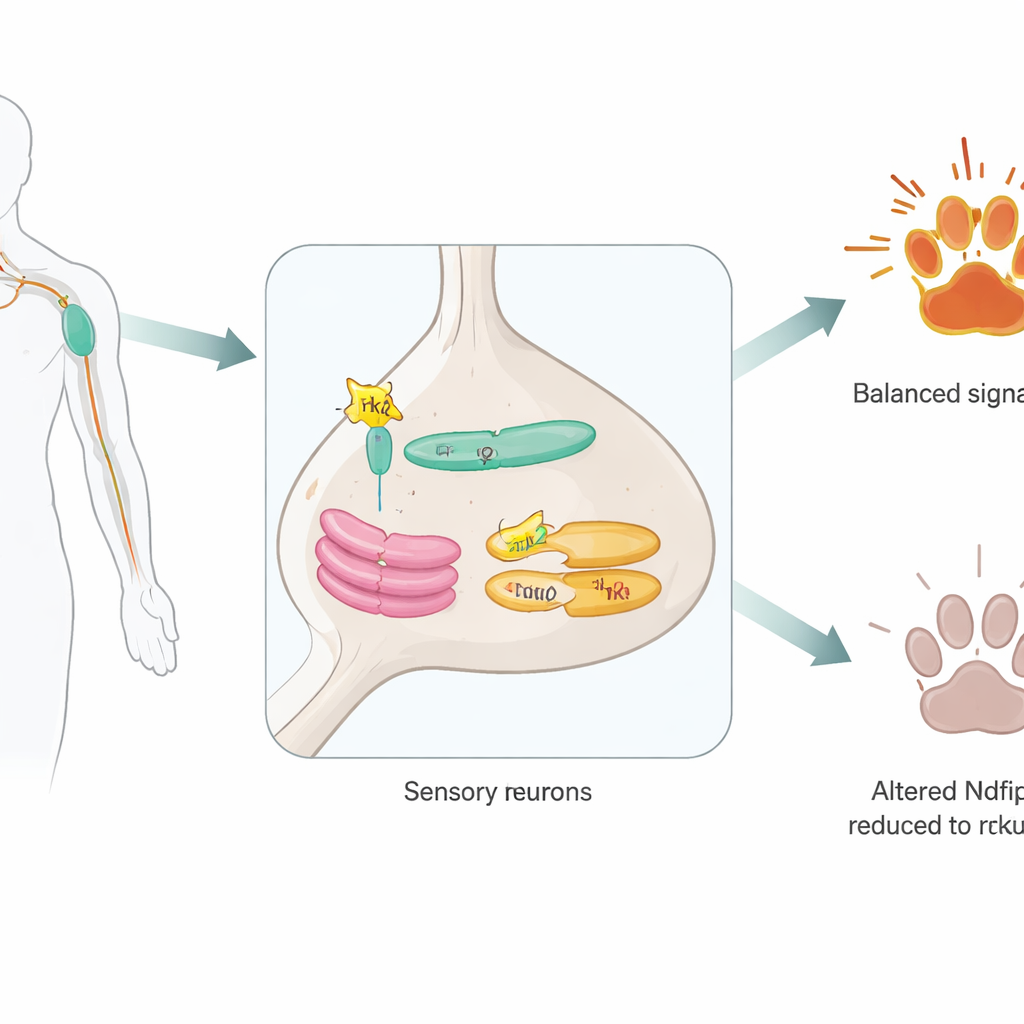
Um ajudante oculto dentro dos neurônios sensoriais
Os pesquisadores focaram no Ndfip2, uma proteína previamente conhecida por auxiliar enzimas que marcam outras proteínas para degradação. Primeiro confirmaram que o Ndfip2 está presente em neurônios adultos detectores de dor nos gânglios da raiz dorsal e é especialmente enriquecido em células que portam TrkA. Dentro desses neurônios, o Ndfip2 se concentra nos centros internos de remessa da célula — o retículo endoplasmático e o aparelho de Golgi — em vez de na superfície celular. Lá ele se associa fisicamente ao próprio TrkA. Curiosamente, camundongos machos apresentaram níveis basais maiores de Ndfip2 nesses neurônios do que fêmeas, sugerindo que essa molécula pode contribuir para diferenças conhecidas entre sexos na percepção da dor.
Reduzindo a dor mecânica sem entorpecer tudo
Para investigar o papel do Ndfip2 em animais vivos, a equipe criou camundongos nos quais o Ndfip2 foi removido apenas de células que expressam TrkA. Esses animais cresceram normalmente e não mostraram diferenças na locomoção ou em comportamentos análogos à ansiedade em comparação com seus irmãos de ninhada. Mas, quando suas patas foram testadas com pressão mecânica calibrada, tanto machos quanto fêmeas mutantes precisaram de força maior antes de se retirar, revelando uma redução seletiva da sensibilidade a estímulos mecânicos nocivos. Em contraste, as respostas ao calor e à maior parte dos testes de frio permaneceram inalteradas, e o comportamento de dor inflamatória aumentou apenas modestamente nas fêmeas nos minutos iniciais após uma injeção de formalina. Esse padrão sugere que o Ndfip2 ajusta finamente um canal específico da dor — pressão nociva — em vez de amortecer amplamente todas as formas de sensação.
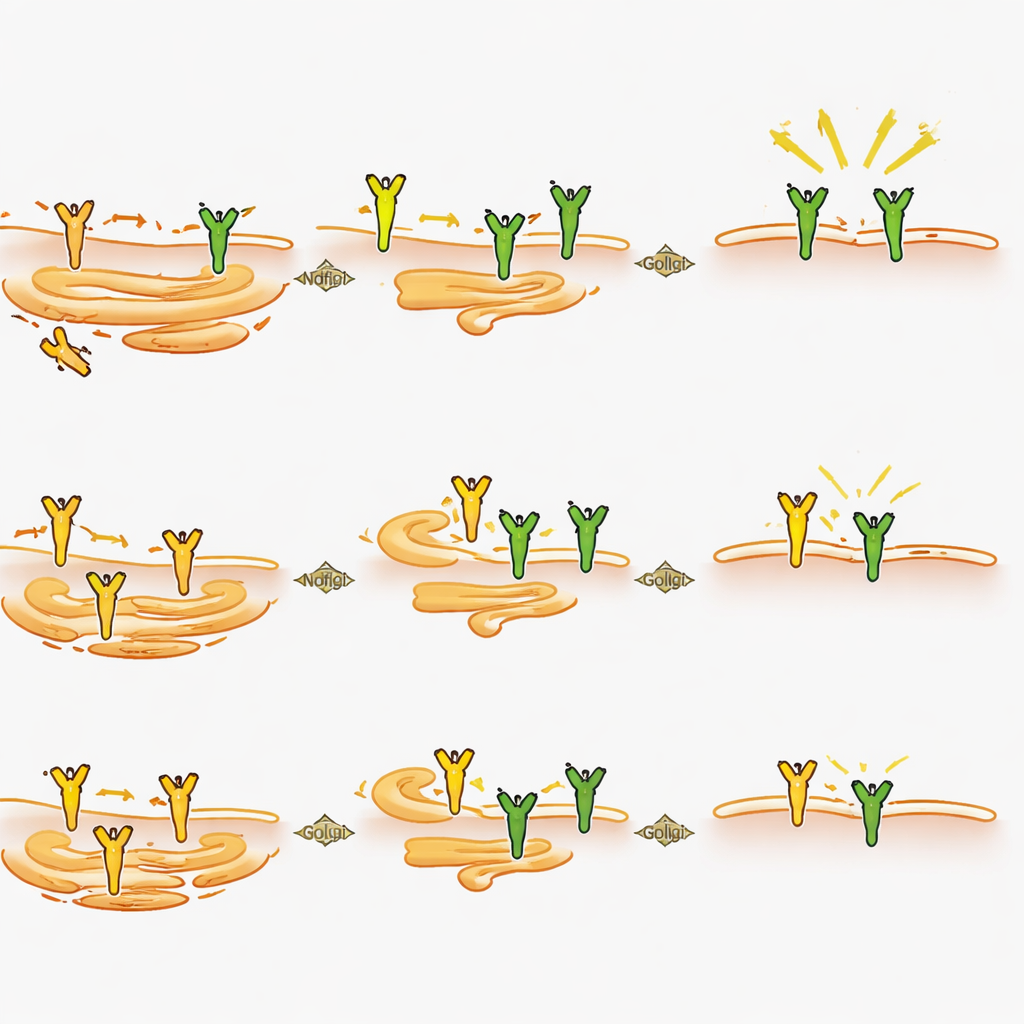
Como o Ndfip2 molda o sinal de dor de dentro da célula
Analisando os neurônios mais de perto, os cientistas descobriram que a deleção de Ndfip2 reduziu a quantidade geral de proteína TrkA nos gânglios da raiz dorsal de adultos, particularmente em machos, embora o gene de TrkA continuasse sendo expresso em níveis normais. Em neurônios em cultura, a perda de Ndfip2 reduziu tanto os níveis de TrkA quanto a intensidade da sinalização desencadeada pelo NGF, novamente de forma mais marcante em machos. Surpreendentemente, esse efeito não derivou de alterações na marcação usual de TrkA para degradação. Em vez disso, experimentos em células revelaram que o excesso de Ndfip2 faz com que o TrkA se acumule em uma forma imatura e não glicosilada, enquanto esgota as versões totalmente processadas que normalmente chegam à superfície celular. Em consonância com isso, reduzir o Ndfip2 em neurônios aumentou a fração de TrkA presente na membrana em machos. Em conjunto, esses achados apontam o Ndfip2 como um regulador de como o TrkA é quimicamente maturado e roteado dentro da célula, controlando assim quanto receptor funcional está disponível para detectar o NGF.
O que isso significa para futuras terapias da dor
Ao revelar o Ndfip2 como um controlador interno do sistema NGF–TrkA, este trabalho adiciona uma nova camada de compreensão sobre como o corpo calibra a sensibilidade à dor, especialmente para estímulos mecânicos nocivos. Em vez de bloquear o NGF de modo absoluto, influenciar o Ndfip2 ou etapas relacionadas na maturação do TrkA pode permitir aos clínicos reduzir sutilmente a sinalização excessiva em vias específicas da dor, preservando a função protetora da dor no geral. As diferenças observadas entre sexos nos níveis e efeitos do Ndfip2 também ressaltam a importância de adaptar futuras terapias da dor ao contexto biológico, em vez de presumir soluções universais.
Citação: Cañada-García, D., Hernández-García, A., Vicente-García, C. et al. Ndfip2 in TrkA-expressing sensory neurons regulates noxious mechanosensation through control of TrkA signaling and protein levels. Cell Death Dis 17, 437 (2026). https://doi.org/10.1038/s41419-026-08670-9
Palavras-chave: dor mecânica, neurônios sensoriais, fator de crescimento neural, receptor TrkA, regulação pós-traducional