Clear Sky Science · es
Ndfip2 en neuronas sensoriales que expresan TrkA regula la mecanosensación nociva mediante el control de la señalización y los niveles de proteína de TrkA
Por qué el dolor necesita un ajuste cuidadoso
El dolor puede parecer una molestia, pero es uno de los sistemas de alarma más importantes del cuerpo. Cuando esta alarma falla —sea porque suena demasiado fuerte en el dolor crónico, o demasiado débil en personas que casi no sienten lesiones— las consecuencias pueden ser devastadoras. Este estudio descubre una molécula hasta ahora desconocida, llamada Ndfip2, que ayuda a fijar la sensibilidad de ciertas neuronas que detectan el dolor. Al entender cómo funciona este regulador interno, los investigadores esperan señalar vías hacia nuevos tratamientos que alivien el dolor sin apagar defensas vitales.
Actores clave en la alarma del dolor
Las células nerviosas que detectan el dolor, conocidas como nociceptores, se agrupan junto a la médula espinal y envían mensajes al cerebro cuando encuentran estímulos dañinos como una punción o un calor extremo. Muchas de estas células dependen de una señal de crecimiento llamada factor de crecimiento nervioso (NGF) y de su receptor en la superficie celular, TrkA. Cuando NGF se une a TrkA, se desencadena una cascada de señales que ayudan a estas neuronas a desarrollarse y más tarde determinan con qué intensidad responden a estímulos dolorosos. Demasiada actividad de TrkA puede amplificar el dolor, mientras que muy poca puede embotarlo. Dado que bloquear NGF directamente ha causado efectos secundarios en ensayos clínicos, los científicos buscan ahora formas más seguras de ajustar esta vía desde dentro de la célula.
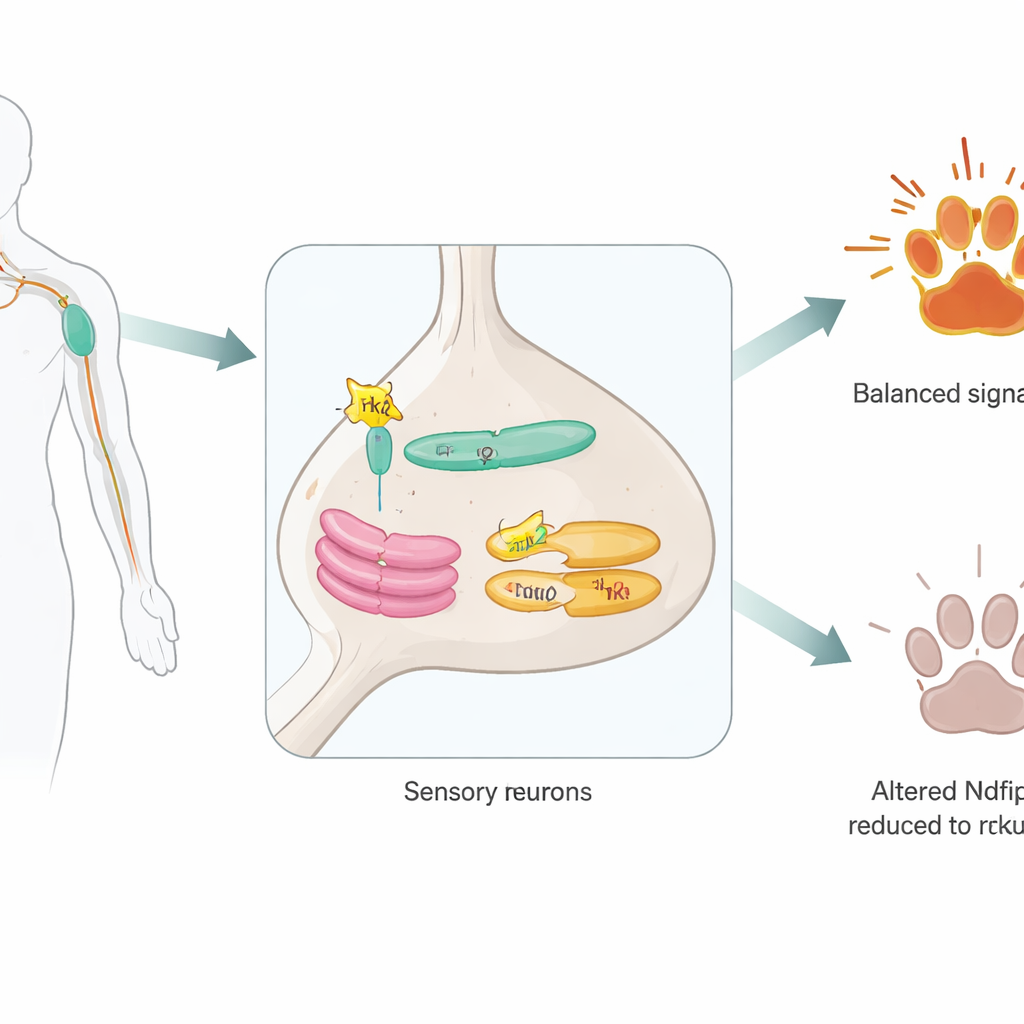
Un ayudante oculto dentro de las neuronas sensoriales
Los investigadores se centraron en Ndfip2, una proteína conocida previamente por ayudar a enzimas que marcan otras proteínas para su degradación. Primero confirmaron que Ndfip2 está presente en neuronas adultas que detectan el dolor en los ganglios de la raíz dorsal y que está especialmente enriquecida en las células que portan TrkA. Dentro de estas neuronas, Ndfip2 se agrupa en los centros de envío internos de la célula —el retículo endoplásmico y el aparato de Golgi— en lugar de en la superficie celular. Allí se asocia físicamente con el propio TrkA. De forma intrigante, los ratones machos mostraron niveles basales más altos de Ndfip2 en estas neuronas que las hembras, lo que sugiere que esta molécula podría contribuir a las diferencias sexuales conocidas en la percepción del dolor.
Reducir el dolor mecánico sin anestesiarlo todo
Para sondear el papel de Ndfip2 en animales vivos, el equipo diseñó ratones en los que Ndfip2 fue eliminado solo de las células que expresan TrkA. Estos animales crecieron con normalidad y no mostraron diferencias en movimiento o comportamiento similar a ansiedad en comparación con sus hermanos. Pero cuando sus patas se probaron con presión mecánica calibrada, tanto los ratones mutantes machos como hembras necesitaron una fuerza mayor antes de retirarse, revelando una reducción selectiva de la sensibilidad a estímulos mecánicos nocivos. En contraste, las respuestas al calor y la mayoría de las pruebas de frío no cambiaron, y el comportamiento de dolor inflamatorio se incrementó solo modestamente en hembras durante los primeros minutos tras una inyección de formalina. Este patrón sugiere que Ndfip2 ajusta finamente un canal específico del dolor —la presión nociva— en lugar de embotar de forma general todos los tipos de sensación.
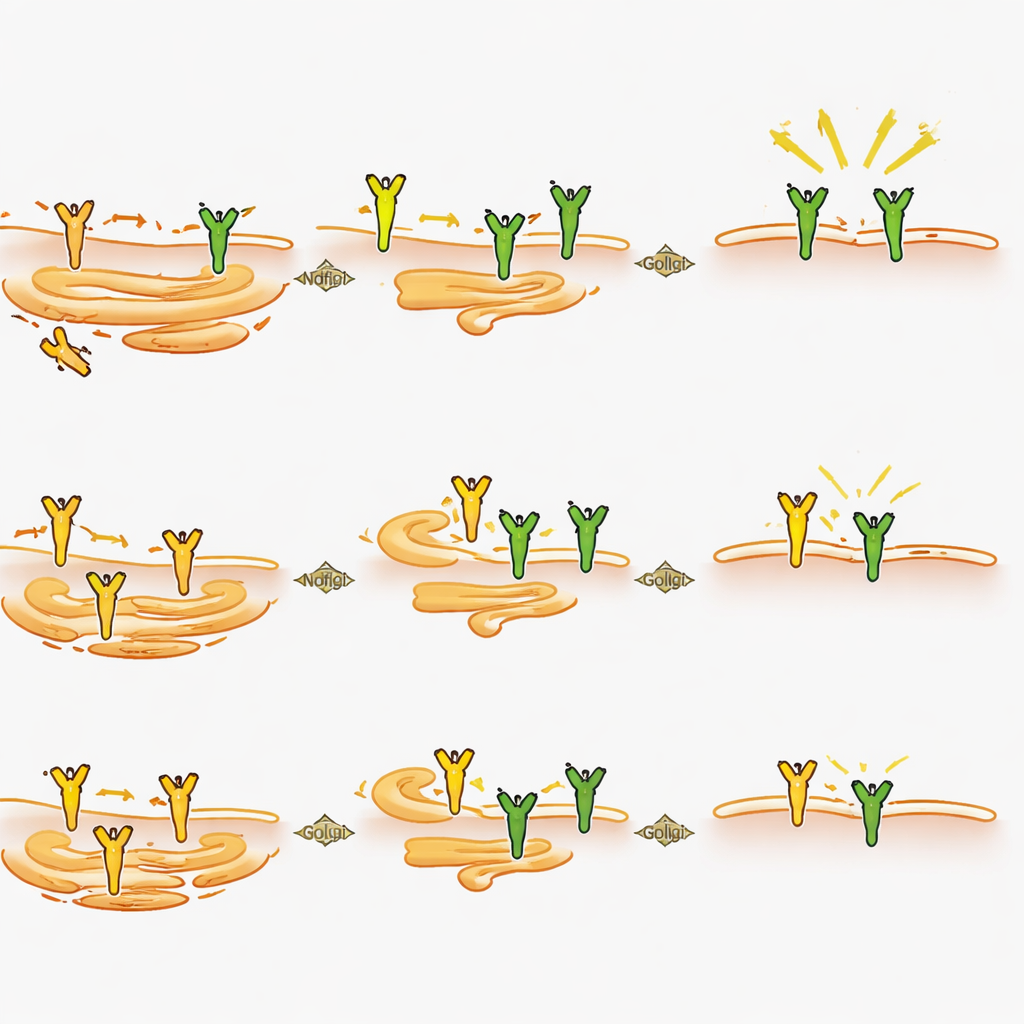
Cómo Ndfip2 moldea la señal del dolor desde dentro de la célula
Al observar más de cerca las neuronas, los científicos hallaron que la eliminación de Ndfip2 redujo la cantidad total de proteína TrkA en los ganglios de la raíz dorsal en adultos, particularmente en machos, aunque el gen de TrkA seguía expresándose a niveles normales. En neuronas en cultivo, la pérdida de Ndfip2 disminuyó tanto los niveles de TrkA como la intensidad de la señalización desencadenada por NGF, de nuevo con mayor marcado en machos. Sorprendentemente, este efecto no provenía de cambios en el marcado habitual de TrkA para su degradación. En cambio, experimentos en células mostraron que un exceso de Ndfip2 hace que TrkA se acumule en una forma inmadura no glicosilada mientras agota las versiones totalmente procesadas que normalmente llegan a la superficie celular. En consonancia con esto, la reducción de Ndfip2 en neuronas aumentó la fracción de TrkA presente en la membrana en machos. En conjunto, estos hallazgos señalan a Ndfip2 como un regulador de cómo TrkA se madura químicamente y se enruta dentro de la célula, controlando así cuánto receptor funcional está disponible para detectar NGF.
Qué significa esto para futuras terapias del dolor
Al descubrir a Ndfip2 como un controlador interno del sistema NGF–TrkA, este trabajo añade una nueva capa de comprensión sobre cómo el cuerpo calibra la sensibilidad al dolor, especialmente frente a estímulos mecánicos nocivos. En lugar de bloquear NGF de forma directa, influir en Ndfip2 o en pasos relacionados de la maduración de TrkA podría permitir a los clínicos reducir sutilmente la señalización excesiva en vías específicas del dolor mientras se preserva la función protectora del dolor en general. Las diferencias sexuales observadas en los niveles y efectos de Ndfip2 también subrayan la importancia de adaptar futuros tratamientos del dolor al contexto biológico en lugar de asumir soluciones universales.»
Cita: Cañada-García, D., Hernández-García, A., Vicente-García, C. et al. Ndfip2 in TrkA-expressing sensory neurons regulates noxious mechanosensation through control of TrkA signaling and protein levels. Cell Death Dis 17, 437 (2026). https://doi.org/10.1038/s41419-026-08670-9
Palabras clave: dolor mecánico, neuronas sensoriales, factor de crecimiento nervioso, receptor TrkA, regulación postraduccional