Clear Sky Science · nl
Ndfip2 in TrkA-expressing sensorische neuronen reguleert nociceptieve mechanosensatie via controle van TrkA-signalerings- en eiwitniveaus
Waarom pijn zorgvuldig bijgesteld moet worden
Pijn kan als een hinderlijk signaal aanvoelen, maar het is een van de belangrijkste waarschuwingssystemen van het lichaam. Wanneer dit alarm fout gaat—ofwel te luid bij chronische pijn, ofwel te zwak bij mensen die bijna geen blessures voelen—kan dat verstrekkende gevolgen hebben. Deze studie onthult een eerder onbekend molecuul, Ndfip2, dat helpt de gevoeligheid van bepaalde pijn-sensorische zenuwcellen in te stellen. Door te begrijpen hoe dit interne draaiknopje werkt, hopen onderzoekers de weg te wijzen naar nieuwe behandelingen die pijn verlichten zonder de vitale bescherming van het lichaam uit te schakelen.
Belangrijke spelers in het pijnalarm
Pijn-detecterende zenuwcellen, bekend als nociceptoren, liggen in clusters naast het ruggenmerg en sturen berichten naar de hersenen wanneer ze schadelijke prikkels zoals een prik of extreme hitte tegenkomen. Veel van deze cellen zijn afhankelijk van een groeisignaal, de zenuwgroeifactor (NGF), en diens partner op het celoppervlak, de receptor TrkA. Wanneer NGF aan TrkA bindt, start dat een cascade van signalen die deze neuronen helpen zich te ontwikkelen en later bepalen hoe sterk ze op pijnprikkels reageren. Te veel TrkA-activiteit kan pijn versterken, terwijl te weinig die pijn kan verminderen. Omdat directe blokkade van NGF in klinische proeven bijwerkingen heeft veroorzaakt, zoeken wetenschappers nu naar veiligere manieren om deze route van binnenuit bij te sturen.
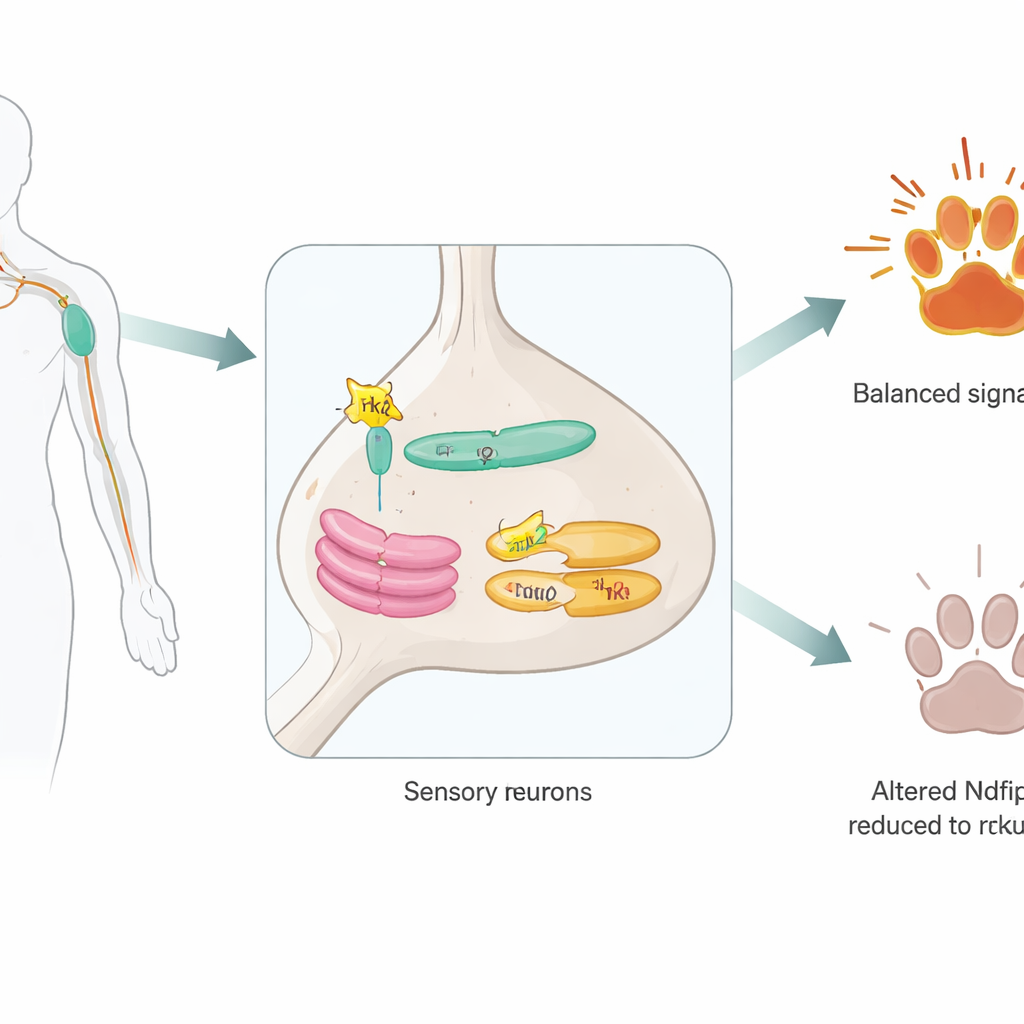
Een verborgen helper binnen sensorische neuronen
De onderzoekers richtten zich op Ndfip2, een eiwit dat eerder werd herkend als assistent van enzymen die andere eiwitten voor afbraak markeren. Ze bevestigden eerst dat Ndfip2 aanwezig is in volwassen pijn-sensorische neuronen in de dorsale wortelganglia en met name verrijkt is in cellen die TrkA dragen. Binnen deze neuronen clustert Ndfip2 in de interne verzendcentra van de cel—het endoplasmatisch reticulum en het Golgi-apparaat—in plaats van aan het celoppervlak. Daar associeert het zich fysiek met TrkA zelf. Intrigerend genoeg toonden mannelijke muizen hogere basale Ndfip2-niveaus in deze neuronen dan vrouwtjes, wat suggereert dat dit molecuul kan bijdragen aan bekende sekseverschillen in pijnwaarneming.
Mechanische pijn verlagen zonder alles te verdoven
Om Ndfip2’s rol in levende dieren te onderzoeken, maakten de onderzoekers muizen waarbij Ndfip2 alleen werd verwijderd uit cellen die TrkA tot expressie brengen. Deze dieren ontwikkelden zich normaal en vertoonden geen verschillen in beweging of angstig gedrag vergeleken met hun nestgenoten. Maar wanneer hun poten werden getest met gekalibreerde mechanische druk, hadden zowel mannelijke als vrouwelijke mutantmuizen sterkere kracht nodig voordat ze hun poot terugtrokken, wat wijst op een selectieve vermindering van de gevoeligheid voor nociceptieve mechanische prikkels. Daarentegen bleven reacties op hitte en de meeste koudtetstests ongewijzigd, en ontstekingspijnachtig gedrag was alleen licht verhoogd bij vrouwtjes tijdens de eerste minuten van een formaline-injectie. Dit patroon suggereert dat Ndfip2 een specifiek kanaal van pijn bijstelt—schadelijke druk—zonder alle vormen van sensatie breed te dempen.
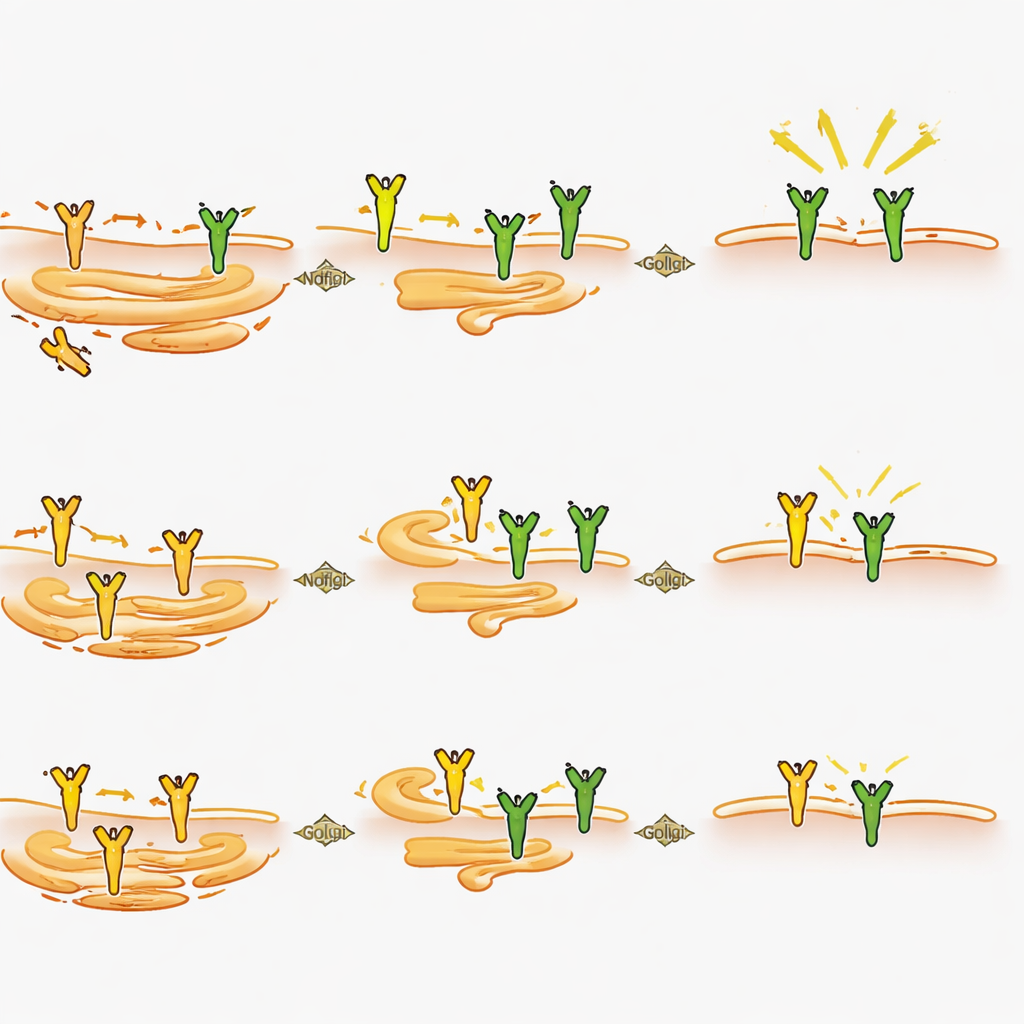
Hoe Ndfip2 het pijnsignaal van binnenuit vormt
Nauwkeuriger onderzoek aan de neuronen liet zien dat het verwijderen van Ndfip2 de totale hoeveelheid TrkA-eiwit in volwassen dorsale wortelganglia verlaagde, vooral bij mannelijke dieren, hoewel het gen voor TrkA nog op normale niveaus werd tot expressie gebracht. In gekweekte neuronen verminderde het verlies van Ndfip2 zowel TrkA-niveaus als de sterkte van NGF-geïnduceerde signalering, opnieuw duidelijker bij mannetjes. Verrassend genoeg bleek dit effect niet voort te komen uit veranderingen in de gebruikelijke markering van TrkA voor afbraak. In plaats daarvan toonden celexperimenten aan dat extra Ndfip2 ervoor zorgt dat TrkA ophoopt in een onvolwassen, niet-glycosyleerde vorm, terwijl de volledig verwerkte versies die normaal het celoppervlak bereiken worden uitgeput. In overeenstemming hiermee verhoogde het neerwaarts reguleren van Ndfip2 in neuronen het aandeel TrkA aanwezig aan het membraan bij mannetjes. Gezamenlijk wijzen deze bevindingen op Ndfip2 als een regulator van hoe TrkA chemisch wordt gerijpt en gerouteerd binnen de cel, en daarmee controleert hoeveel functionele receptor beschikbaar is om NGF waar te nemen.
Wat dit betekent voor toekomstige pijntherapieën
Door Ndfip2 te identificeren als een interne regelaar van het NGF–TrkA-systeem voegt dit werk een nieuwe laag van begrip toe over hoe het lichaam pijngevoeligheid kalibreert, vooral voor schadelijke mechanische prikkels. In plaats van NGF volledig te blokkeren, kan beïnvloeding van Ndfip2 of verwante stappen in TrkA-rijping klinische mogelijkheden bieden om overmatige signalering in specifieke pijnroutes subtiel te verminderen, terwijl de beschermende functie van pijn behouden blijft. De geobserveerde sekseverschillen in Ndfip2-niveaus en -effecten benadrukken ook het belang van het afstemmen van toekomstige pijnbehandelingen op biologische context in plaats van uit te gaan van één oplossing voor iedereen.
Bronvermelding: Cañada-García, D., Hernández-García, A., Vicente-García, C. et al. Ndfip2 in TrkA-expressing sensory neurons regulates noxious mechanosensation through control of TrkA signaling and protein levels. Cell Death Dis 17, 437 (2026). https://doi.org/10.1038/s41419-026-08670-9
Trefwoorden: mechanische pijn, sensorische neuronen, zenuwgroeifactor, TrkA-receptor, post-translationele regulatie