Clear Sky Science · ar
دور Ndfip2 في الخلايا العصبية الحسية المعبرة عن TrkA في تنظيم الإحساس الميكانيكي المؤلم عبر التحكم في إشارة ومستويات بروتين TrkA
لماذا يحتاج الألم إلى معايرة دقيقة
قد يبدو الألم مصدر إزعاج، لكنه واحد من أهم أنظمة التحذير في الجسم. عندما يعمل هذا الإنذار بشكل خاطئ — إما بصوت عالٍ جدًا في الألم المزمن، أو خافتًا جدًا لدى الأشخاص الذين لا يشعرون بالإصابات — يمكن أن تكون النتائج مدمرة. تكشف هذه الدراسة عن جزيء لم يُعرف سابقًا يُدعى Ndfip2 يساعد على ضبط حساسية نوع معين من خلايا العصب الحسية. من خلال فهم كيفية عمل هذا الضابط الداخلي، يأمل الباحثون في الإشارة نحو علاجات جديدة تريح الألم دون تعطيل الدفاعات الحيوية.
الجهات الفاعلة الرئيسية في إنذار الألم
تقع خلايا الأعصاب المكتشفة للألم، المعروفة باسم مستقبلات الأذى (nociceptors)، في عناقيد بجانب الحبل الشوكي وترسل رسائل إلى الدماغ عند مواجهة محفزات ضارة مثل وخزة أو حرارة شديدة. تعتمد العديد من هذه الخلايا على إشارة نمو تُسمى عامل نمو الأعصاب (NGF) وشريكها على سطح الخلية، مستقبل يُدعى TrkA. عند ارتباط NGF بـ TrkA، يطلق ذلك سلسلة من الإشارات التي تساعد هذه الخلايا العصبية على التطور وتحديد مدى استجابتها لاحقًا للمحرضات المؤلمة. يمكن أن يؤدي نشاط TrkA المفرط إلى تضخيم الألم، بينما يؤدي القليل منه إلى تخفيفه. ونظرًا لأن حجب NGF مباشرة تسبب في آثار جانبية في التجارب السريرية، يبحث العلماء الآن عن طرق أكثر أمانًا لضبط هذا المسار من داخل الخلية.
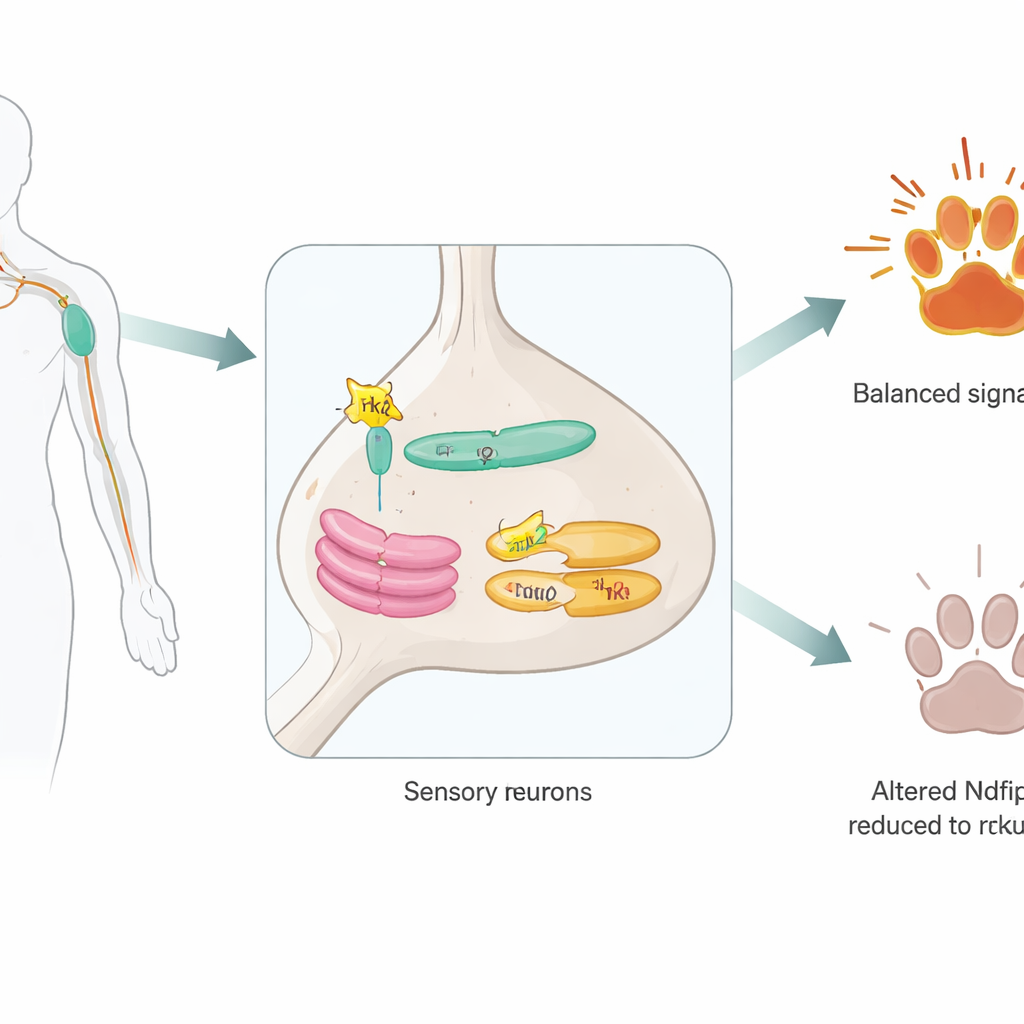
مساعد مخفي داخل الخلايا الحسية
ركز الباحثون على Ndfip2، وهو بروتين كان معروفًا سابقًا بمساعدة الإنزيمات التي تضع علامات على بروتينات أخرى لتتحلل. أكدوا أولاً أن Ndfip2 موجود في الخلايا العصبية الحساسة للألم في العقد الجذرية الظهرية لدى البالغين، وأنه مبرز بشكل خاص في الخلايا الحاملة لـ TrkA. داخل هذه الخلايا، يتجمع Ndfip2 في مراكز الشحن الداخلية للخلية — الشبكة الإندوبلازمية وجهاز غولجي — بدلًا من السطح الخلوي. هناك يرتبط فعليًا بـ TrkA نفسه. ومن المثير للاهتمام أن الفئران الذكور أظهرت مستويات أساسية أعلى من Ndfip2 في هذه الخلايا مقارنة بالإناث، ما يوحي بأن هذا الجزيء قد يساهم في اختلافات الجنس المعروفة في إدراك الألم.
خفض الألم الميكانيكي دون تخدير كل شيء
لاختبار دور Ndfip2 في الحيوانات الحية، صمم الفريق فئرانًا أُزيل فيها Ndfip2 فقط من الخلايا التي تعبر عن TrkA. نمت هذه الحيوانات بشكل طبيعي ولم تظهر اختلافات في الحركة أو السلوك الشبيه بالقلق مقارنة بإخوانها. لكن عند اختبار باطن أقدامهم بضغط ميكانيكي مضبوط، احتاجت الفئران الطافرة من كلا الجنسين لقوة أكبر قبل السحب، ما أظهر انخفاضًا انتقائيًا في الحساسية للمحفزات الميكانيكية المؤلمة. بالمقابل، لم تتغير الاستجابات للحرارة ومعظم اختبارات البرودة، وكان سلوك الألم الالتهابي مرتفعًا بشكل طفيف فقط لدى الإناث في الدقائق الأولى بعد حقن الفورمالين. تشير هذه النمطية إلى أن Ndfip2 يضبط قناة محددة من قنوات الألم — الضغط الضار — بدلاً من تخدير كل أشكال الإحساس بشكل واسع.
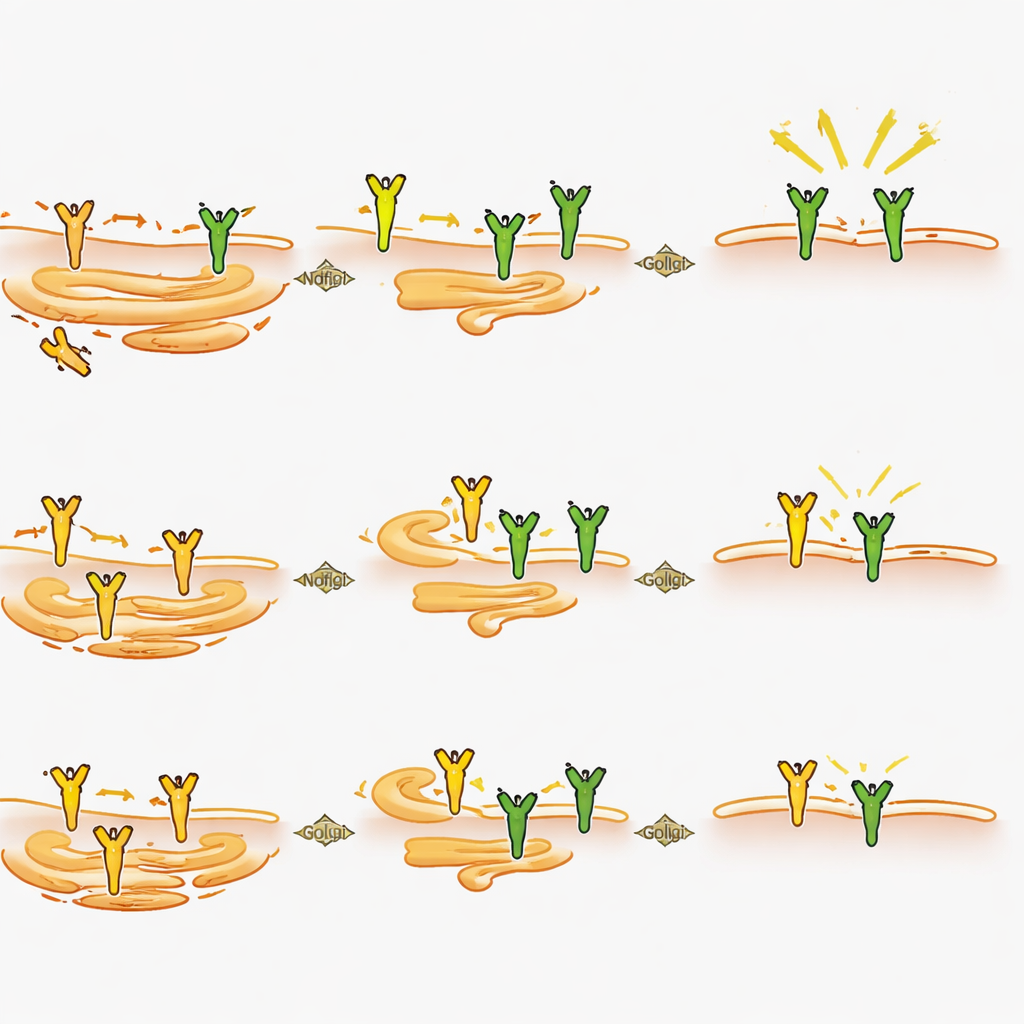
كيف يشكل Ndfip2 إشارة الألم من داخل الخلية
بالنظر عن قرب إلى الخلايا العصبية، وجد العلماء أن حذف Ndfip2 خفض كمية بروتين TrkA الإجمالية في العقد الجذرية الظهرية البالغة، لا سيما لدى الذكور، رغم أن جين TrkA ظل معبرًا عنه بمستويات طبيعية. في الخلايا المزروعة، أدى فقدان Ndfip2 إلى خفض كل من مستويات TrkA وقوة الإشارات التي يطلقها NGF، مرة أخرى بشكل أوضح لدى الذكور. بشكل مفاجئ، لم ينجم هذا التأثير عن تغييرات في الوسوم المعتادة التي توضع على TrkA لتفكيكه. بدلاً من ذلك، أظهرت تجارب في خلايا أن زيادة Ndfip2 تسبب تراكم TrkA في شكل غير ناضج وغير مكسو بالسكر (غير مُغلف بالغلَيكوزيل) بينما تستنزف الأشكال المعالجة بالكامل التي تصل عادة إلى سطح الخلية. وبما يتوافق مع ذلك، أدى خفض Ndfip2 في الخلايا العصبية إلى زيادة نسبة TrkA الموجودة على الغشاء في الذكور. مجتمعة، تشير هذه النتائج إلى أن Ndfip2 ينظم كيفية نضج TrkA كيميائيًا وتوجيهه داخل الخلية، وبالتالي يحدد مقدار المستقبل الوظيفي المتاح لاستشعار NGF.
ما يعنيه هذا لعلاجات الألم المستقبلية
من خلال الكشف عن Ndfip2 كضابط داخلي لنظام NGF–TrkA، تضيف هذه الدراسة طبقة جديدة من الفهم لكيفية معايرة الجسم لحساسية الألم، خاصة للمحفزات الميكانيكية الضارة. بدلاً من حظر NGF بشكل مباشر، قد يسمح التأثير على Ndfip2 أو خطوات مرتبطة بنضج TrkA للسريريين بخفض الإشارات المفرطة بدقة في مسارات ألم محددة مع الحفاظ على الوظيفة الوقائية للألم بشكل عام. كما تؤكد الاختلافات المرصودة بين الجنسين في مستويات Ndfip2 وتأثيراتها أهمية تكييف العلاجات المستقبلية للألم حسب السياق البيولوجي بدلًا من افتراض حل واحد يناسب الجميع.
الاستشهاد: Cañada-García, D., Hernández-García, A., Vicente-García, C. et al. Ndfip2 in TrkA-expressing sensory neurons regulates noxious mechanosensation through control of TrkA signaling and protein levels. Cell Death Dis 17, 437 (2026). https://doi.org/10.1038/s41419-026-08670-9
الكلمات المفتاحية: ألم ميكانيكي, الخلايا العصبية الحسية, عامل نمو الأعصاب, مستقبل TrkA, تنظيم بعد الترجمة