Clear Sky Science · fr
Ndfip2 dans les neurones sensoriels exprimant TrkA régule la mécanosensation nociceptive par le contrôle du signalement et des niveaux de protéine TrkA
Pourquoi la douleur doit être finement réglée
La douleur peut sembler être une nuisance, mais elle est l’un des systèmes d’alerte les plus importants du corps. Lorsque cette alarme se déclenche de façon inappropriée — trop forte dans la douleur chronique, ou trop faible chez des personnes qui ressentent à peine les blessures — les conséquences peuvent être dévastatrices. Cette étude met en lumière une molécule jusqu’alors inconnue, appelée Ndfip2, qui contribue à régler la sensibilité de certains neurones sensoriels. En comprenant comment fonctionne ce réglage interne, les chercheurs espèrent ouvrir la voie à de nouveaux traitements qui soulagent la douleur sans neutraliser les défenses vitales.
Acteurs clés de l’alarme douloureuse
Les cellules nerveuses détectant la douleur, appelées nocicepteurs, se trouvent en amas près de la moelle épinière et envoient des messages au cerveau lorsqu’elles rencontrent des stimuli nocifs comme une piqûre ou une chaleur extrême. Nombre d’entre elles dépendent d’un signal de croissance appelé facteur de croissance nerveuse (NGF) et de son partenaire à la surface cellulaire, un récepteur nommé TrkA. Lorsque NGF se lie à TrkA, cela déclenche une cascade de signaux qui aide ces neurones à se développer et, plus tard, à déterminer l’intensité de leur réponse aux stimuli douloureux. Une activité excessive de TrkA peut amplifier la douleur, tandis qu’une activité insuffisante peut l’atténuer. Parce que le blocage direct de NGF a provoqué des effets indésirables lors d’essais cliniques, les scientifiques cherchent maintenant des moyens plus sûrs d’ajuster cette voie depuis l’intérieur de la cellule.
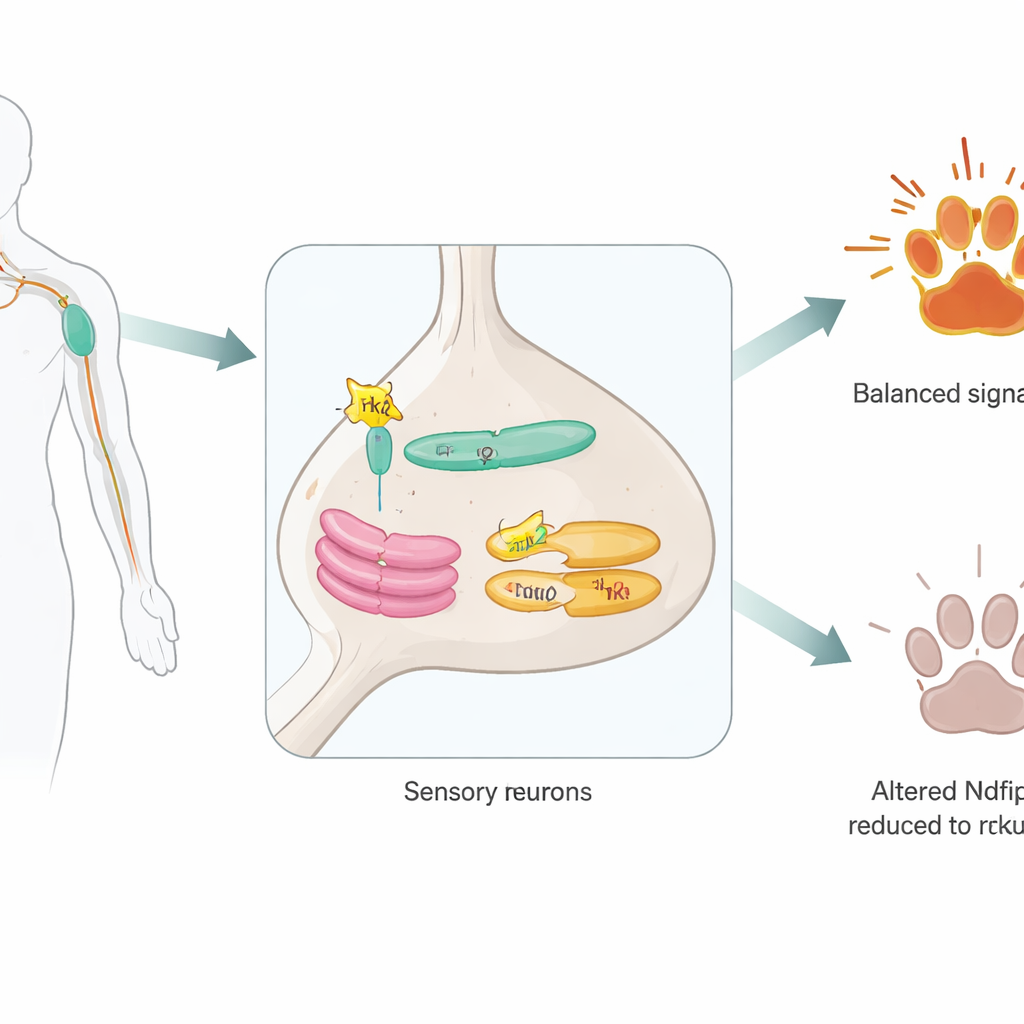
Un assistant caché à l’intérieur des neurones sensoriels
Les chercheurs se sont concentrés sur Ndfip2, une protéine connue auparavant pour aider des enzymes qui marquent d’autres protéines en vue de leur dégradation. Ils ont d’abord confirmé que Ndfip2 est présente dans les neurones adultes sensibles à la douleur des ganglions rachidiens dorsaux et est particulièrement enrichie dans les cellules qui portent TrkA. Au sein de ces neurones, Ndfip2 se regroupe dans les centres d’expédition internes de la cellule — le réticulum endoplasmique et l’appareil de Golgi — plutôt qu’à la surface cellulaire. Là, elle s’associe physiquement à TrkA lui-même. Fait intrigant, les souris mâles présentaient des niveaux basaux de Ndfip2 plus élevés dans ces neurones que les femelles, ce qui suggère que cette molécule pourrait contribuer aux différences sexuelles connues dans la perception de la douleur.
Réduire la douleur mécanique sans tout engourdir
Pour étudier le rôle de Ndfip2 chez l’animal vivant, l’équipe a conçu des souris chez lesquelles Ndfip2 a été supprimée uniquement dans les cellules exprimant TrkA. Ces animaux ont grandi normalement et n’ont présenté aucune différence de locomotion ou de comportement lié à l’anxiété par rapport à leurs congénères. Mais lorsqu’on a appliqué une pression mécanique calibrée sur leurs pattes, les souris mutantes mâles et femelles ont nécessité une force plus élevée avant de se retirer, révélant une réduction sélective de la sensibilité aux stimuli mécaniques nocifs. En revanche, les réponses à la chaleur et à la plupart des tests au froid sont restées inchangées, et le comportement de douleur inflammatoire n’a été que légèrement augmenté chez les femelles durant les premières minutes suivant une injection de formol. Ce profil suggère que Ndfip2 module spécifiquement une voie de la douleur — la pression nocive — plutôt que d’atténuer de manière globale toutes les formes de sensation.
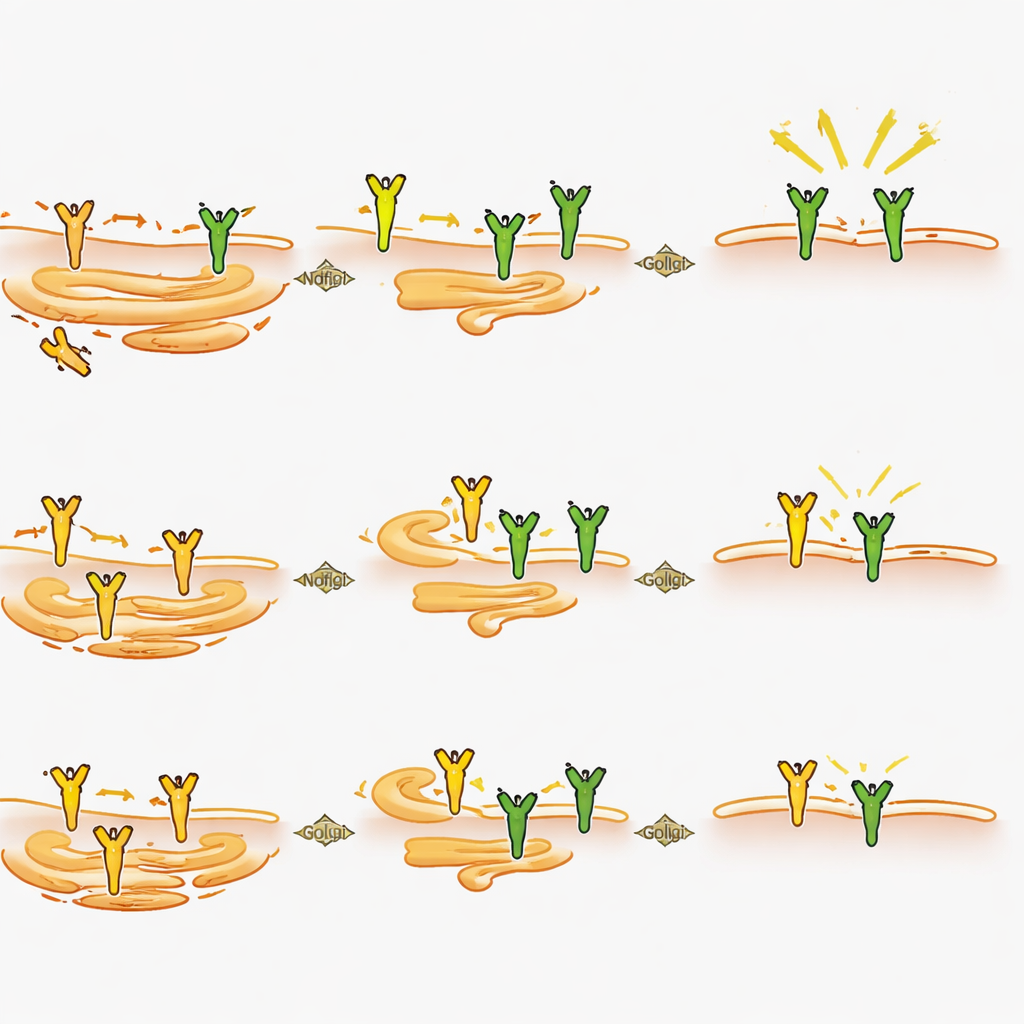
Comment Ndfip2 façonne le signal de la douleur depuis l’intérieur de la cellule
En examinant de plus près les neurones, les scientifiques ont constaté que la suppression de Ndfip2 réduisait la quantité totale de protéine TrkA dans les ganglions rachidiens dorsaux adultes, en particulier chez les mâles, alors même que le gène codant TrkA était toujours exprimé à des niveaux normaux. En cultures neuronales, la perte de Ndfip2 diminuait à la fois les niveaux de TrkA et l’intensité du signal déclenché par NGF, là encore de manière plus marquée chez les mâles. De manière surprenante, cet effet ne provenait pas de modifications du marquage habituel de TrkA en vue de sa dégradation. Au lieu de cela, des expériences en cellule ont montré qu’un excès de Ndfip2 entraîne l’accumulation de TrkA sous une forme immature non glycosylée tout en diminuant les formes entièrement traitées qui atteignent normalement la surface cellulaire. Concordant avec cela, l’inhibition de Ndfip2 dans les neurones augmentait la fraction de TrkA présente à la membrane chez les mâles. Ensemble, ces résultats désignent Ndfip2 comme un régulateur de la maturation chimique et du routage intracellulaire de TrkA, contrôlant ainsi la quantité de récepteur fonctionnel disponible pour détecter NGF.
Ce que cela signifie pour les thérapies antalgiques futures
En révélant Ndfip2 comme un régulateur interne du système NGF–TrkA, ce travail apporte un nouveau niveau de compréhension sur la façon dont l’organisme calibre la sensibilité à la douleur, en particulier pour les stimuli mécaniques nocifs. Plutôt que de bloquer NGF de manière frontale, cibler Ndfip2 ou des étapes similaires de la maturation de TrkA pourrait permettre aux cliniciens de réduire subtilement les signaux excessifs dans des voies douloureuses spécifiques tout en préservant la fonction protectrice globale de la douleur. Les différences observées selon le sexe dans les niveaux et les effets de Ndfip2 soulignent également l’importance d’adapter les futurs traitements de la douleur au contexte biologique plutôt que d’adopter des solutions universelles.
Citation: Cañada-García, D., Hernández-García, A., Vicente-García, C. et al. Ndfip2 in TrkA-expressing sensory neurons regulates noxious mechanosensation through control of TrkA signaling and protein levels. Cell Death Dis 17, 437 (2026). https://doi.org/10.1038/s41419-026-08670-9
Mots-clés: douleur mécanique, neurones sensoriels, facteur de croissance nerveuse, récepteur TrkA, régulation post-traductionnelle