Clear Sky Science · pl
Ndfip2 w neuronach czuciowych wyrażających TrkA reguluje mechanonocicepcję poprzez kontrolę sygnalizacji i poziomów białka TrkA
Dlaczego ból wymaga precyzyjnego dostrajania
Ból może wydawać się uciążliwy, ale jest jednym z najważniejszych systemów ostrzegawczych organizmu. Gdy ten alarm zawodzi — albo jest zbyt głośny w przewlekłym bólu, albo zbyt cichy u osób słabo odczuwających urazy — skutki mogą być druzgocące. W badaniu odkryto wcześniej nieznaną cząsteczkę nazwaną Ndfip2, która pomaga ustawić czułość pewnych neurONów czucia bólu. Poznanie działania tego wewnętrznego pokrętła może wskazać drogę do nowych terapii łagodzących ból bez wyłączania niezbędnych mechanizmów obronnych.
Kluczowi gracze w alarmie bólowym
Komórki wykrywające ból, zwane nocyceptorami, leżą w skupiskach obok rdzenia kręgowego i wysyłają sygnały do mózgu, gdy napotkają szkodliwe bodźce, takie jak ukłucie czy ekstremalne ciepło. Wiele z tych komórek zależy od sygnału wzrostowego nazwanego czynnikiem wzrostu nerwów (NGF) oraz jego partnera na powierzchni komórki — receptora TrkA. Gdy NGF wiąże się z TrkA, uruchamia kaskadę sygnałów, które pomagają tym neuronům rozwijać się i później określają, jak silnie odpowiadają na bodźce bólowe. Zbyt wysoka aktywność TrkA może wzmacniać ból, podczas gdy zbyt niska może go osłabić. Ponieważ bezpośrednie blokowanie NGF wywołało działania niepożądane w badaniach klinicznych, naukowcy poszukują teraz bezpieczniejszych sposobów dostrajania tej ścieżki od wewnątrz komórki.
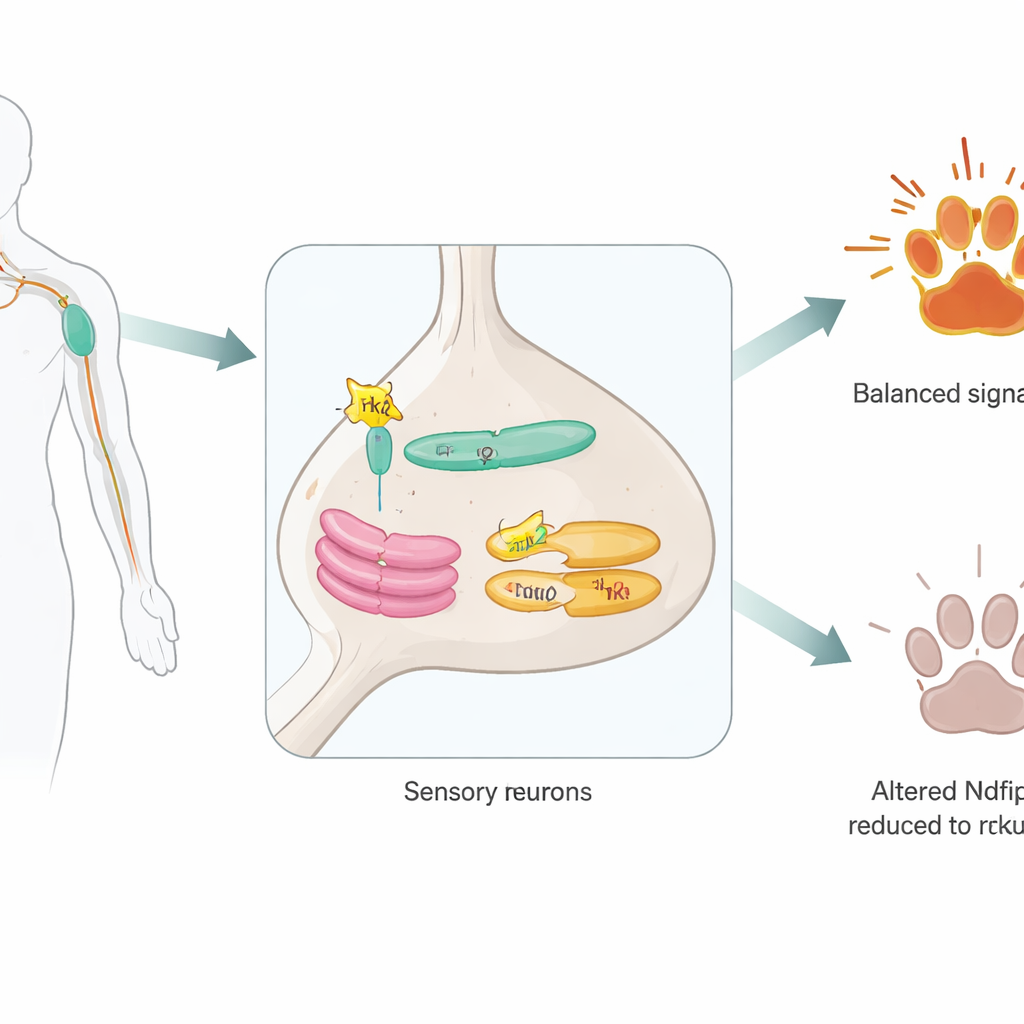
Ukryty pomocnik wewnątrz neuronów czuciowych
Naukowcy skupili się na Ndfip2 — białku wcześniej znanym z pomagania enzymom oznaczającym inne białka do degradacji. Najpierw potwierdzili, że Ndfip2 występuje w dorosłych neuronach czucia bólu w zwojach rdzeniowych (dorsal root ganglia) i jest szczególnie wzbogacone w komórkach niosących TrkA. W tych neuronach Ndfip2 skupia się w wewnętrznych centrach wysyłkowych komórki — retikulum endoplazmatycznym i aparacie Golgiego — zamiast na powierzchni komórki. Tam fizycznie wiąże się z samym TrkA. Co ciekawe, samce myszy wykazywały wyższe wyjściowe poziomy Ndfip2 w tych neuronach niż samice, co sugeruje, że cząsteczka ta może przyczyniać się do znanych różnic płciowych w percepcji bólu.
Przyciszanie bólu mechanicznego bez ogólnego odrętwienia
Aby zbadać rolę Ndfip2 u żywych zwierząt, zespół zmodyfikował myszy tak, aby Ndfip2 został usunięty tylko z komórek wyrażających TrkA. Zwierzęta te rozwijały się normalnie i nie wykazywały różnic w ruchu ani zachowaniach przypominających lęk w porównaniu z ich rodzeństwem. Jednak gdy łapy poddano skalibrowanemu naciskowi mechanicznego, zarówno samce, jak i samice mutantów potrzebowały silniejszej siły, by się wycofać, ujawniając selektywne obniżenie wrażliwości na szkodliwe bodźce mechaniczne. W przeciwieństwie do tego, reakcje na ciepło i większość testów zimna nie uległy zmianie, a zachowania związane z bólem zapalnym były tylko nieznacznie nasilone u samic w pierwszych minutach po wstrzyknięciu formaliny. Taki wzór sugeruje, że Ndfip2 precyzyjnie dostraja specyficzny kanał bólu — szkodliwy nacisk — zamiast ogólnie tłumić wszystkie formy odczuwania.
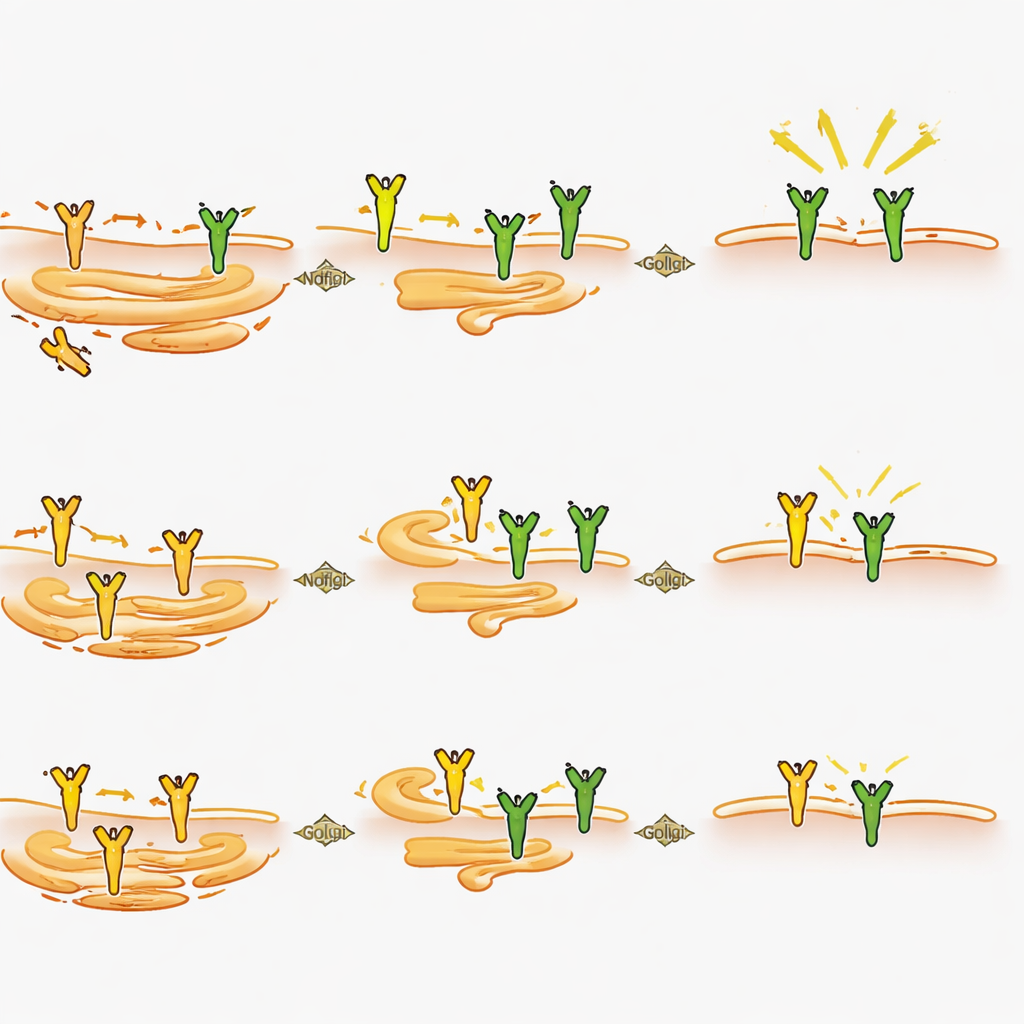
Jak Ndfip2 kształtuje sygnał bólowy od wnętrza komórki
Dokładniejsze badania neuronów wykazały, że usunięcie Ndfip2 obniża całkowitą ilość białka TrkA w dorosłych zwojach rdzeniowych, szczególnie u samców, choć gen TrkA był nadal wyrażany na normalnym poziomie. W hodowanych neuronach utrata Ndfip2 zmniejszała zarówno poziomy TrkA, jak i siłę sygnalizacji wywoływanej przez NGF, ponownie silniej u samców. Zaskakująco efekt ten nie wynikał ze zmian w typowym znakowaniu TrkA kierującym je do degradacji. Zamiast tego eksperymenty w komórkach ujawniły, że nadmiar Ndfip2 powoduje akumulację TrkA w nieodmierzonym, niezglykozylowanym stanie, jednocześnie zmniejszając w pełni przetworzone formy, które normalnie trafiają na powierzchnię komórki. Zgodnie z tym, zmniejszenie Ndfip2 w neuronach zwiększało u samców ułamek TrkA obecnego w błonie komórkowej. Razem te obserwacje wskazują, że Ndfip2 reguluje chemiczne dojrzewanie i trasowanie TrkA wewnątrz komórki, a tym samym kontroluje, ile funkcjonalnego receptora jest dostępne do wykrywania NGF.
Co to oznacza dla przyszłych terapii bólu
Odkrycie Ndfip2 jako wewnętrznego regulatora układu NGF–TrkA dodaje nową warstwę zrozumienia mechanizmów kalibracji czułości bólowej, zwłaszcza wobec szkodliwych bodźców mechanicznych. Zamiast całkowicie blokować NGF, wpływanie na Ndfip2 lub pokrewne etapy dojrzewania TrkA może pozwolić klinicystom delikatnie zmniejszyć nadmierną sygnalizację w określonych szlakach bólowych, zachowując jednocześnie ochronną funkcję bólu. Zaobserwowane różnice płciowe w poziomach i efektach Ndfip2 podkreślają także znaczenie dopasowywania przyszłych terapii bólowych do kontekstu biologicznego, zamiast zakładać uniwersalne rozwiązania.
Cytowanie: Cañada-García, D., Hernández-García, A., Vicente-García, C. et al. Ndfip2 in TrkA-expressing sensory neurons regulates noxious mechanosensation through control of TrkA signaling and protein levels. Cell Death Dis 17, 437 (2026). https://doi.org/10.1038/s41419-026-08670-9
Słowa kluczowe: ból mechaniczny, neurony czuciowe, czynnik wzrostu nerwów, receptor TrkA, regulacja potranslacyjna